МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ВИЧ-ИНФЕКЦИЯ У ДЕТЕЙ
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: B20, B21, B22, B23, B24, R75, Z21, Z20.6
Год утверждения (частота пересмотра): 2024
Возрастная категория: Дети
Пересмотр не позднее: 2026
ID: 459
Разработчик клинической рекомендации
- Национальная ассоциация специалистов по профилактике, диагностике и лечению ВИЧ-инфекции
Одобрено Научно-практическим Советом Минздрава РФ
Список сокращений
АГ Антиген
АРВП Антиретровирусные препараты (АТХ: J05A противовирусные препараты прямого действия)
АРТ Антиретровирусная терапия
АТ Антитело
АТХ Анатомо-терапевтическо-химическая классификация, рекомендованная Всемирной Организацией Здравоохранения
в/в Внутривенное введение
ВГ Вирусный гепатит
ВГВ Вирусный гепатит B
ВГС Вирусный гепатит C
ВИЧ Вирус иммунодефицита человека
ВН Вирусная нагрузка
ВПГ Вирус простого герпеса
ВСВИС Воспалительный синдром восстановления иммунной системы
ВОЗ Всемирная Организация Здравоохранения
ДН Диспансерное наблюдение
ДНК Дезоксирибонуклеиновая кислота
ДУ Диспансерный учет
ЖКТ Желудочно-кишечный тракт
ИБ Иммунный блоттинг
ИВ Ингибитор внедрения (АТХ: J05AX прочие противовирусные препараты)
ИД Иммунодефицит
ИИ Ингибиторы интегразы ВИЧ (АТХ: J05AJ ингибиторы интегразы)
ИК Иммунная категория
ИМТ Индекс массы тела
ИП Ингибиторы протеазы ВИЧ (АТХ: J05AE ингибиторы протеаз)
ИРИ Иммунорегуляторный индекс, соотношение CD4- и CD8-T-лимфоцитов
ИФА Иммуноферментный анализ
ИХЛА Иммунохемилюминесцентный анализ
КОП Количественная оценка приверженности
КР Когнитивные расстройства
КТ Компьютерная томография
МЕ Международные единицы
МЗ Министерство здравоохранения
МКБ-10 Международная статистическая классификация болезней и проблем, связанных со здоровьем, 10-й пересмотр
МНО международное нормализованное отношение
МО Медицинская организация
МРТ Магнитно-резонансная томография
МТ Масса тела
НИОТ Нуклеозидные (нуклеотидные) ингибиторы обратной транскриптазы ВИЧ (Нуклеозиды и нуклеотиды - ингибиторы обратной транскриптазы ВИЧ, АТХ: J05AF)
НК Нуклеиновая кислота
НКР Нейрокогнитивные расстройства
ННИОТ Ненуклеозидные ингибиторы обратной транскриптазы ВИЧ (АТХ: J05AG)
НР Нежелательная реакция
НЯ Нежелательное явление
ПКП Постконтактная профилактика
ПМР Передача ВИЧ от матери ребенку
ППМР Профилактика передачи ВИЧ от матери ребенку
ППТ Площадь поверхности тела
ПТ Поверхность тела
ПЦР Полимеразная цепная реакция
РК Российская клиническая классификация ВИЧ-инфекции, 2006 г
РНК Рибонуклеиновая кислота
РС Раз в сутки (кратность назначения)
РФ Российская Федерация
СП Санитарные правила
СПИД Синдром приобретенного иммунодефицита
Ф-АЗТ Фосфазид <**> (АТХ: J05AF)
ФКД Фиксированные комбинации доз
ФО Федеральный округ
ЦМВ Цитомегаловирусная инфекция
ЦНС Центральная нервная система
3TC Ламивудин <**> (АТХ: J05AF05)
ABC Абакавир <**> (АТХ: J05AF06)
ATV Атазанавир <**> (АТХ: J05AE08)
BIC + TAF + FTC Биктегравир + тенофовира алафенамид + эмтрицитабин <**> (комбинированный препарат) (АТХ: J05AR20)
CD4 T-лимфоциты с рецептором CD4
CD8 T-лимфоциты с рецептором CD8
DRV Дарунавир <**> (АТХ: J05AE10)
DTG Долутегравир <**> (АТХ: J05AX12)
EFV Эфавиренз <**> (АТХ: J05AG03)
EMA Европейское Медицинское Агентство
ETR Этравирин <**> (АТХ: J05AG04)
FDA Администрация по пищевым и лекарственным продуктам США
FPV Фосампренавир <**> (АТХ: J05AE07)
FTC Эмтрицитабин <**> (АТХ: J05AF09)
EVG + COBI + TAF + FTC Кобицистат + Тенофовира алафенамид + Элвитегравир + Эмтрицитабин <**> (комбинированный препарат) (АТХ: J05AR09)
HADS Госпитальная шкала оценки тревоги и депрессии
HLA-B*5701 Аллель 5701 локуса B главного комплекса гистосовместимости человека
LPV + r Лопинавир + Ритонавир <**> (комбинированный препарат) (АТХ: J05AR10)
NVP Невирапин <**> (АТХ: J05AG01)
PedsQL Тест для оценки качества жизни у детей
PENTA Педиатрическая Европейская Сеть по Лечению ВИЧ-инфекции
RAL Ралтегравир <**> (АТХ: J05AX08)
RPV Рилпивирин (АТХ: J05AG05)
RTV,/r Ритонавир <**> (АТХ: J05AE03)
TAF Тенофовира алафенамид <**> (АТХ: J05AF13)
TDF Тенофовир <**> (активное вещество: тенофовира дизопроксила фумарат (J05AF07)
TMP + SMX Ко-тримоксазол [Сульфаметоксазол + Триметоприм] <**> (АТХ: J01EE01)
XTC Или 3TC (ламивудин <**>), или FTC (эмтрицитабин)
ZDV Зидовудин <**> (АТХ: J05AF01)
--------------------------------
<**> Препарат включен в Перечень жизненно необходимых и важнейших лекарственных препаратов для медицинского применения
Термины и определения
Люди, живущие с ВИЧ-инфекцией - собирательное понятие, определяющее принадлежность человека (людей) к группе инфицированных ВИЧ.
Серодискордантные пары - пары, поддерживающие продолжительные сексуальные взаимоотношения, в которых только один из партнеров имеет ВИЧ-инфекцию.
Возраст
Перинатальный период - с 22 недели гестации до 7-го дня жизни
Период новорожденности - первые 28 дней жизни
Детский возраст - с рождения до 17 лет 11 месяцев 29 дней
Младенческий возраст - первый год жизни
Подростковый возраст - с 10 лет до 17 лет 11 месяцев 29 дней (младший - 10 - 13 лет, старший - 14 - 17 лет).
Вирус
Вирус иммунодефицита человека - возбудитель ВИЧ-инфекции из группы ретровирусов, семейства лентивирусов, вызывающий постепенное развитие иммунодефицита.
Вирусная нагрузка - показатель репликативной активности вируса, количество копий РНК ВИЧ в 1 мл биологической жидкости пациента (кровь, ликвор и т.д.). При неопределяемом уровне вирусной нагрузки количество копий РНК ВИЧ ниже порога чувствительности тест-системы, при определяемом уровне - выше порога чувствительности тест-системы. Используется для оценки эффективности АРТ; при этом рекомендуется использовать тест-системы с порогом чувствительности не выше 50 копий/мл плазмы.
Вирусологическая супрессия - цель АРТ, заключающаяся в снижении и поддержании вирусной нагрузки в крови ниже уровня, выявляемого при использовании высокочувствительных тест-систем (РНК ВИЧ < 50 копий/мл плазмы).
Вирусологическая неудача - невозможность достичь или поддерживать вирусную нагрузку на уровне < 200 копий/мл плазмы через 24 недели АРТ.
Вирусологическая реверсия - продолжающееся повышение вирусной нагрузки > 200 копий/мл плазмы после достижения вирусологической супрессии на фоне АРТ.
Вирусологический подскок - изолированное выявление определяемого уровня ВН у пациентов с вирусологической супрессией (не выше 500 копий/мл), после которого следует возврат к неопределяемой ВН. Связан со спонтанной активацией репликативной активности ВИЧ.
Неполный вирусологический ответ - дважды подтвержденная ВН > 200 копий/мл плазмы через 24 недели АРТ у пациента, не достигшего вирусологической супрессии.
Низкоуровневая виремия - сохраняющийся на фоне АРТ определяемый уровень вирусной нагрузки < 200 копий/мл плазмы.
Вертикальная передача
Перинатальный контакт по ВИЧ-инфекции - контакт ребенка с ВИЧ-инфицированной матерью на протяжении периода гестации, родов и грудного вскармливания. Традиционно перинатальный период продолжается с 22 недель гестации до 7-го дня жизни ребенка включительно. Понятие "вертикальное инфицирование" подразумевает заражение во время беременности и родов. Понятие "перинатальный контакт по ВИЧ-инфекции" введено в связи с отсутствием подходящего термина для объединения в одну группу всех детей, заразившихся от матерей естественным путем - в течение беременности, во время родов и при грудном вскармливании.
Профилактика передачи ВИЧ-инфекции от матери ребенку - комплекс мер для предупреждения ВИЧ-инфицирования плода и ребенка от матери во время беременности, родов и грудного вскармливания.
Диагностика
Иммунный блоттинг - лабораторный метод определения в крови антител к различным антигенам ВИЧ раздельно по каждому. Используется как подтверждающий метод при получении положительного результата ИФА или ИХЛА.
Иммуноферментный анализ и иммунохемилюминесцентный анализ - лабораторные методы определения в крови антител к ВИЧ.
Полимеразная цепная реакция - лабораторный метод качественного и количественного определения генетического материала ВИЧ, основанный на использовании уникальности нуклеотидных последовательностей участков РНК/ДНК. Обладает высокой чувствительностью и специфичностью. Качественное определение ДНК ВИЧ в лимфоцитах крови используется у взрослых для раннего выявления ВИЧ-инфекции в установленном/предполагаемом периоде "серологического окна" (в первые недели после инфицирования, когда количество вырабатываемых специфических антител к ВИЧ в организме заразившегося человека недостаточно для выявления). Количественное определение РНК ВИЧ используется при выборе препаратов в составе схем АРТ, для оценки эффективности АРТ и с прогностической целью (см. "Вирусная нагрузка"). Молекулярные методы являются основными при ранней диагностике у детей, рожденных ВИЧ-серопозитивными матерями.
Иммунология
Иммунный статус - оценка состояния иммунной системы. При ВИЧ-инфекции исследуют процентное содержание и абсолютное количество иммунных клеток регуляторного звена (CD4+ T-лимфоциты) и эффекторного звена (CD8+ T-лимфоциты), наиболее важных в патогенезе заболевания. Используется для мониторинга естественного течения ВИЧ-инфекции и оценки эффективности АРТ. Процентное содержание определяется по отношению к общему содержанию лейкоцитов. Абсолютное число выражается в количестве клеток в 1 микролитре, т.е. 1 мм3.
Иммунорегуляторный индекс - соотношение абсолютного количества CD4+- и CD8+- T-лимфоцитов. У лиц с сохранной иммунной системой значение ИРИ равно или выше 1. При ВИЧ-инфекции происходит инверсия показателя за счет снижения доли CD4+- T-лимфоцитов; прогрессирование поражения иммунной системы сопровождается снижением ИРИ. Используется в прогностических целях.
CD4+- T-лимфоциты (дословно "кластер дифференцировки N 4") - трансмембранный гликопротеин, молекула на поверхности регуляторных T-лимфоцитов (T-хелперов), которая в качестве корецептора участвует в осуществлении этими клетками иммунных функций и служит маркером при исследовании субпопуляций T-лимфоцитов. CD4 выполняют функции "дирижеров иммунного ответа".
CD8+- T-лимфоциты (дословно "кластер дифференцировки N 8") - трансмембранный гликопротеин, молекула на поверхности эффекторных T-лимфоцитов (цитотоксических лимфоцитов), которая в качестве корецептора участвует в осуществлении этими клетками иммунных функций и служит маркером при исследовании субпопуляций T-лимфоцитов. CD8 лизируют клетки - мишени, несущие на поверхности чужеродные антигены или измененные аутоантигены.
Лечение
Антиретровирусная терапия - этиотропная терапии инфекции, вызванной вирусом иммунодефицита человека (ВИЧ-инфекции), позволяющая добиться контролируемого течения заболевания, назначаемая пожизненно и основанная на одновременном использовании нескольких антиретровирусных препаратов, действующих на разные этапы жизненного цикла ВИЧ.
Предполагаемая терапия ВИЧ-инфекции у новорожденных - назначение трехкомпонентной схемы АРТ новорожденным с высоким риском заражения ВИЧ. Предполагаемая терапия ВИЧ является ранним началом лечения для тех детей, у которых будет подтверждена ВИЧ-инфекция. Также она является постконтактной профилактикой и предотвращает заражение ребенка вирусом иммунодефицита человека от матери.
Мутации устойчивости - изменения в геноме структурных и функциональных (ферменты) компонентах ВИЧ, делающие его менее чувствительным к антиретровирусным препаратам.
Резистентность (устойчивость) - нечувствительность ВИЧ к антиретровирусному препарату (препаратам).
Перекрестная резистентность - наличие общих мутаций устойчивости у нескольких препаратов одного класса.
Барьер резистентности - способность антиретровирусного препарата сохранять активность по отношению к ВИЧ при формировании в его геноме мутаций устойчивости.
Нежелательная реакция - непреднамеренная неблагоприятная реакция организма, связанная с применением лекарственного средства, предполагающая наличие, как минимум, возможной взаимосвязи с применением подозреваемого лекарственного препарата.
Нежелательное явление - любое неблагоприятное изменение в состоянии здоровья пациента, которому назначался лекарственный препарат, независимо от причинно-следственной связи с его применением. Нежелательное явление может представлять собой любое неблагоприятное и непреднамеренное изменение (например, отклонение лабораторного показателя от нормы), симптом или заболевание, возникшее во время применения лекарственного препарата, вне зависимости от наличия или отсутствия взаимосвязи с применением лекарственного препарата.
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
ВИЧ-инфекция - болезнь, вызванная вирусом иммунодефицита человека - антропонозное инфекционное хроническое заболевание, характеризующееся специфическим поражением иммунной системы, приводящим к медленному ее разрушению до формирования синдрома приобретенного иммунодефицита (СПИД), сопровождающегося развитием оппортунистических инфекций и вторичных злокачественных новообразований [1].
СПИД - состояние, развивающееся на фоне ВИЧ-инфекции и характеризующееся появлением одного или нескольких заболеваний, отнесенных к СПИД-индикаторным. СПИД является эпидемиологическим понятием и используется в целях эпидемиологического надзора за ВИЧ-инфекцией [1].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Возбудитель ВИЧ-инфекции - вирус иммунодефицита человека - относится к подсемейству лентивирусов семейства ретровирусов. Существует два типа вируса: ВИЧ-1 и ВИЧ-2.
ВИЧ-инфекцию вызывает РНК-содержащий вирус, относящийся к семейству ретровирусов, роду лентивирусов. ВИЧ попадает в организм с такими инфицированными жидкостями как кровь, грудное молоко, семенная жидкость и вагинальные выделения. Мишенями для ВИЧ являются клетки-носители рецептора CD4, основными представителями которых являются иммунорегуляторные лимфоциты T-хелперы. Последующее развитие инфекционного процесса приводит постепенному снижению уровня CD4 и ИРИ. В результате этого ВИЧ, с одной стороны, подрывает защитную функцию иммунной системы человека, а с другой - создает условия для персистирования неспецифической воспалительной активации. Кроме того, CD4-рецепторы есть и на некоторых других клетках - моноцитах, эозинофилах, мегакариоцитах, клетках Лангерганса, альвеолярных макрофагах легких, дендритных клетках головного мозга эпителиальных клетках кишечника и шейки матки. Все они, наряду с T-лимфоцитами, также являются клетками-мишенями для ВИЧ и многие из них, имея более длительное время жизни, выступают в качестве резервуаров ВИЧ в организме инфицированного человека.
Итогом поражения CD4-несущих клеток является спектр заболеваний нарушенного гомеостаза: от несостоятельности противомикробной и противоопухолевой защиты до заболеваний хронического воспаления с поражением всех органов и систем. Не связанными напрямую с ВИЧ-инфекцией состояниями являются аутоиммунные реакции, болезни иммунных комплексов и метаболические нарушения, приводящие к поражению эндотелия сосудов и соединительной ткани. Таким образом, прогрессирование заболевания ведет к появлению ВИЧ-связанных вторичных инфекций и опухолей, а также связанных и несвязанных с ВИЧ заболеваний - кардиоваскулярной, неврологической, почечной и костно-суставной патологии.
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Источником ВИЧ-инфекции являются люди, инфицированные ВИЧ на любой стадии заболевания, в том числе в инкубационном периоде.
Механизм и факторы передачи
ВИЧ-инфекция может передаваться при реализации как естественного, так и искусственного механизма передачи.
К естественному механизму передачи ВИЧ относятся:
- контактный, который реализуется преимущественно при половых контактах (как при гомо-, так и гетеросексуальных) и при контакте слизистой или раневой поверхности с кровью;
- вертикальный (инфицирование ребенка от ВИЧ-инфицированной матери: во время беременности, в родах и при грудном вскармливании).
К искусственному механизму передачи относятся:
- артифициальный при немедицинских инвазивных процедурах, в том числе внутривенном введении наркотиков (использование шприцев, игл, другого инъекционного оборудования и материалов), нанесение татуировок, при проведении косметических, маникюрных и педикюрных процедур нестерильным инструментарием;
- артифициальный при инвазивных вмешательствах в медицинских организациях. Инфицирование ВИЧ может осуществляться при переливании крови, ее компонентов и препаратов, пересадке органов и тканей, использования донорской спермы, донорского грудного молока от ВИЧ-инфицированного донора, а также через медицинский инструментарий для парентеральных вмешательств, изделия медицинского назначения, контаминированные ВИЧ и не подвергшиеся обработке в соответствии с требованиями нормативных документов.
Основными факторами передачи возбудителя являются биологические жидкости человека (кровь, компоненты крови, сперма, вагинальное отделяемое, грудное молоко).
Особенности эпидемического процесса ВИЧ-инфекции в России на современном этапе
Доля потребителей инъекционных наркотиков в структуре первичных больных ВИЧ-инфекцией в 2018 г. снизилась до 39%, ВИЧ-инфекция вышла за пределы традиционных групп повышенного риска в общую популяцию. В настоящее время прослеживается тенденция к росту удельного числа женщин в структуре инфицированных ВИЧ, в 2018 году доля женщин составила 41% [2 - 4]. Увеличение бремени ВИЧ-инфекции среди женщин фертильного возраста и рост числа родов у ВИЧ-положительных женщин обуславливают ежегодный прирост числа детей с установленным диагнозом ВИЧ-инфекции, сохраняющийся, несмотря на значительные успехи в ППМР [2, 5].
По данным учетных форм государственного статистического наблюдения к концу 2020 года в России выявлено более 10 тысяч ВИЧ-инфицированных детей [2, 5 - 7]. Для детей первых лет жизни основным фактором риска заражения является рождение от ВИЧ-инфицированной матери. Для детей подросткового возраста пути передачи такие же, как и у взрослых - половые контакты с больными ВИЧ-инфекцией и внутривенное употребление психоактивных веществ. Для детей всех возрастных групп возможными путями инфицирования являются переливание крови и ее препаратов и использование контаминированного ВИЧ медицинского инструментария.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
В Международной классификации болезней и проблем, связанных со здоровьем, 10-го пересмотра предусмотрены коды для различных состояний и медицинских услуг, связанных с ВИЧ-инфекцией [8, 9]. Кодирование предназначено для статистического учета и не предполагает определение тяжести течения или прогноза заболевания. При практическом использовании кодов МКБ им могут соответствовать различные категории или стадии в клинических классификациях ВИЧ-инфекции.
B20 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде инфекционных и паразитарных болезней:
B20.0 Болезнь, вызванная ВИЧ, с проявлениями микобактериальной инфекции;
B20.1 Болезнь, вызванная ВИЧ, с проявлениями других бактериальных инфекций;
B20.2 Болезнь, вызванная ВИЧ, с проявлениями цитомегаловирусного заболевания;
B20.3 Болезнь, вызванная ВИЧ, с проявлениями других вирусных инфекций;
B20.4 Болезнь, вызванная ВИЧ, с проявлениями кандидоза;
B20.5 Болезнь, вызванная ВИЧ, с проявлениями других микозов;
B20.6 Болезнь, вызванная ВИЧ, с проявлениями пневмонии, вызванной Pneumocystis jirovecii;
B20.7 Болезнь, вызванная ВИЧ, с проявлениями множественных инфекций;
B20.8 Болезнь, вызванная ВИЧ, с проявлениями других инфекционных и паразитарных болезней;
B20.9 Болезнь, вызванная ВИЧ, с проявлениями неуточненных инфекционных и паразитарных болезней;
B21 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде злокачественных новообразований:
B21.0 Болезнь, вызванная ВИЧ, с проявлениями саркомы Капоши;
B21.1 Болезнь, вызванная ВИЧ, с проявлениями лимфомы Беркитта;
B21.2 Болезнь, вызванная ВИЧ, с проявлениями других неходжкинских лимфом;
B21.3 Болезнь, вызванная ВИЧ, с проявлениями других злокачественных новообразований лимфатической, кроветворной и родственных им тканей;
B21.7 Болезнь, вызванная ВИЧ, с проявлениями множественных злокачественных новообразований;
B21.8 Болезнь, вызванная ВИЧ, с проявлениями других злокачественных новообразований;
B21.9 Болезнь, вызванная ВИЧ, с проявлениями неуточненных злокачественных новообразований;
B22 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде других уточненных болезней:
B22.0 Болезнь, вызванная ВИЧ, с проявлениями энцефалопатии;
B22.1 Болезнь, вызванная ВИЧ, с проявлениями лимфатического интерстициального пневмонита;
B22.2 Болезнь, вызванная ВИЧ, с проявлениями изнуряющего синдрома;
B22.7 Болезнь, вызванная ВИЧ, с проявлениями множественных болезней, классифицированных в других рубриках;
B23 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], проявляющаяся в виде других состояний:
B23.0 Острый ВИЧ-инфекционный синдром;
B23.1 Болезнь, вызванная ВИЧ, с проявлениями персистентной генерализованной лимфаденопатии;
B23.2 Болезнь, вызванная ВИЧ, с проявлениями гематологических и иммунологических нарушений, не классифицированных в других рубриках;
B23.8 Болезнь, вызванная ВИЧ, с проявлениями других уточненных состояний;
B24 Болезнь, вызванная вирусом иммунодефицита человека [ВИЧ], неуточненная.
R75 Лабораторное обнаружение вируса иммунодефицита человека [ВИЧ].
Z20.6 Контакт с больным и возможность заражения вирусом иммунодефицита человека [ВИЧ].
Z21 Бессимптомный инфекционный статус, вызванный вирусом иммунодефицита человека [ВИЧ].
При постановке диагноза ВИЧ-инфекции нецелесообразно использовать код Z21 у детей с подтвержденной ВИЧ-инфекцией. Основными кодами формы N 61 статистического наблюдения МКБ-10, используемыми в Российской Федерации при составлении медицинской отчетности о больных ВИЧ-инфекцией (2), являются коды B20 - B24. Поскольку в настоящее время научно доказано отсутствие возможности носительства вируса иммунодефицита человека, а обнаружение в организме человека ВИЧ свидетельствует о наличии заболевании с различной скоростью прогрессирования, использование кода Z21 в отношении пациентов с подтвержденным диагнозом ВИЧ-инфекции некорректно. Вместо него рекомендуется использование кодов B23.1, B23.2 [10].
У детей с перинатальным контактом по ВИЧ-инфекции используются коды МКБ-10 R75 и Z20.6 (R75/Z20.6) [9].
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Согласно действующей в России классификации ВИЧ-инфекции стадия и фаза заболевания устанавливается только на основании клинических проявлений - по наличию и значимости вторичных заболеваний. Уровень ВН и количество CD4 не являются критериями для определения клинической стадии или фазы заболевания [10 - 12].
Российская клиническая классификация (РК) ВИЧ-инфекции
1 Стадия инкубации
2 Стадия первичных проявлений:
2А. Бессимптомная;
2Б Острая ВИЧ-инфекция без вторичных заболеваний;
2В Острая ВИЧ-инфекция с вторичными заболеваниями
3 Субклиническая стадия
4 Стадия вторичных заболеваний:
4А Потеря массы тела < 10%; грибковые, вирусные, бактериальные поражения кожи и слизистых оболочек; опоясывающий герпес; повторные фарингиты, синуситы
- фаза прогрессирования (на фоне отсутствия АРТ; на фоне АРТ);
- фаза ремиссии (спонтанная; после ранее проводимой АРТ; на фоне АРТ)
4Б Потеря массы тела > 10%; необъяснимые диарея или лихорадка длительностью более 1 месяца; повторные стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних органов; локализованная саркома Капоши; повторный или диссеминированный опоясывающий герпес
- фаза прогрессирования (на фоне отсутствия АРТ; на фоне АРТ);
- фаза ремиссии (спонтанная; после ранее проводимой АРТ; на фоне АРТ)
4В Кахексия; генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания; пневмоцистная пневмония; кандидоз пищевода, бронхов, трахеи, легких; злокачественные опухоли; поражения центральной нервной системы
- фаза прогрессирования (на фоне отсутствия АРТ; на фоне АРТ);
- фаза ремиссии (спонтанная; после ранее проводимой АРТ; на фоне АРТ)
В варианте классификации, утвержденной Приказом Минздравсоцразвития России от 17 марта 2006 г N 166 [11], предусматривалась также стадия 5 - "терминальная". Однако в настоящее время в связи с появлением эффективной АРТ постановка этой стадии не рекомендуется [10].
В случае, если на фоне ВИЧ-инфекции хотя бы одно из вторичных заболеваний имеет степень проявления, соответствующую критериям синдрома приобретенного иммунодефицита (всего 28), после фазы заболевания указывается СПИД [10, 11].
Перечень состояний, свидетельствующих о наличии у пациента СПИДа [10 - 15]:
1. Бактериальные инфекции (множественные или возвратные) у ребенка в возрасте до 13 лет;
2. Кандидоз пищевода;
3. Кандидоз трахеи, бронхов или легких;
4. Рак шейки матки (инвазивный);
5. Кокцидиомикоз (диссеминированный или внелегочный);
6. Внелегочный криптококкоз;
7. Криптоспоридиоз кишечника с диареей > 1 месяца;
8. Цитомегаловирусная инфекция (с поражением других органов, кроме печени, селезенки, лимфатических узлов) у пациента в возрасте старше одного месяца;
9. Цитомегаловирусный ретинит с потерей зрения;
10. Энцефалопатия, обусловленная действием ВИЧ;
11. Инфекция, обусловленная вирусом простого герпеса: хронические язвы, сохраняющиеся более 1 мес., или бронхит, пневмония, эзофагит у пациента в возрасте старше одного месяца;
12. Гистоплазмоз диссеминированный или внелегочный;
13. Изоспороз кишечника (с диареей длительностью более 1 мес.);
14. Саркома Капоши;
15. Интерстициальная лимфоидная пневмония у ребенка в возрасте до 13 лет;
16. Лимфома Беркитта;
17. Иммунобластная лимфома;
18. Лимфома мозга первичная;
19. Микобактериозы, вызванные M. kansasii, M. avium-intracellulare, диссеминированные или внелегочные;
20. Туберкулез легких у пациента старше 13 лет (российские критерии случаев, в которых туберкулез следует рассматривать как проявление СПИДа у пациентов с ВИЧ-инфекцией: выраженный иммунодефицит, подтвержденный лабораторными методами или диагностируемый на основании клинических проявлений ВИЧ-инфекции; диссеминация туберкулезного процесса; значительное снижение реактивности, регистрируемое при морфологическом исследовании тканей, вовлеченных в туберкулезный процесс, например, лимфатического узла);
21. Туберкулез внелегочный (российские критерии случаев, в которых туберкулез следует рассматривать как проявление СПИДа у больных ВИЧ-инфекцией - см. п. 20);
22. Другие не дифференцированные диссеминированные или внелегочные микобактериозы;
23. Пневмоцистная пневмония;
24. Пневмонии возвратные (две и более в течение 12 месяцев);
25. Прогрессирующая многоочаговая лейкоэнцефалопатия;
26. Сальмонеллезные (не тифоидные) септицемии возвратные;
27. Токсоплазмоз мозга у пациента в возрасте старше одного месяца;
28. Синдром истощения, обусловленный ВИЧ.
Классификация иммунных нарушений
У детей с ВИЧ-инфекцией выделяют 4 степени состояния иммунной системы - без иммуносупрессии, умеренная иммуносупрессия, выраженная иммуносупрессия и тяжелая иммуносупрессия. Оценка иммунного статуса проводится по результатам исследования абсолютного количества и процентного содержания CD4-лимфоцитов в зависимости от возраста ребенка (таблица 1) [10, 12 - 17].
Таблица 1. Классификация иммунных категорий у детей в соответствии с возрастом
|
Иммунные категории
|
CD4 в микролитре (клеток в мм3 и %)
|
||
|
< 12 месяцев
|
1 - 5 лет
|
>= 6 лет
|
|
|
Категория 1
Без иммуносупрессии
|
> 1500
> 35%
|
> 1000
> 30%
|
> 500
> 25%
|
|
Категория 2
Умеренная иммуносупрессия
|
1000 - 1500
30 - 35%
|
750 - 999
25 - 30%
|
350 - 499
20 - 25%
|
|
Категория 3
Выраженная иммуносупрессия
|
750 - 999
25 - 29%
|
500 - 749
20 - 24%
|
200 - 349
15 - 19%
|
|
Категория 4
Тяжелая иммуносупрессия
|
< 750
< 25%
|
< 500
< 20%
|
< 200
< 15%
|
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Ниже представлено клиническое течение ВИЧ-инфекции без применения АРТ.
Инкубационный период. Это период от момента заражения до ответа организма на внедрение вируса (появление клинической симптоматики или выработки антител), обычно составляет 1 - 3 месяца, однако при наличии иммунодефицитных состояний у пациента на фоне лечения противоопухолевыми препаратами L01 (цитостатиками) или антиретровирусными препаратами может увеличиваться до 12 месяцев. В данном периоде у инфицированного антитела к ВИЧ не обнаруживаются, в связи с чем возрастает риск передачи от него инфекции, в том числе при оказании медицинской помощи.
Первичные проявления ВИЧ-инфекции. У 30 - 50% инфицированных появляются симптомы острой ВИЧ-инфекции, которая сопровождается различными проявлениями: лихорадка, лимфаденопатия, неспецифические (пятнисто-папулезные, уртикарные, петехиальные) высыпания на коже и слизистых, миалгии или артралгии, диарея, головная боль, тошнота и рвота, увеличение печени и селезенки, менингеальный синдром. Эти симптомы проявляются на фоне высокой вирусной нагрузки и снижения количества CD4 лимфоцитов в разных сочетаниях, имеют разную степень выраженности и продолжительность. В редких случаях уже на этой стадии при отсутствии антиретровирусной терапии могут развиваться тяжелые вторичные заболевания, приводящие к гибели пациентов. В данном периоде возрастает частота обращаемости инфицированных в медицинские организации; риск передачи инфекции - высокий в связи с высокой вирусной нагрузкой, большим количеством вируса в крови.
В соответствии с РК Стадия 2 может иметь несколько вариантов течения. Вариант 2А (бессимптомная), характеризуется отсутствием каких-либо клинических проявлений ВИЧ-инфекции и проявляется лишь выработкой антител (сероконверсией). Вариант 2Б, острая инфекция без вторичных заболеваний, проявляется разнообразной клинической симптоматикой: лихорадка, полиморфные высыпания на коже и слизистых, лимфоаденопатия, фарингит, гепатоспленомегалия, диарея, менингизм. Иногда такой вариант течения называют "мононуклеозоподобный синдром", т.к. в крови в этот период могут обнаруживаться мононуклеары. Яркая симптоматика выявляется у 15 - 30% больных, у остальных имеет место 1 - 2 из вышеперечисленных симптомов в любых сочетаниях. При этом варианте часто регистрируется транзиторное снижение уровня CD4. Вариант 2В, острая инфекция с вторичными заболеваниями, характеризуется значительным снижением уровня CD4, и в результате иммунодефицита появляются вторичные заболевания различной этиологии (кандидозы, герпетическая инфекция и т.д.). Их проявления, как правило, слабо выражены и кратковременны, но у младенцев, особенно при внутриутробном инфицировании, могут быть тяжелыми (сепсис, пневмоцистная пневмония) и даже фатальными.
В прогностическом плане бессимптомное течение стадии первичных проявлений ВИЧ-инфекции является более благоприятным. Чем раньше в отношении гестационного возраста ребенка произошло инфицирование, тем тяжелее протекает эта стадия и тем больше вероятность быстрого прогрессирования ВИЧ-инфекции и гибели пациента при отсутствии АРТ.
Субклиническая стадия. В этой стадии инфицированный длительно является источником инфекции. Характеризуется медленным падением CD4 и низкой скоростью репликации ВИЧ. Основным клиническим проявлением является персистирующая генерализованная лимфоаденопатия, для которой характерно увеличение не менее двух лимфоузлов не менее чем в двух не связанных между собой группах (не считая паховых), у детей до размера в диаметре более 0,5 см, сохраняющееся в течение не менее 3-х месяцев. При осмотре лимфатические узлы обычно бывают эластичными, безболезненными, не спаянными с окружающей тканью, кожа над ними не изменена.
Длительность субклинической стадии варьирует от 2-х до 20-ти и более лет, но в среднем она продолжается 6 - 7 лет. У детей с перинатальным инфицированием эта стадия может отсутствовать, когда ВИЧ-инфекция в стадии первичных проявлений имеет неуклонное прогрессирующее течение.
Стадия вторичных заболеваний. На фоне продолжающейся репликации ВИЧ и нарастающего иммунодефицита появляются вторичные заболевания (инфекционные, аутоиммунные, онкологические). Заболевания инфекциями вирусной, бактериальной, грибковой природы сначала протекают довольно благоприятно и купируются обычными терапевтическими средствами; первоначально это преимущественно поражения кожи и слизистых. По мере прогрессирующего снижения CD4-лимфоцитов развиваются органные и генерализованные поражения, приводящие к смерти пациента при отсутствии АРТ.
В соответствии с РК для стадии 4А характерны бактериальные, грибковые и вирусные поражения слизистых и кожных покровов, воспалительные заболевания верхних дыхательных путей. При стадии 4Б кожные поражения носят более глубокий характер и склонны к затяжному течению. Начинают развиваться поражения внутренних органов и периферической нервной системы, локализованная саркома Капоши. Стадия 4В характеризуется развитием тяжелых, угрожающих жизни вторичных заболеваний, их генерализованным характером, поражением центральной нервной системы. Спонтанно или вследствие проводимой терапии клинические проявления вторичных заболеваний могут исчезать. Поэтому в этой стадии выделяют фазы прогрессирования (в отсутствие антиретровирусной терапии или на фоне антиретровирусной терапии) и ремиссии (спонтанной, после ранее проводимой антиретровирусной терапии или на фоне антиретровирусной терапии).
В педиатрической практике скорость развития инфекционного процесса отличается от естественного течения ВИЧ-инфекции у взрослых в сторону более быстрого прогрессирования у детей младшего возраста. Также у детей первым признаком прогрессирования ВИЧ-инфекции может выступать задержка физического и/или психомоторного развития, опережая развернутую клинику вторичных заболеваний.
Наиболее типичные проявления ВИЧ-инфекции у детей (по стадиям РК, 2006 г.) [13 - 16, 18, 19]:
В стадии 3:
- персистирующая генерализованная лимфоаденопатия.
В стадии 4А:
- снижение массы тела менее чем на 10%;
- длительная необъяснимая гепатоспленомегалия;
- грибковое поражение ногтей;
- ангулярный хейлит;
- рецидивирующие язвенные поражения полости рта;
- персистирующий/рецидивирующий необъяснимый паротит;
- опоясывающий герпес;
- рецидивирующие или хронические инфекции верхних дыхательных путей (средний отит, синусит, тонзиллит).
В стадии 4Б:
- снижение массы тела более чем на 10%;
- персистирующая необъяснимая диарея (более 14 дней);
- персистирующая необъяснимая лихорадка (более 30 дней);
- персистирующий кандидоз полости рта в возрасте старше двух месяцев;
- волосистоклеточная лейкоплакия языка;
- язвенно-некротический гингивит или периодонтит;
- туберкулез легких;
- тяжелые рецидивирующие бактериальные пневмонии;
- лимфоидная интерстициальная пневмония;
- анемия с уровнем гемоглобина < 80 г/л;
- нейтропения < 0,5 x 109/л;
- тромбоцитопения < 50 x 109/л.
В стадии 4В:
- синдром истощения;
- пневмоцистная пневмония;
- тяжелые рецидивирующие бактериальные инфекции, исключая пневмонию (менингит, инфекции костей и суставов, эмпиема и др.);
- инфекция, вызванная вирусом простого герпеса - персистирующие более 30 дней поражения кожи и слизистых, язвенно-некротические формы, висцеральная форма;
- ВИЧ-энцефалопатия;
- кандидоз пищевода, трахеи, бронхов;
- цитомегаловирусная инфекция, начавшаяся в возрасте старше 1 месяца - ретинит, поражение центральной нервной системы и других внутренних органов;
- токсоплазмоз мозга в возрасте старше 1 месяца;
- внелегочный криптококкоз, включая криптококковый менингит;
- диссеминированный глубокий микоз (например, внелегочный гистоплазмоз, кокцидиоидомикоз, пенициллиоз);
- хронический криптоспоридиоз (с диарейным синдромом);
- хронический изоспороз;
- диссеминированная инфекция, вызванная нетуберкулезными микобактериями;
- прогрессирующая многоочаговая лейкоэнцефалопатия;
- внелегочный туберкулез;
- криптококковый менингит;
- ВИЧ-миокардиодистрофия;
- ВИЧ-нефропатия;
- первичные лимфомы.
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза
Диагноз ВИЧ-инфекции устанавливается в соответствии с РК и на основании комплекса эпидемиологических данных, результатов клинического обследования и лабораторных исследований (в том числе на основании выявления ДНК или РНК ВИЧ), с оформлением обоснования диагноза в медицинской документации. Диагноз "ВИЧ-инфекция" устанавливается врачом Центра по профилактике и борьбе со СПИД или врачом уполномоченной специализированной медицинской организации, осуществляющей работу по проведению диагностических, лечебных, профилактических и противоэпидемических мероприятий по ВИЧ-инфекции [1, 10, 12, 19].
Основными направлениями диагностических исследований у детей являются:
- диагностика ВИЧ-инфекции;
- оценка клинико-лабораторных маркеров прогрессирования ВИЧ-инфекции;
- оценка клинико-лабораторных показателей эффективности АРТ (см. раздел 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения);
- оценка клинико-лабораторных показателей безопасности АРТ (см. раздел 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения и раздел 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики).
Диагностика ВИЧ-инфекции у детей преследует цель раннего выявления ВИЧ-инфекции, что необходимо для решения основных задач по противодействию распространению ВИЧ-инфекции: снижение заболеваемости и летальности от СПИДа [1 - 4, 20]
Эпидемиологические критерии диагноза ВИЧ-инфекции [1, 3, 10, 12, 14, 16]:
1. Факторы, свидетельствующие об очень высоком риске заражения ВИЧ:
- переливание крови или ее препаратов, пересадка органов и тканей от ВИЧ-инфицированного лица;
2. Факторы, свидетельствующие о высоком риске заражения ВИЧ:
- рождение ребенка от ВИЧ-инфицированной матери, не получавшей ППМР;
- регулярные незащищенные (без использования презерватива) половые контакты с ВИЧ-инфицированным пациентом или совместный с ним парентеральный прием психоактивных веществ;
3. Факторы, свидетельствующие об определенном риске заражения ВИЧ:
- повреждение кожных покровов или слизистых оболочек инструментом, контаминированным ВИЧ, попадание крови больного ВИЧ-инфекцией на слизистые оболочки или поврежденную кожу обследуемого;
- половые контакты с ВИЧ-инфицированным партнером: однократный незащищенный или регулярные с использованием презерватива (возможны случаи его неправильного использования);
- половые контакты, парентеральный прием наркотиков на территориях, где ВИЧ распространен среди той группы риска, к которой относится пациент;
- переливание крови, пересадка органов и тканей, парентеральные вмешательства на территориях с высоким (> 1% всего населения) уровнем распространения ВИЧ;
4. Факторы, свидетельствующие о возможности заражения ВИЧ:
- половые контакты, прием психоактивных веществ, парентеральные вмешательства на территориях с низким уровнем распространения ВИЧ.
2.1 Жалобы и анамнез
- С целью раннего выявления ВИЧ-инфекции Не рекомендуется при осмотре ребенка отвергать возможность ВИЧ-инфицирования только на основании отсутствия жалоб у пациента [21] (C4).
Комментарий: Наличие жалоб у ВИЧ-инфицированного ребенка зависит от сроков заражения. При вертикальном инфицировании на ранних сроках внутриутробного периода жалобы появляются в первые дни после рождения и отражают наличие внутриутробной ВИЧ-инфекции - гипотрофия, вялость или раздражительный крик, снижение мышечного тонуса, запрокидывание головы, лихорадка, одышка, кашель, жидкий стул, высыпания на покровных тканях, бледность кожи, цианоз и другие. При инфицировании незадолго до рождения или в родах жалобы появляются спустя 3 - 4 месяца после рождения. Инфицирование при грудном вскармливании может происходить в течение всего периода лактации, поэтому сроки появления первых жалоб и их характер становятся неопределенными. При горизонтальном инфицировании ВИЧ у подростков, так же, как и у взрослых, жалобы могут отсутствовать в течение длительного времени.
- Рекомендуется врачам МО при оказании помощи детскому населению соблюдать высокую настороженность в отношении вероятности ВИЧ-инфекции с целью наиболее раннего выявления заболевания [22, 23] (C4).
Комментарий: Учитывая распространение ВИЧ-инфекции в общей популяции населения России, феминизацию эпидемического процесса, рост доли серонегативных матерей, длительное отсутствие специфических жалоб и патогномоничных симптомов, целесообразно предполагать наличие ВИЧ-инфекции у ребенка при любом нетипичном течении заболевания и/или при выявлении эпидемиологического анамнеза (вне зависимости от социального статуса семьи ребенка). Учитывая результаты анализа позднего выявления ВИЧ-инфекции у российских детей и преследуя цель наиболее раннего выявления заболевания, эта рекомендация относится в первую очередь к специалистам МО первичного звена [3 - 5, 20, 24, 25].
- Рекомендуется с целью выявления всех возможных механизмов заражения при сборе анамнеза учитывать ВИЧ-статус матери, в том числе обследование на ВИЧ во время беременности; полноту предпринятых мер, направленных на профилактику перинатальной передачи ВИЧ от матери ребенку; наличие грудного вскармливания; гемотрансфузии, инвазивные медицинские манипуляции, случайные травмы иглой, небезопасные инъекции; половые контакты и выявление других инфекций, передаваемых половым путем [26 - 28] (C4).
- Рекомендуется при каждом осмотре ребенка в процессе диспансерного наблюдения 1 раз в 3 месяца обращать внимание на любое ухудшение самочувствия, что может быть связано как с прогрессированием ВИЧ-инфекции, так и с развитием нежелательных реакций и нежелательных явлений [29] (C5).
2.2 Физикальное обследование
- С целью возможно раннего выявления ВИЧ-инфекции Не рекомендуется отвергать возможность ВИЧ-инфицирования у детей только на основании отсутствия клинических проявлений заболевания у пациента [30] (C5).
Комментарий: Данные объективного осмотра зависят от стадии ВИЧ-инфекции у ребенка и при отсутствии АРТ могут варьировать от отсутствия клинических проявлений до тяжелых проявлений оппортунистических инфекций. Наличие жалоб у ВИЧ-инфицированного ребенка зависит от сроков заражения. При вертикальном инфицировании на ранних сроках внутриутробного периода клинические проявления могут быть выявлены в первые дни после рождения в виде симптомокомплекса задержки внутриутробного развития и вторичных инфекций. При инфицировании незадолго до рождения или в родах манифестация клиники приходится на первые месяцы жизни ребенка в виде острого ретровирусного синдрома - неспецифических симптомов в виде повышения температуры, респираторного катара, стоматита, сыпи, диспепсии; однако, отмечается не у всех детей. Инфицирование при грудном вскармливании может происходить в течение всего периода лактации, поэтому сроки появления первых симптомов ВИЧ-инфекции становятся неопределенными. При горизонтальном инфицировании ВИЧ у подростков, так же, как и у взрослых, клиника острой стадии инфекции может отсутствовать, и клинические проявления заболевания могут появиться только в стадии вторичных заболеваний [1 - 5, 20, 24, 25].
- Рекомендуется назначать обследование на ВИЧ-инфекцию при обращении детей со следующими клиническими проявлениями для раннего выявления ВИЧ-инфекции [1, 31 - 34] (B1):
- лихорадка более 1 месяца;
- увеличение лимфоузлов двух и более групп свыше 1 месяца;
- диарея, длящаяся более 1 месяца;
- необъяснимая потеря массы тела на 10 и более процентов;
- затяжные, рецидивирующие и возвратные пневмонии или пневмонии, не поддающиеся обычной терапии;
- затяжные и рецидивирующие гнойно-бактериальные или паразитарные заболевания, сепсис;
- подострый энцефалит и нейро-когнитивные расстройства у ранее здоровых лиц;
- волосистая лейкоплакия языка;
- хронические и рецидивирующие бактериальные, грибковые и вирусные заболевания кожи и слизистых, в том числе с рецидивирующая пиодермия;
- хронические воспалительные заболевания женской репродуктивной системы неясной этиологии;
- анемии и другие цитопении (лейкопения, тромбоцитопения, лимфопения) неясной этиологии;
у детей младше 13 лет:
- длительная необъяснимая гепато-(сплено)-мегалия;
- персистирующий/рецидивирующий необъяснимый паротит;
- задержка психомоторного и физического развития;
- нейтропения < 0,5 x 109/л;
- тромбоцитопения < 50 x 109/л.
Комментарий: Интерпретация клинических проявлений на ранних стадиях ВИЧ-инфекции при отсутствии выраженного нарушения иммунного статуса может вызывать трудности в связи с отсутствием типичных проявлений, характерных для продвинутых стадий болезни и проявляющихся в виде тяжелых оппортунистических инфекций и СПИД-связанных заболеваний.
Интерпретация клинических проявлений у детей, рожденных ВИЧ-инфицированными женщинами, представляет определенные трудности в связи с тем, что такие дети, даже не будучи инфицированы ВИЧ, часто рождаются недоношенными, имеют признаки внутриутробной гипотрофии, могут быть инфицированы от матерей вирусами группы герпеса (простого герпеса, цитомегалии, Эпштейна-Барр и другие), вирусами гепатитов B и C, токсоплазмой и другими возбудителями, а также имеют выраженное отставание в психомоторном и физическом развитии, часто обусловленное психосоциальной дезадаптацией.
- Настоятельно рекомендуется назначать обследование на ВИЧ-инфекцию при обращении детей со следующими установленными диагнозами для выявления ВИЧ-инфекции и начала лечения, так как данные заболевания являются СПИД-индикаторными [14]:
- саркома Капоши [35 - 38] (B2);
- лимфома мозга [39 - 41] (C4);
- Т-клеточный лейкоз [42] (C5);
- легочный и внелегочный туберкулез [43 - 45] (B2);
- заболевание, обусловленное цитомегаловирусом [46] (C4);
- генерализованная или хроническая формы инфекции, обусловленной вирусом простого герпеса [47] (C4);
- рецидивирующий опоясывающий герпес [47] (C4;
- инфекционный мононуклеоз (у лиц старше 13 лет) [47, 48, 49] (B3);
- пневмоцистоз (пневмония) [50, 51] (B2);
- токсоплазмоз с поражением центральной нервной системы [50] (C4);
- криптококкоз (внелегочный) [52] (C4);
- криптоспоридиоз [50] (C4);
- изоспороз [50, 53] (C4);
- гистоплазмоз [54] (C4);
- кандидоз пищевода, бронхов, трахеи или легких [50] (C4);
- глубокий микоз [50] (C4);
- атипичный микобактериоз [50] (C4);
- прогрессирующая многоочаговая лейкоэнцефалопатия [39, 50, 55] (C4);
- рака шейки матки (инвазивный) [36, 37, 56] (C4);
- кокцидиомикоз (диссеминированный или внелегочный) [50] (C4);
- лимфома (в том числе неходжскинская, иммунобластная, лимфома Беркитта, болезнь Ходжкина и другие) [36, 37, 41] (C4);
- сальмонеллезная (нетифоидная) септицемия возвратная [57] (C4);
- бактериальные инфекции (множественные или возвратные) у ребенка в возрасте до 13 лет [50] [58, 59] (B2);
- интерстициальная лимфоидная пневмония у ребенка в возрасте до 13 лет [60, 61] (C4);
- онкологическое заболевание у детей в возрасте до 13 лет [41] (C4).
- Рекомендуется врачам МО, ответственных за наблюдение ВИЧ-инфицированных детей, при каждом осмотре ребенка в процессе диспансерного наблюдения проводить тщательное исследование всех органов и систем с целью выявления проявлений ВИЧ-инфекции, вторичных и сопутствующих заболеваний [31, 50, 51, 62, 63] (A2).
Комментарий: следует обращать особенное внимание на оценку:
- общего состояния (температура тела, активность, физическое развитие, прибавки массы тела и роста);
- состояния кожных покровов и слизистых оболочек (выявление желтушности, проявлений грибковых инфекций, простого и опоясывающего герпеса, себорейного и другого дерматита, неопластических элементов, волосистой лейкоплакии языка и др. патологических изменений);
- состояния периферических лимфатических узлов (выявление персистирующей генерализованной лимфаденопатии);
- состояния околоушной железы (выявление персистирующего паротита);
- дыхательной системы (выявление одышки, катаральных изменений);
- сердечно-сосудистой системы (определение перкуторных размеров сердца и аускультативных изменений),
- размеров печени и селезенки;
- состояния желудочно-кишечного тракта (выявление диарейного синдрома);
- состояния эндокринной системы (выявление изменений щитовидной железы);
- неврологического и психического статуса (выявление депрессии и нейрокогнитивных нарушений: сознание, настроение, сон, зрение, невропатические проявления, когнитивные процессы - память, внимание, успеваемость и др.), у детей младшего возраста проводится оценка психомоторного развития.
2.3 Лабораторные диагностические исследования
Обследование детей ВИЧ-инфицированных матерей преследует цель выявить максимально возможное число ВИЧ-инфицированных в максимально короткие сроки. При отсутствии лечения смертность среди ВИЧ-инфицированных детей в течение первого года жизни крайне высока [64]. В этот период раннее обследование на ВИЧ-инфекцию, быстрое получение результатов и незамедлительное начало АРТ имеют жизненно важное значение.
Для лабораторной диагностики ВИЧ-инфекции используют методы обнаружения генного материала ВИЧ (РНК, ДНК) - молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1), его антигенов - определение антигена p24 вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в крови, а также методы обнаружения антител к ВИЧ - определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в крови, Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV-2) в крови. Генный материал ВИЧ может обнаруживаться уже на 7-й день после заражения, антиген p24 - на 15-й, первые антитела - на 30-й день, поздние - через 3 - 4 месяца.
Лабораторным критерием подтверждения ВИЧ-инфекции у детей является получение двух и более положительных результатов определения РНК или ДНК ВИЧ методом ПЦР [65]. При получении у ребенка лабораторного подтверждения наличия ВИЧ-инфекции в период не более 2-х недель необходимо провести обследование у специалиста по ВИЧ-инфекции для установления клинической стадии, иммунной категории, выявления вторичных заболеваний и решения вопроса о начале АРТ.
Лабораторным критерием отсутствия ВИЧ-инфекции является получение двух и более отрицательных результатов определения РНК или ДНК ВИЧ методом ПЦР, полученных в возрасте старше 14 дней при отсутствии грудного вскармливания с рождения (у детей ВИЧ-инфицированных матерей проводить обследование в декретированные сроки) [65].
При получении лабораторных критериев отсутствия ВИЧ-инфекции методами определения НК ВИЧ у ребенка серопозитивной матери необходимо продолжать дальнейшее обследование для определения антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в крови и определения антигена p24 вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в крови 1 раз в 3 месяца (начиная с 9 - 12 месячного возраста) до прекращения циркуляции материнских АТ в крови ребенка (при получении отрицательного результата исследования повторное обследование проводится через 1 месяц; при получении лабораторных критериев отсутствия ВИЧ-инфекции осуществлять снятие с диспансерного учета детей, имевших риск ВИЧ-инфекции, решением врачебной комиссии при наличии совокупности критериев снятия с учета (см. раздел Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики).
Рекомендуемые методы диагностики ВИЧ-инфекции и сроки обследования у детей различных категорий представлены в Приложении А3. Справочные материалы и Приложении Б. Алгоритмы действий врача.
- Рекомендуется врачам МО, оказывающих помощь детскому населению, с целью наиболее раннего выявления обследовать ребенка на ВИЧ-инфекцию [64, 66 - 69] (A2):
- при выявлении ВИЧ-инфекции у матери (и/или отца);
- при выявлении ВИЧ-инфекции у кормящей матери;
- при отсутствии перинатального контакта по ВИЧ-инфекции при выявлении факторов риска инфицирования или клинико-лабораторных признаков ВИЧ-инфекции;
- детей, оставшихся без попечения родителей.
- Рекомендуется у детей с перинатальным контактом по ВИЧ-инфекции в возрасте старше 18 месяцев, а также у детей без перинатального контакта в качестве стандартного метода лабораторной диагностики ВИЧ-инфекции использовать исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2 и антигена p24 (Human immunodeficiency virus HIV-1/2 + Agp24) в крови с помощью ИФА или ИХЛА с последующим применением подтверждающих тестов (иммунный, линейный блот) [70 - 73] (A2).
Комментарий: Диагностика ВИЧ-инфекции у детей, рожденных ВИЧ-серопозитивными матерями, проводится с учетом циркуляции материнских антител в крови ребенка до 18-месячного возраста, делающей методы определения антител к ВИЧ неинформативными.
- С целью выявления ВИЧ-инфекции в наиболее ранние сроки Рекомендуется у детей с перинатальным контактом по ВИЧ-инфекции в возрасте младше 18 месяцев, а также у лиц, находящихся в инкубационном периоде, использовать определение РНК или ДНК ВИЧ - молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) [1, 16, 74 - 76, 81, 88, 94 - 96] (A1).
Комментарий: Диагностика ВИЧ-инфекции у детей, рожденных ВИЧ-серопозитивными матерями, проводится с учетом циркуляции материнских антител в кровеносном русле ребенка до 18-месячного возраста, делающей методы определения антител к ВИЧ неинформативными. У детей, рожденных ВИЧ-инфицированными серонегативными матерями, выработка антител происходит, как правило, через 1 - 4 месяца от момента последнего эпизода возможного заражения (роды и грудное вскармливание). У детей с перинатальным контактом по ВИЧ-инфекции качественный метод определения ДНК ВИЧ позволяет выявить внутриклеточную ДНК в периферических мононуклеарных клетках крови у 20 - 55% детей в течение первой недели жизни, у > 90% детей в возрасте 2 - 4 недели и у 100% детей в возрасте 3 месяца и 6 месяцев. Количественный метод определения РНК ВИЧ (вирусная нагрузка) позволяет выявить внеклеточную вирусную РНК в плазме у 25 - 58% детей в течение первой недели жизни, у 89% детей в возрасте 1 месяц и у 90 - 100% детей в возрасте от 2-х до 3-х месяцев [16, 77 - 88].
При проведении диагностики ВИЧ-инфекции у ребенка в возрасте 14 - 21 день, получающего АРТ, целесообразно использовать определение ДНК ВИЧ методом ПЦР. Информативность выявления РНК ВИЧ методом ПЦР может быть нарушена у детей, получающих комбинированную профилактику перинатальной передачи тремя АРВП в связи с возможным невысоким уровнем виремии у новорожденных и ее подавлением на фоне лечения. В связи с этим у детей данной категории более целесообразно использовать молекулярные методы, направленные на качественное определение НК ВИЧ.
2.3.1. Обследование на ВИЧ-инфекцию детей ВИЧ-серопозитивных матерей в возрасте до 18 месяцев, получающих искусственное вскармливание с рождения
- Рекомендуется обследовать на ВИЧ-инфекцию всех детей, рожденных матерями, серопозитивными во время беременности и родов, с целью раннего выявления ВИЧ-инфекции [1, 16, 64, 89, 307, 308] (A2).
- Рекомендуется при наличии высокого риска заражения (и/или клинических проявлений внутриутробной инфекции/иммунодефицитного состояния) у ребенка, рожденного ВИЧ-инфицированной матерью, с целью раннего выявления ВИЧ-инфекции и перевода со схемы предполагаемого лечения на терапевтические дозы АРВП, провести исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) с помощью молекулярно-биологических методов, направленных на выявление ДНК ВИЧ, не прерывая курс предполагаемой терапии, в следующие декретированные сроки [1, 16, 84, 90 - 94, 307, 309] (C1):
- в первые 48 часов жизни (нельзя исследовать кровь из пуповины); при получении положительного результата провести повторное исследование в кратчайшие сроки;
- при получении отрицательного результата повторить исследование в возрасте 21 - 28 дней; при получении положительного результата провести повторное исследование в кратчайшие сроки;
Комментарий: Если выявлены факторы повышенного риска передачи ВИЧ от матери во время беременности:
- мать не принимала АРТ во время беременности;
- мать получала АРТ во время беременности, но не достигнута вирусная супрессия (РНК ВИЧ > 50 копий/мл) к 36 неделям беременности и/или в течение 4 недель до родов, или обследование на ВИЧ у матери не проведено или проведено не полностью;
- наличие у матери острой ВИЧ-инфекции во время беременности;
- выявлен положительный экспресс-тест у матери во время родов
обследование ребенка в первые 2 дня после рождения позволяет осуществить раннее выявление ВИЧ-инфекции и раннее начало АРТ.
Молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1), проведенное в первые дни после рождения, позволяет выявить детей, инфицированных ВИЧ in utero и не выявляет детей, инфицированных в течение недели перед родами и в родах. Если ребенок заразился ВИЧ-инфекцией менее, чем за 10 дней до обследования, результат обследования на НК ВИЧ может быть ложноотрицательным, поэтому отрицательные результаты обследований, проведенных в первые 7 - 10 дней жизни, в дальнейшем не учитываются [1, 16, 77, 81, 84, 307].
Диагностическая чувствительность молекулярно-биологических методов существенно возрастает к 2-недельному возрасту, а раннее выявление инфекции позволяет перейти от предполагаемой терапии ВИЧ к лечебным дозам АРТ.
- Настоятельно рекомендуется у всех детей, рожденных ВИЧ-инфицированными матерями, провести после окончания курса АРТ (профилактического у детей с низким риском заражения или предполагаемой терапии у детей с высоким риском заражения) молекулярно-биологические исследования крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в декретированные сроки с использованием методов, направленных на выявление ДНК или РНК ВИЧ [1, 16, 74, 81, 88, 94 - 96, 307] (B2):
- через 2 недели после окончания профилактического курса АРТ, т.е. в возрасте 6 недель у детей с низким риском заражения и в возрасте 8 недель у детей с высоким риском заражения; при получении положительного результата обследования провести второе (подтверждающее) обследование в кратчайшие сроки;
- при получении отрицательного результата обследования провести второе (подтверждающее) обследование в возрасте 4 - 6 месяцев; при получении положительного результата этого обследования провести второе (подтверждающее) обследование в кратчайшие сроки.
|
Критерии риска ВИЧ-инфицирования ребенка
|
Диагностика ВИЧ-инфекции у детей с помощью молекулярных методов (ПЦР ДНК и ПЦР РНК)
|
|
Высокий риск:
- мать получала АРТ во время беременности, но не достигнута вирусная супрессия (РНК ВИЧ менее 50 копий/мл) к 36 неделям беременности и/или в течение 4 недель до родов, или данное обследование у матери не проведено или проведено не полностью;
- мать не принимала АРТ во время беременности;
- наличие у матери острой ВИЧ-инфекции во время беременности;
- выявлен положительный экспресс-тест у матери во время родов
|
- При рождении (ДНК)
- В возрасте 14 - 21 день на фоне курса предполагаемой терапии (ДНК)
- Через 2 недели после окончания курса АРТ (в 8 недель) (ДНК или РНК)
- В 4 - 6 месяцев (ДНК или РНК)
|
|
Низкий риск:
- мать получала АРТ во время беременности; и
- в течение беременности сохранялась вирусная супрессия (РНК ВИЧ менее 50 копий/мл); и
- у матери была высокая приверженность АРТ
|
- Через 2 недели после окончания курса АРТ (в 6 недель) (ДНК или РНК)
- В 4 - 6 месяцев (ДНК или РНК)
|
2.3.2. Обследование на ВИЧ-инфекцию детей ВИЧ-серопозитивных матерей в возрасте 18 месяцев и старше, не обследованных с помощью методов выявления нуклеиновых кислот ВИЧ и получающих искусственное вскармливание с рождения
- Рекомендуется решать вопрос о наличии/отсутствии лабораторных критериев ВИЧ-инфекции по результатам исследований на АТ/АГ ВИЧ с помощью стандартных методов лабораторной диагностики ВИЧ-инфекции [1, 16, 96, 307, 325, 326] (B3).
2.3.3. Обследование на ВИЧ-инфекцию детей, рожденных ВИЧ-серопозитивными матерями и получающих грудное вскармливание
- Рекомендуется у детей ВИЧ-серопозитивных матерей, если мать приняла решение проводить грудное вскармливание, проводить обследования на ВИЧ-инфекцию в соответствии с алгоритмом диагностики у детей с высоким риском ВИЧ-инфекции:
- при рождении, в 14 - 21 день и в 4 - 6 недель [84, 90 - 94, 307, 308, 309] (C4);
- через 2 недели после прекращения курса АРТ и в возрасте и 4 - 6 месяцев [1, 16, 81, 88, 94 - 96, 307] (C2);
- затем в течение всего периода грудного вскармливания (1 раз в 3 месяца) и после полного прекращения грудного вскармливания (через 4 - 6 недель, через 3 месяца, через 6 месяцев) [1, 93, 307, 308, 309] (C3).
Комментарий: Риск передачи ВИЧ-инфекции от матери ребенку при грудном вскармливании составляет 16 - 30% и более в дополнение к риску передачи во время беременности и родов, поэтому ВИЧ-инфицированным женщинам настоятельно не рекомендуется прикладывать детей к груди и кормить сцеженным грудным молоком. Несмотря на это, некоторые матери принимают осознанное решение кормить ребенка грудью (чаще по религиозным, семейным причинам и в результате СПИД-отрицания). В последние годы увеличилась доля женщин, серонегативных во время беременности и родов, у которых ВИЧ-инфекция выявляется во время проведения грудного вскармливания или уже после его прекращения. Возможность инфицирования посредством грудного вскармливания сохраняется вплоть до последнего прикладывания к груди [68].
2.3.4. Объем обследований при взятии на диспансерный учет ребенка с ВИЧ-инфекцией
Задачи диагностического обследования при взятии ребенка под наблюдение (диспансерный учет):
- установление клинического диагноза ВИЧ-инфекции;
- определение степени поражения иммунной системы, позволяющее прогнозировать течение заболевания и определять лечебную тактику;
- выявление показаний к быстрому началу АРТ;
- выявление показаний к первичной профилактике вторичных заболеваний;
- выявление вторичных заболеваний и показаний к их лечению;
- выявление сопутствующей патологии и показаний к ее лечению.
- Рекомендуется при постановке ребенка, инфицированного ВИЧ, на диспансерный учет провести исследования:
- исследование CD4+ лимфоцитов с определением процентного содержания и абсолютного количества CD4-лимфоцитов и оценкой степени поражения иммунной системы в соответствии с иммунными категориями в зависимости от возраста ребенка, для выявления показаний к быстрому началу АРТ (см. таблицу 1) [97 - 99] (B2).
Комментарий: У детей с ВИЧ-инфекцией, не получающих АРТ, по мере прогрессирования заболевания происходит истощение иммунной системы, проявляющееся снижением процентного содержания и абсолютного количества CD4-лимфоцитов, что приводит к развитию вторичных заболеваний, включая оппортунистические инфекции. В настоящее время показано, что абсолютное количество CD4-лимфоцитов является более надежным прогностическим фактором прогрессирования ВИЧ-инфекции, чем их процентное содержание, т.к. развитие вторичных заболеваний и оппортунистических инфекций зависит от количества циркулирующих клеток, которое может быть низким при наличии высокого процентного содержания на фоне лейко- и лимфопении. При этом у детей до 5 лет определение процентного содержания CD4-лимфоцитов по-прежнему является достоверным альтернативным показателем состояния иммунной системы.
Показатели CD4-лимфоцитов не имеют значения для начала АРТ, т.к. она показана всем детям независимо от иммунного статуса и других клинико-лабораторных показателей. Однако, решение о быстром начале АРТ, а также о начале и проведении профилактики и лечения вторичных инфекций принимается на основании возрастных показателей процентного содержания и абсолютного количества CD4-лимфоцитов [16, 17, 77, 100, 101].
- исследование CD8+ лимфоцитов с определением процентного содержания и абсолютного количества CD8-лимфоцитов и вычислением иммунорегуляторного индекса - соотношения абсолютных показателей CD4/CD8 для определения прогноза [102, 103] (C4).
Комментарий: в результате ВИЧ-инфекции абсолютное количество CD4-лимфоцитов постепенно снижается, что приводит к инверсии соотношения CD4/CD8 (в норме показатель соотношения CD4-лимфоцитов и CD8-лимфоцитов выше 1,0). Как правило, даже у пациентов в бессимптомной стадии ВИЧ-инфекции, а также при отсутствии иммунодефицитного состояния этот показатель снижается и составляет менее 1,0. По мере прогрессирования ВИЧ-инфекции и истощения популяции CD4-лимфоцитов ИРИ снижается существенно менее 1,0. ИРИ имеет важное прогностическое значение, т.к. является достоверным предиктором прогрессирования ВИЧ-инфекции и летального исхода независимо от количественных показателей CD4- и CD8-лимфоцитов. Кроме того, снижение ИРИ на фоне проводимой АРТ является предиктором повышения вирусной нагрузки и вирусологической неудачи [104 - 112].
- количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР ("вирусная нагрузка") с целью определения прогноза заболевания [113] (B2);
- общий (клинический) анализ крови развернутый для оценки общего состояния пациента и выбора АРВП [114, 115] (B3);
- анализ крови по оценке нарушений липидного обмена биохимический для оценки общего состояния пациента, оценки нутритивного статуса пациента и выбора АРВП (C5), [116], для оценки липидного профиля - (A3) [116];
- выявление аллели 5701 локуса B главного комплекса гистосовместимости человека (HLA B*5701) с целью определения чувствительности к абакавиру** при назначении АРТ [117 - 121] (A1);
- общий (клинический) анализ мочи с целью оценки общего состояния пациента [122, 123] (A4);
- скрининговое обследование на вирусный гепатит C (см. соответствующие клинические рекомендации): определение антител к вирусу гепатита C (Hepatitis C virus) в крови; скрининговое обследование на вирусный гепатит B (см. соответствующие клинические рекомендации): определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови [124] (C4);
- определение антител класса G (IgG) и класса M (IgM) к токсоплазме (Toxoplasma gondii) в крови с целью раннего выявления заболевания [125] (C4);
- определение антител классов M, G (IgM, IgG) к цитомегаловирусу (Cytomegalovirus) в крови с целью раннего выявления заболевания [126] (C4);
- скрининговое обследование на туберкулез (см. соответствующие клинические рекомендации) [127, 128] (A2).
- Рекомендуется при тяжелой иммуносупрессии в соответствии с возрастной нормой провести исследования:
- определение антигена криптококка (Cryptococcus neoformans) в крови с целью диагностики криптококкоза и определения показаний к началу лечения заболевания [129] (C4);
- определение кислотоустойчивых бактерий в кале, моче и мокроте - с целью диагностики микобактериоза и определения показаний к началу лечения: микроскопическое исследование мокроты на микобактерии (Mycobacterium spp.), микробиологическое (культуральное) исследование мокроты на микобактерии туберкулеза (Mycobacterium tuberculosis complex), определение ДНК Mycobacterium tuberculosis complex (микобактерий туберкулеза) в мокроте, микробиологическое (культуральное) исследование кала на микобактерии (Mycobacterium spp.) [130] (B2); или промывных водах бронхов методом ПЦР, (см. соответствующие клинические рекомендации).
Комментарий: диагностика микобактериозов проводится с использованием лабораторных мощностей противотуберкулезной службы.
- Рекомендуется после получения результатов лабораторных, инструментальных исследований и консультаций врачей-специалистов провести повторный прием врача-инфекциониста с целью окончательного заключения о стадии и фазе заболевания, определения плана дальнейшего наблюдения за пациентом и его лечения [1, 10, 19] (C5).
Комментарий: С пациентом проводится беседа о необходимости раннего начала АРТ, регулярного прохождения плановых обследований в структуре диспансерного наблюдения.
2.3.5 Оценка динамики состояния ребенка с ВИЧ-инфекцией, состоящего на диспансерном учете (в процессе наблюдения и проведения АРТ)
- Рекомендуется всем пациентам, состоящим на диспансерном учете, проводить плановые диагностические исследования с целью оценки и мониторинга состояния пациента:
1) прогрессирования ВИЧ-инфекции и/или эффективности АРТ [131 - 136] (B2):
- исследование CD4+ лимфоцитов [136] (A2);
- исследование ИРИ по соотношению CD4 и CD8-лимфоцитов [136] (A2);
- количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР [135] (B2);
- молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) - при наличии признаков неэффективности АРТ (см. раздел "Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения");
2) прогрессирования ВИЧ-инфекции и выявления побочных эффектов лечения: общий (клинический) анализ крови, развернутый; биохимический анализ крови; анализ крови по оценке нарушений липидного обмена биохимический [136] (A2); анализ мочи общий [137] (C4);
3) проявлений вторичных и сопутствующих заболеваний: диагностика туберкулеза (см. соответствующие клинические рекомендации) при отсутствии активного туберкулеза [38, 131, 138] (B2); скрининговое обследование на вирусный гепатит B при отсутствии диагноза вирусного гепатита B [131, 138] (B2); скрининговое обследование на вирусный гепатит C при отсутствии диагноза вирусного гепатита C [124] (C4); определение антител к бледной трепонеме (Treponema pallidum) в крови - по показаниям (см. соответствующие клинические рекомендации) [131] (C5).
4) гепатотоксичности лекарственных препаратов и/или активности гепатита [139, 140 - 142] (B3):
- определение активности аспартатаминотрансферазы и аланинаминотрансферазы в крови;
- исследование уровня общего билирубина в крови;
- определение активности щелочной фосфатазы в крови - при выявлении цитолитического синдрома;
- определение активности гамма-глутамилтранспептидазы в крови - при выявлении цитолитического синдрома;
5) нефротоксичности препаратов и/или активности имеющейся патологии почек [139, 141, 142] (B3); уровня креатинина в крови [401, 402, 403] (B3);
6) состояния костной ткани и побочных эффектов лечения [143] (C4):
- исследование уровня общего кальция в крови;
- исследование уровня неорганического фосфора в крови и уровня фосфора в моче;
7) исследование уровня альфа-фетопротеина в сыворотке крови - каждые 6 месяцев у детей с циррозом печени, см. соответствующие клинические рекомендации) [144] (C5);
8) цитологическое исследование микропрепарата цервикального канала - у молодых женщин, ведущих половую жизнь, для своевременной диагностики предраковых заболеваний шейки матки (см. соответствующие клинические рекомендации) [145] (C5).
Комментарий: В случае выявления маркеров хронических вирусных гепатитов B или C требуется проведение диагностических мероприятий, направленных на установление клинического диагноза или его исключения, в соответствии с клиническими рекомендациями по данным заболеваниям.
В том случае, если хронический вирусный гепатит B или C был выявлен у пациента и лечение его не проведено - нецелесообразно ежегодно повторять скрининговое исследование маркеров хронических вирусных гепатитов.
График и объем исследований в процессе наблюдения и проведения АРТ представлены в Приложении А3.
При уровне CD4-лимфоцитов, соответствующем 1-ой иммунной категории и ВН ниже уровня определения (менее 50 копий/мл) в течение последних 24 месяцев АРТ исследования с кратностью 1 раз в 3 месяца можно проводить 1 раз в 6 месяцев (при отсутствии патологии). При выявлении повышенных показателей одного или нескольких биохимических маркеров частота их контроля может быть увеличена (в соответствии с клинической ситуацией).
- Рекомендуется у детей, не получающих АРТ, каждые 3 - 4 месяца проводить мониторинг клинических, вирусологических и иммунологических показателей [24, 146] (C4).
Комментарий: в настоящее время рекомендуется начинать АРТ всем пациентам после выявления ВИЧ-инфекции независимо от клинико-лабораторных показателей. В дополнение к доказанной эффективности АРТ у пациентов с клиническими проявлениями ВИЧ-инфекции и нарушенным иммунитетом, было достоверно доказано снижение риска прогрессирования заболевания и летальности у асимптомных пациентов, начинающих АРТ на фоне высоких показателей CD4.
Показаниями для быстрого начала АРТ являются возраст младше 1 года; клинические проявления ВИЧ-инфекции, соответствующие стадиям 2В, 4Б и 4В независимо от возраста; содержание CD4-лимфоцитов <= 500 клеток/мм3 у детей 1 г - 5 лет и <= 200 клеток/мм3 у детей старше 5 лет. (см. раздел 3.1, табл. 2).
2.4 Инструментальные диагностические исследования
Диагностика ВИЧ-инфекции не подразумевает специального инструментального обследования.
Инструментальное обследование используется для диагностики вторичных заболеваний, выявление которых может повлиять на исход заболевания и тактику лечения пациента, а также факторов риска и сопутствующих заболеваний, влияющих на сроки назначения и выбор схемы АРТ.
2.4.1. Инструментальные диагностические исследования при проведении диспансерного наблюдения ВИЧ-инфицированного ребенка
- Рекомендуется провести следующие инструментальные диагностические исследования всем пациентам при постановке на диспансерный учет с целью оценки общего состояния пациента, наличия сопутствующих заболеваний, выявления нежелательных явлений вследствие АРТ:
- рентгенография легких [45, 147 - 149] (B2);
- регистрация электрокардиограммы (в соответствии с возрастными особенностями) [150] (C4);
- ультразвуковое исследование органов брюшной полости (комплексное) [151] (C4);
- ультразвуковое исследование почек и надпочечников [152, 153] (C4).
- Рекомендуется всем пациентам, находящимся на диспансерном учете, проводить плановые обследования с целью мониторинга состояния ребенка:
- флюорография или рентгенография легких детям 15 лет и старше: 1 раз в 6 месяцев при отсутствии активного туберкулеза [45, 147 - 149] (B2);
- регистрация электрокардиограммы (в соответствии с возрастными особенностями) [150] (A3);
- ультразвуковое исследование органов брюшной полости (комплексное) [151] (C4); 1 раз в 12 месяцев, у детей с циррозом печени - 1 раз в 6 месяцев;
- ультразвуковое исследование почек и надпочечников [152, 153] (C4);
- иные инструментальные исследования при наличии показаний.
2.5 Иные диагностические исследования
- Рекомендуется при получении клинико-лабораторных данных, подтверждающих неэффективность проводимой терапии, с целью подбора эффективных АРВП провести молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) [154] (B3).
Комментарий: Исследование резистентности проводится на фоне АРТ, в крайнем случае течение 2х недель после прекращения приема всех препаратов схемы (следует учитывать длительный период полувыведения ННИОТ). При ВН от 500 до 1.000 копий/мл плазмы мутации могут остаться не выявленными с помощью обычных методов (не высокочувствительных).
2.5.1. Консультации врачей-специалистов
В процессе диспансерного наблюдения ВИЧ-инфицированных детей до начала и во время проведения АРТ следует соблюдать график периодичности плановых приемов врачей-специалистов в соответствии с Перечнем исследований при проведении профилактических медицинских осмотров несовершеннолетних [1], а также проводить осмотры врачей-специалистов при наличии показаний.
Структурные и функциональные нарушения со стороны сердечно-сосудистой системы выявляются у ВИЧ-инфицированных детей с частотой 62 - 76%, при этом часто остаются не выявленными при отсутствии настороженности у врачей, наблюдающих ВИЧ-инфицированного ребенка [392 - 394]. Раннее начало АРТ и ее непрерывное проведение способствуют улучшению состояния сердечно-сосудистой системы [392, 395, 397 - 400], однако, частота ее поражения может возрастать при позднем начале АРТ, низкой приверженности лечению, наличии сопутствующей патологии, а также вследствие побочного действия антиретровирусных препаратов [394 - 399]. Результаты исследований и наблюдений показывают, что независимо от наличия АРТ ВИЧ-инфицированные дети должны проходить регулярные обследования у врача-кардиолога детского [392, 394, 395, 397, 399].
2.5.2. Поражение центральной нервной системы, обусловленное вирусом иммунодефицита человека
- Рекомендуется при постановке на диспансерный учет провести у ребенка когнитивную психодиагностику, направленную на выявление познавательных (когнитивных) нарушений [155, 156, 317, 377, 378, 388] (A2).
Комментарий: Обследование проводится врачом, ответственным за наблюдение ВИЧ-инфицированного ребенка, или медицинским психологом МО, ответственной за наблюдение ВИЧ-инфицированного ребенка. В возрасте младше 6 лет используется методика Стребелевой; в возрасте от 6 до 17 лет - тест Векслера, версия не ниже 3.0.
- Рекомендуется у детей 0 - 17 лет, состоящих на диспансерном учете, проводить углубленное неврологическое обследование с целью выявления неврологических нарушений не реже 1 раза в 6 месяцев. [155, 156, 281, 317, 377 - 385, 387 - 390] (A2);
- Рекомендуется у детей 6 - 17 лет, состоящих на диспансерном учете, проводить клинико-психологическое нейропсихологическое обследование медицинским психологом с целью выявления когнитивных нарушений не реже 1 раза в 6 месяцев. [281, 314, 315, 317, 378, 380, 381 - 391] (A2);
Комментарий: У детей, инфицированных ВИЧ перинатально и получающих АРТ, наиболее частыми проявлениями ВИЧ-инфекции в настоящее время являются неврологические и когнитивные нарушения, которые имеют многофакторные причины, включая: формирования резервуаров ВИЧ в ЦНС уже в первые дни после заражения, необратимое поражение ЦНС до начала АРТ, продолжающуюся низкоуровневую репликацию ВИЧ в ЦНС и нейровоспаление на фоне эффективной АРТ [316, 317, 318]. Общая частота выявления неврологических нарушений и нейрокогнитивных расстройств у детей достигает 90%, наиболее часто регистрируются ВИЧ-энцефалопатия, ВИЧ-энцефалит, двигательные нарушения. 50% пациентов, получающих АРТ, имеют выраженный когнитивный дефицит [6].
- Рекомендуется при постановке ребенка на диспансерный учет провести МРТ головного мозга или функциональную МРТ головного мозга с целью выявления очагов поражения, а также на визуализацию других признаков патологии развития и функций [156 - 158, 379, 381, 386, 389] (B3).
- Рекомендуется врачу, ответственному за наблюдение ВИЧ-инфицированного ребенка, проводить у ребенка нейровизуализацию с помощью МРТ или функциональной МРТ не реже 1 раза в 12 месяцев при наличии неврологических нарушений и/или нейрокогнитивных расстройств с целью выявления патологических изменений вещества мозга [156, 158 - 161, 379, 381, 386, 389, 391] (B3).
Комментарий: Учитывая нейротропность вируса иммунодефицита человека и высокую частоту поражения ЦНС и нарушений психической сферы у ВИЧ-инфицированных пациентов (даже при отсутствии клинических проявлений поражения головного мозга), а также в связи с возможными трудностями в дифференциальной диагностике данных патологических процессов, следует всем детям в качестве мероприятия, направленного на выявление патологии ЦНС и психической сферы, проводить комплексное клинико-психологическое нейропсихологическое обследование независимо от наличия клинических проявлений, иммунного статуса и вирусной нагрузки. Показано, что патологические изменения коры мозга происходят до появления нарушений, выявляемых с помощью нейропсихологических тестов и значительно ранее клинической симптоматики. Нейровизуализация головного мозга с помощью МРТ имеет важное значение для ранней клинической диагностики, ведения пациентов и выбора тактики дальнейшей терапии [66, 156 - 161, 281, 316, 381, 386, 390].
- Рекомендуется при выявлении у ребенка когнитивного дефицита или ментальных расстройств проводить психокогнитивную реабилитацию [281, 379, 383, 384, 387, 388, 391] (C4).
2.5.3. Клинико-психологическое нейропсихологическое и социальное обследование ребенка с ВИЧ-инфекцией, направленное на повышение приверженности наблюдению и лечению
Данный вид обследования проводится медицинским психологом МО, ответственным за наблюдение ВИЧ-инфицированного ребенка, а при его отсутствии - врачом, ответственным за наблюдение ВИЧ-инфицированного ребенка.
- Рекомендуется начиная с раннего возраста ребенка проводить регулярную работу, направленную на расширение знаний ребенка о заболевании (ВИЧ-инфекции), и подготовку к дальнейшему раскрытию ВИЧ-статуса в возрасте 10 - 14 лет [162, 163] (B4).
Комментарий: Раскрытие ВИЧ-статуса особенно важно в подростковом возрасте, что позволяет избежать горизонтальной и вертикальной передачи ВИЧ-инфекции и достоверно влияет на приверженность наблюдению и АРТ, эффективность АРТ, качество жизни, социальную сферу и др. аспекты жизни ребенка с ВИЧ-инфекцией.
- Рекомендуется проводить 1 раз в 6 месяцев оценку медикаментозной приверженности (независимо от того, получает ребенок АРТ или нет) для оценки соблюдения режима приема АРВП [164, 165] (B4).
Комментарий: Достоверно установлено, что для достижения и длительного поддержания вирусологической супрессии необходима приверженность АРТ 95% и выше. Последствиями сниженной и, в особенности, низкой приверженности АРТ являются формирование резистентности к АРВП; повышение частоты госпитализаций; снижение эффективности лечения и повышение вероятности прогрессирования ВИЧ-инфекции и наступления летального исхода; необходимость назначения второй и последующих линий АРТ, стоимость которых, как правило, существенно превышает стоимость схемы стартовой терапии; продолжающееся распространение ВИЧ в популяции.
- Рекомендуется для количественной оценки медикаментозной приверженности использовать:
- 8-вопросный тест Мориски-Грин: [168, 169] (B3):
- адаптированный для подростков в возрасте 11 - 17 лет;
- адаптированный для законных представителей детей в возрасте младше 11 лет. [168, 169] (B3).
- подсчет таблеток по формуле:
где x - комплаентность в %-ном выражении; a - количество предписанных пациенту таблеток (доз); b - количество оставшихся у пациента таблеток (доз)
- Для диагностики уровня медикаментозной приверженности применять не менее двух методов: исследование вирусной нагрузки плюс анкетирование или подсчет таблеток.
- Рекомендуется при выявлении приверженности АРТ < 95% у ребенка провести тест с целью выявления и выраженности тревожной и депрессивной симптоматики [174 - 184] (B3).
Комментарий: Психические нарушения выявляются у ВИЧ-инфицированных детей достоверно чаще, чем в популяции, и являются предикторами прогрессирования ВИЧ-инфекции, нарушения приверженности АРТ, снижения качества жизни. Частота встречаемости психических расстройств у ВИЧ-инфицированных детей составляет от 20 до 61%, более одного психического расстройства имеют 25% детей. Высокая тревожность регистрируется с частотой до 46%, депрессия - 20 - 41%, психосоматизация - 18%, суицидальные идеи - 16%, социофобия - 13%, оппозиционное расстройство и синдром дефицита внимания и гиперактивности - 12%, судорожные припадки - 8%. Важным фактором риска снижения продолжительности АРТ и соблюдения режима лечения является депрессия. Кумулятивная вероятность длительного продолжения линии АРТ достоверно выше у пациентов с менее выраженной депрессивной симптоматикой: пациенты значительно лучше соблюдают схему лечения [175 - 178].
- Рекомендуется для выявления тревожных и депрессивных расстройств провести тестирование с помощью госпитальной шкалы оценки тревоги и депрессии (HADS) у детей в возрасте 11 лет и старше, или у законных представителей детей в возрасте младше 11 лет [174, 179 - 184] (B3).
- Рекомендуется при выявлении субклинического или клинического уровня депрессии и/или тревоги (по госпитальной шкале оценки тревоги и депрессии HADS) у ВИЧ-инфицированного ребенка направить на консультацию к врачу-психотерапевту или врачу-психиатру детскому самого ребенка, если он в возрасте 11 лет и старше, или законных представителей детей в возрасте младше 11 лет с целью уточнения диагноза и тактики дальнейшего ведения [184 - 187] (B3).
Тестирование детей в возрасте младше 15 лет проводится только в присутствии их законных представителей.
При невозможности проведения комплекса нейропсихологического и социального обследования и сопровождения, включая вопросы приверженности лечению, в процессе осуществлении диспансерного наблюдения ребенка с ВИЧ-инфекцией по месту жительства необходимо направлять такого ребенка в профильную специализированную МО областного, краевого, окружного, федерального значения, имеющую в своем штате специалистов врачей-неврологов, врачей-психиатров детских/врачей-психотерапевтов, медицинских психологов с опытом работы с ВИЧ-инфицированными детьми, а также возможность проведения нейровизуализации.
Информация о приверженности АРТ и методах ее повышения и поддержания представлена в разделе 7. Дополнительная информация; алгоритм социо-психологической помощи, включая оценку и коррекцию приверженности, НКР и депрессии, представлен в Приложении Б. Алгоритмы действий врача; характеристика методов исследования приверженности, качества жизни и тревоги/депрессии представлены в Приложениях Г1 - Г4. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях; классификация нейрокогнитивных нарушений представлена в разделе 7. Дополнительная информация.
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Главная задача лечения ВИЧ-инфекции у детей на современном этапе - сохранение здоровья для полной и продуктивной жизнедеятельности во взрослой жизни. АРТ является единственным специфическим методом лечения ВИЧ-инфекции, способным сохранить жизнь ВИЧ-инфицированного ребенка и обеспечить ее высокое качество. Выделяют две цели АРТ у детей: снижение СПИД-связанной летальности и снижение заболеваемости <1>.
--------------------------------
<1> Приказ Министерства здравоохранения Российской Федерации от 10.08.2017 N 514н "О порядке проведения профилактических медицинских осмотров несовершеннолетних" (в ред. Приказов Минздрава РФ от 03.07.2018 N 410н, от 13.06.2019 N 396н, от 19.11.2020 N 1235н)
Основной механизм достижения этих целей - максимальное и надежное подавление репликации ВИЧ в организме путем назначения АРТ.
Общая информация об АРТ представлена в Приложении 7. Дополнительная информация.
Принципами АРТ являются:
- добровольность - осознанное принятие решения о начале лечения и его проведении, документированное "информированным согласием"; в случае отказа законного представителя ребенка от терапии необходимо принимать законные меры для начала (возобновления) терапии ребенком;
- своевременность - как можно более раннее начало АРТ;
- непрерывность - длительное (пожизненное) соблюдение режима приема АРВП.
Важнейшим условием проведения АРТ у ребенка является готовность и способность его самого или лиц, осуществляющих уход за ним, выполнить все назначения врача. Подготовка к АРТ заключается в оценке состояния ребенка и консультировании ребенка (соответственно возрасту) и/или ухаживающих за ним лиц. По результатам консультирования врач делает выводы о социально-психологическом статусе ребенка или лиц, ухаживающих за ребенком, и об их способности соблюдать правила хранения, дозирования препаратов и выполнять режимные моменты [188 - 191].
Таким образом, необходимо перед началом АРТ обсудить с пациентом или его законным представителем следующие основные вопросы:
- важность строгого соблюдения режима АРТ (временной, пищевой, водный режим и другие режимные моменты);
- возможные побочные действия АРВП, в случае которых необходимо обратиться к врачу;
- признаки частых заболеваний у ВИЧ-инфицированных детей, требующие срочной диагностики и лечения;
- профилактика вторичных инфекций, в том числе пневмоцистной пневмонии;
- важность проведения профилактических прививок;
- вскармливание и питание ВИЧ-инфицированного ребенка: оптимальный рацион, рекомендации по применению пищевых добавок, особенности питания при наличии нарушений аппетита или способности принимать пищу. Для детей первого года жизни необходима консультация родителя/опекуна по искусственному вскармливанию;
- возможность развития синдрома восстановления иммунитета, сопровождающегося временным ухудшением клинического состояния, разъяснение, что это является показателем эффективности проводимой терапии и не является основанием для ее отмены или прерывания.
- Рекомендуется перед началом АРТ провести консультирование, т.е. обсудить с ребенком (в соответствии с его возрастом и степенью понимания им диагноза) и/или лицами, осуществляющими уход за ним, вопросы, связанные с течением ВИЧ-инфекции, проведением АРТ с целью обсуждения необходимости строгого соблюдения рекомендаций по наблюдению и лечению, а также с целью выявления возможных барьеров приверженности [192 - 194] (A2).
Комментарий: Консультирование детей необходимо проводить с начала АРТ и продолжать в процессе лечения, меняя его форму и содержание в соответствии с возрастными особенностями ребенка [188 - 191].
После проведения консультирования лицо, несущее юридическую ответственность за ребенка в возрасте до 15 лет, подписывает информированное согласие на проведение АРТ или отказ от ее проведения (см. Приложение А3. Справочные материалы). По достижении 15 лет подросток имеет право на сохранение врачебной тайны и подписывает информированное согласие самостоятельно. При отказе родителей или иного законного представителя лица, не достигшего возраста 15 лет, либо законного представителя лица, признанного в установленном законом порядке недееспособным, от медицинского вмешательства, необходимого для спасения его жизни, медицинская организация имеет право обратиться в суд для защиты интересов такого лица [2].
Особенности применения АРВП у детей:
- перед назначением абакавира** необходимо провести исследование для выявления аллели 5701 локуса B главного комплекса гистосовместимости человека (HLA B*5701);
- рилпивирин не следует назначать при ВН > 100 000 копий/мл плазмы;
- у детей старше 12 лет при ВН > 100 000 копий/мл плазмы более предпочтительно использовать тенофовир** вместо абакавира**;
- зидовудин** не следует назначать при наличии анемии, тромбоцитопении, лимфопении, а если эти отклонения развились на фоне его применения, следует заменить его на абакавир** или - в возрасте старше 12 лет - на тенофовир**;
- эфавиренз** целесообразно использовать у детей, получающих для лечения вторичных инфекций рифампицин** (рифампицин** применяется у детей с 3 лет) или противогрибковые препараты производные триазола;
- невирапин** не используется у детей первого года жизни, если он применялся у матери и/или ребенка для профилактики передачи ВИЧ. Не следует назначать невирапин** девочкам пост-пубертатного возраста с CD4 > 250 клеток/мм3;
- у детей используются ИП, усиленные ритонавиром** (бустирование - добавление низкой дозы ритонавира** для улучшения фармакодинамики ИП);
- применение комбинированных АРВП позволяет снизить бремя пожизненной терапии и повысить приверженность лечению. Использование комбинированных форм определяется особенностями входящих в их состав монопрепаратов и возможно при достижении возраста и массы тела ребенка, указанных в инструкции к комбинированному препарату (см. Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата).
Решая вопрос о выборе АРВП у ребенка, следует учитывать их преимущества и недостатки и соотносить их с особенностями течения ВИЧ-инфекции, наличием вторичных и сопутствующих заболеваний, требующих лечения, характером лабораторных показателей, особенностями ухода за ребенком и др. факторами, которые, по мнению лечащего врача, могут повлиять на переносимость, эффективность и безопасность АРТ (см. таблицу 10. Преимущества и недостатки различных АРВП в разделе 7. Дополнительная информация). Каждому ребенку следует подобрать для стартовой терапии наиболее приемлемую схему из числа препаратов предпочтительного ряда, а при наличии показаний - альтернативного.
Правила расчета доз представлены в разделе 7. Дополнительная информация и Приложении A3. Справочные материалы (таблица 20. Рекомендуемые дозы АРВП у детей и особенности их применения).
Выработка режима приема АРВП представлена в разделе 7. Дополнительная информация.
3.1 Показания к началу АРТ
- Рекомендуется начать АРТ всем детям с подтвержденной ВИЧ-инфекцией, независимо от возраста, клинических проявлений и показателей CD4 с целью максимально раннего подавления размножения ВИЧ, предотвращения образования резервуаров вируса, увеличения продолжительности и улучшения качества жизни [195] (A2).
- Рекомендуется быстрое начало АРТ (в течение 2х недель от момента постановки на диспансерный учет) детям с подтвержденной ВИЧ-инфекцией в возрасте младше 1 года с целью предотвращения быстрого прогрессирования заболевания и ранней смертности (см. табл. 2) [196 - 198] (A1).
Комментарий: Современные диагностические подходы позволяют выявить ВИЧ-инфекцию у детей, заразившихся во время беременности и родов, уже в первые дни и недели жизни: у 55 - 76% - при рождении и у всех детей в возрасте от 6 недель до 3х месяцев (74, 311).
В многочисленных клинических исследованиях и наблюдениях было показано, что раннее начало АРТ (в первые дни и недели жизни) драматическим образом влияет на течение ВИЧ-инфекции у детей: значительно снижается размер вирусных резервуаров (322); улучшается вирусологический контроль (328); улучшаются функции иммунной системы и в первую очередь CD4- и CD-8 лимфоцитов (329, 330); происходит улучшение метаболического профиля, что приводит к снижению частоты патологии сердечно-сосудистой системы (321, 322); снижается риск смерти (333); значительно снижается риск нейропсихических нарушений (334 - 336); почти у половины детей происходит серореверсия - исчезновение антител к ВИЧ (325, 337, 338); сокращается время достижения вирусологической супрессии (339); стойкое подавление репликации вируса и подавление резервуаров ВИЧ (по исследованию количества тотальной ДНК ВИЧ) сохраняется вплоть до подросткового возраста (340).
- Рекомендуется быстрое начало АРТ (в течение 2х недель от момента постановки на диспансерный учет) детям с подтвержденной ВИЧ-инфекцией в возрасте >= 1 года < 6 лет с выраженными клиническими проявлениями (стадии 2В, 4Б, 4В по РК, а также проявления СПИД-индикаторных заболеваний) и/или с тяжелым иммунодефицитом (CD4 <= 500 клеток/мм3) с целью предотвращения быстрого прогрессирования заболевания и наступления летального исхода (см. табл. 2) [199] (A2).
- Рекомендуется быстрое начало АРТ (в течение 2х недель от момента постановки на диспансерный учет) детям в возрасте 6 лет и старше с выраженными клиническими проявлениями (стадии 2В, 4Б, 4В по РК, а также проявления СПИД-индикаторных заболеваний) и/или с выраженными иммунными нарушениями (CD4 <= 200 клеток/мм3) с целью предотвращения быстрого прогрессирования заболевания и наступления летального исхода (см. табл. 2) [97, 200, 309] (B3).
Таблица 2. Показания к быстрому началу АРТ у детей
|
Критерий
|
Показания
|
|
|
Возраст
|
младше 1 года
|
|
|
Клинические проявления
|
стадии 2В, 4Б, 4В по Российской классификации
|
|
|
Уровень CD4, клеток/мм3
|
1 г - 5 лет
|
<= 500
|
|
6 лет и старше
|
<= 200
|
|
- Рекомендуется при выявлении тяжелых вторичных/оппортунистических инфекций у детей с очень низким количеством CD4-лимфоцитов (< 50 - 100 клеток/мм3), не получающих АРТ, вначале начать лечение вторичной инфекции, а после стабилизации состояния начать АРТ с целью предотвращения утяжеления вторичных/оппортунистических инфекций на фоне синдрома восстановления иммунной системы [97, 200, 201] (B3).
Комментарий: при выявлении ВИЧ-инфекции (или поступлении под наблюдение) ребенка с поздними стадиями ВИЧ-инфекции и выраженными клиническими проявлениями на фоне очень низких показателей CD4-лимфоцитов перед началом АРТ следует убедиться в отсутствии вторичных инфекций, требующих неотложного этиотропного лечения. Если вначале назначить АРТ, возможно развитие угрожающего жизни воспалительного синдрома восстановления иммунной системы. При туберкулезе АРТ начинают, как правило, не позднее 2х недель после начала лечения противотуберкулезными препаратами; при криптококковом менингите АРТ начинают не ранее чем через 2 недели от начала противогрибковой терапии (как правило, через 5 недель).
АРТ может быть отложена на короткий срок, требующийся для проведения уточняющих исследований и для подготовки пациента к лечению.
3.2 Выбор схемы стартовой АРТ
Классификация АРВП представлена в разделе 7. Дополнительная информация.
Приведенная ниже информация о применении АРВП у детей может иметь отличия от инструкций к лекарственным препаратам по медицинскому применению, зарегистрированным на территории Российской Федерации. При выборе схем АРТ и дозирования АРВП были учтены рекомендации Всемирной Организации Здравоохранения, Педиатрической Европейской Сети по Лечению ВИЧ-инфекции (PENTA), Европейского клинического общества по СПИДу (EACS), Панели экспертов по АРТ и ведению детей с ВИЧ-инфекцией (Департамент здравоохранения США), российских экспертов, а также инструкций к АРВП, утвержденных Администрацией по пищевым и лекарственным продуктам США (FDA) и Европейским Медицинским Агентством (EMA) [16, 81, 202, 203, 281, 294]. Обоснованием является Распоряжение Правительства Российской Федерации 16.05.2022 г. N 1180-р (в редакции Распоряжения Правительства Российской Федерации от 01.08.2023 N 2064-р) об утверждении Перечня заболеваний или состояний (групп заболеваний или состояний), при которых допускается применение лекарственного препарата в соответствии с показателями (характеристиками) лекарственного препарата, не указанными в инструкции по его применению.
Стартовая схема лечения (первая линия АРТ) назначается "наивным" пациентам, не получавшим АРВП в качестве лечения, и состоит из 2-х НИОТ и третьего препарата: или 1 ННИОТ, или 1 ИП, или 1 ИИ (таблица 3).
- Рекомендуется осуществлять выбор АРВП на индивидуализированной основе, с учетом характеристик препаратов и ребенка, сопутствующих заболеваний и состояний, данных об эффективности АРВП и их побочных действий, особенностей ухода за ребенком с целью выбора оптимальной для ребенка схемы АРТ на длительный срок [96, 193, 194] (A2).
- Рекомендуется в качестве стартовой АРТ с целью эффективного подавления ВИЧ назначить схему из трех АРВП: 2 НИОТ плюс третий препарат из группы ИИ или ИП или ННИОТ [96, 198, 204 - 209] (A1)
Комментарий: Основой стартовой схемы АРТ является применение трех препаратов одновременно для подавления различных стадий развития вируса, т.е. относящихся к различным классам. В качестве стартовой терапии используют комбинацию из двух нуклеозидных/нуклеотидных ингибиторов обратной транскриптазы и одного препарата из группы ингибиторов протеазы, ненуклеозидных ингибиторов обратной транскриптазы или ингибиторов интегразы ВИЧ: 2 НИОТ + 1 ИП или 2 НИОТ + 1 ННИОТ, или 2 НИОТ + 1 ИИ.
- НЕ рекомендуется назначать детям стартовую схему АРТ в виде одного АРВП (монотерапия), двух АРВП (битерапия), трех НИОТ или включающую препараты из трех классов с целью предотвращения формирования мутаций устойчивости ВИЧ [96, 198, 204 - 208] (A1).
Комментарий: Использование неполноценных схем АРТ ведет к развитию резистентности ВИЧ и потери контроля над течением инфекции. Особая ситуация предусмотрена для ВИЧ-инфицированных детей с подавленной ВН ВИЧ на период лечения туберкулеза с использованием рифампицина** (противопоказан до 3 лет): в случае невозможности применения полноценной АРТ в этот период ребенок переводится на схему из 3-х НИОТ. В настоящий момент времени отсутствуют данные о возможности упрощения схемы АРТ (симплификации) до би- и монотерапии у детей со стабильным течением ВИЧ-инфекции и полной супрессией вируса (у взрослых пациентов такая возможность доказана в рандомизированных клинических исследованиях).
- Рекомендуется начать стартовую терапию препаратами предпочтительного ряда в зависимости от возраста пациента с целью наиболее оптимального выбора препаратов [96] (C5).
Комментарий: Комбинации АРВП делят на предпочтительные, альтернативные и используемые в особых случаях. При выборе схемы стартовой терапии следует в первую очередь рассмотреть возможность применения предпочтительных препаратов/схем.
- Рекомендуется в качестве стартовой терапии назначать препараты, которые в сочетании с двумя НИОТ составляют предпочтительные схемы АРТ в зависимости от возраста ребенка:
- Младше 2х недель: невирапин** [210, 211]; (B2)
- От 2х недель до 6 лет: лопинавир + ритонавир** [211, 212] (A2)
- От 2х до 6 лет: ралтегравир** [209, 413]; (B2)
- Старше 6 лет: долутегравир** [214] (C4).
- Рекомендуется в качестве стартовой терапии использовать АРВП с ФКД, включающие все препараты схемы в одной таблетке в зависимости от возраста ребенка:
- Старше 6 лет: Биктегравир + Тенофовира алафенамид + Эмтрицитабин** [302, 303]; (C4).
- Рекомендуется в составе стартовой терапии назначать препараты, которые составляют нуклеотидную основу схемы АРТ и являются предпочтительными в зависимости от возраста ребенка:
- Младше 2х недель: зидовудин** + #ламивудин** [230, 341 - 346] (C4);
- От 2х недель до 3х месяцев: #абакавир** + #ламивудин** [230, 281, 341 - 353] (B2);
- Старше 3х месяцев: абакавир** + ламивудин** [230, 281, 341 - 353] (B2);
- Старше 12 лет: тенофовир** + ламивудин** или тенофовир** + эмтрицитабин или абакавир** + ламивудин** [16, 96, 169] (C5)
- Рекомендуется в качестве альтернативы в составе стартовой терапии в сочетании с двумя НИОТ следующие АРВП в зависимости от возраста ребенка:
- От 2х недель до 3х лет: невирапин** [204, 216, 217] (B2);
- От 2х до 6 лет: #этравирин** [301, 404] (C4);
- Старше 3х лет: эфавиренз** [204, 217, 218] (C4);
- Старше 6 лет: лопинавир + ритонавир** [219] (B2) или ралтегравир** или эфавиренз** [209, 307] (B2) [206] (A2);
- Старше 12 лет: эфавиренз** [209, 307] (B2).
- Рекомендуется в качестве альтернативы в составе стартовой терапии следующие сочетания НИОТ в зависимости от возраста ребенка:
- От 2х недель до 3х месяцев: зидовудин** + #ламивудин** [216] (B2)
- Старше 3х месяцев: зидовудин** + ламивудин** [216] (B2)
- Старше 3х лет: фосфазид** [412] (C5) + ламивудин** [216]. (B2)
- Рекомендуется в качестве альтернативы использовать АРВП с ФКД, включающие все препараты схемы в одной таблетке, в зависимости от возраста ребенка:
- Старше 6 лет: Кобицистат + Тенофовира алафенамид + Элвитегравир + Эмтрицитабин** [221, 405] (C4);
- Старше 12 лет: Рилпивирин + Тенофовир + Эмтрицитабин** [222] (4C).
Комментарий: Альтернативные схемы включают препараты с более выраженными побочными эффектами, либо более сложные в дозировании и др. и могут быть применены в случае, когда выявлены противопоказания для назначения предпочтительных препаратов/схем, обусловленные различными причинами (отклонения лабораторных показателей, возможные лекарственные взаимодействия, ожидаемые непереносимость и токсичность, возрастные особенности, возможное наступление беременности и другие).
- Рекомендуется при невозможности подобрать для стартовой АРТ препараты из группы предпочтительных или альтернативных (т.е. в особых случаях) у детей в возрасте старше 6 лет назначить #этравирин** [300, 301] (C4).
Комментарий: К категории используемых в особых случаях отнесены АРВП, которые менее изучены, либо имеют возрастные особенности применения и т.д. Эти препараты назначаются только при отсутствии выбора препаратов предпочтительной или альтернативной группы.
Последующие линии терапии (вторая и т.д., резервная) назначаются при вирусологической неэффективности предыдущей линии терапии, подбираются с учетом результатов исследования резистентности ВИЧ к АРВП и экспертного мнения.
Назначение АРТ и выбор схемы проводится по решению врачебной комиссии после рассмотрения показаний и противопоказаний к назначению конкретных АРВП и расчета надлежащих терапевтических доз препаратов.
Выбор схемы терапии осуществляется с учетом соматического статуса ребенка и возможных межлекарственных взаимодействий в случае лечения вторичных/сопутствующих заболеваний во избежание значимых колебаний плазменных концентраций препаратов. Особого внимания требуют: снижение функции печени и почек, замедляющее клиренс метаболизируемых ими препаратов; прием препаратов для лечения туберкулеза; гормональные и противосудорожные препараты. В сложных случаях следует подбирать альтернативные схемы лечения (как ВИЧ-инфекции, так и сопутствующей патологии) или привлечь клинического фармаколога для пересчета доз препаратов.
- Рекомендуется производить оптимизацию схем АРВТ у детей, получающих препараты с невысоким барьером резистентности, при появлении возможности назначения более мощных режимов для минимизации появления резистентных штаммов [90, 106] (C4).
Таблица 3. Препараты стартовой АРТ в зависимости от возраста ребенка [96, 221 - 224]
|
Возраст
|
Предпочтительные
|
Альтернативные
|
||
|
НИОТ
|
3-й препарат
|
НИОТ
|
3-й препарат
|
|
|
0 < 2 нед
|
ZDV** + #3TC**
|
NVP**
|
#ABC** + #3TC** (в особых случаях)
|
-
|
|
>= 2 нед < 3 мес
|
#ABC** + #3TC**
|
LPV + r**
|
ZDV** + #3TC**
|
NVP**
|
|
>= 3 мес < 2 лет
|
ABC** + 3TC**
|
LPV + r**
|
ZDV** + 3TC**
|
NVP**
|
|
>= 2 < 3 лет
|
ABC** + 3TC**
|
LPV + r**
RAL**
|
ZDV** + 3TC**
|
#ETR**
|
|
>= 3 < 6 лет
|
ABC** + 3TC**
|
LPV + r**
RAL**
|
ZDV** + 3TC**
Ф-АЗТ** + 3TC**
|
#ETR**
EFV**
|
|
>= 6 < 12 лет
|
ABC** + 3TC**
|
RAL**
BIC + TAF + FTC**
DTG**
|
ZDV** + 3TC**
Ф-АЗТ** + 3TC**
|
EFV**
DRV** + r**
ATV** + r**
#ETR** (в особых случаях)
LPV + r**
|
|
EVG + COBI + TAF + FTC**
|
||||
|
>= 12 лет
|
TDF** + 3TC**
TDF** + FTC
ABC** + 3TC**
|
DTG**
ATV** + r**
BIC + TAF + FTC**
|
ZDV** + 3TC**
|
EFV**
DRV** + r**
RAL**
#ETR** (в особых случаях)
LPV + r**
|
|
RPV + TDF + FTC**
EVG + COBI + TAF + FTC**
|
||||
3.3 Изменение схемы стартовой АРТ
Основными задачами при проведении АРТ у детей являются:
- достижение и длительное поддержание клинической, иммунологической и вирусологической эффективности АРТ;
- длительная безопасность АРТ (минимизация побочных действий АРВП);
- хорошая переносимость АРВП;
- формирование и сохранение высокой приверженности лечению.
При проведении АРТ довольно часто встает вопрос о замене одного - двух препаратов в схеме или всей схемы полностью.
Если при проведении стартовой (первой линии) терапии достигнуты клиническая, иммунологическая и вирусологическая эффективность лечения, частичное или полное изменение схемы лечения осуществляется в пределах первой линии АРТ.
- Рекомендуется расценивать замену препарата(ов) в схеме АРТ или всей схемы АРТ на фоне достигнутой клинической, иммунологической и вирусологической эффективности как оптимизацию лечения [192, 193, 208] (B2).
Комментарий: среди факторов, лежащих в основе необходимости смены терапии, основными у детей являются:
- низкая приверженность лечению;
- токсичность и непереносимость терапии;
- получение новых данных о возможности применения у ребенка более эффективных препаратов или их комбинаций, чем текущая терапия;
- необходимость применения препаратов, несовместимых с назначенными АРВП;
- неэффективность проводимой терапии и очевидное прогрессирование болезни, подтвержденное клиническими, иммунологическими и вирусологическими параметрами (может быть следствием низкой приверженности лечению, непереносимости терапии или развития резистентности).
Особенности причин неэффективности у детей и тактика ведения ребенка при появлении признаков токсичности/непереносимости АРВП представлены в разделе 7. Дополнительная информация.
3.3.1 Изменение схемы АРТ при выявлении неэффективности лечения
Эффективность АРТ оценивается на протяжении всего периода приема АРТ. Для решения вопроса об эффективности АРТ используют клинические, иммунологические и вирусологические показатели. Наиболее четко сформулированы критерии оценки вирусологической эффективности лечения, в меньшей степени - клинической эффективности, в отношении иммунологической эффективности единого мнения нет.
АРТ 2й линии - это следующий режим (схема), назначаемый сразу после выявления неэффективности АРТ первой линии - клинической и/или иммунологической, и/или вирусологической.
Оценка вирусологической эффективности АРТ
Наиболее частые причины вирусологической неудачи изложены в разделе 7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния).
Алгоритм оценки вирусологической эффективности АРТ у детей изложен в Приложении Б. Алгоритмы действий врача.
- Рекомендуется оценивать эффективность АРТ определением динамики снижения ВН ВИЧ и считать вирусологической супрессией уровень РНК ВИЧ < 50 копий/мл через 6 месяцев АРТ [225, 226] (B1).
Комментарий: Об эффективности лечения свидетельствуют следующие показатели динамики вирусной нагрузки: снижение более чем на 1 log10 через 4 недели лечения; снижение более чем на 3 log10 через 12 недель лечения; снижение до неопределяемого уровня (< 50 копий/мл плазмы) через 24 недели лечения. Для оценки вирусологической эффективности не рекомендуется использовать тест-системы с порогом чувствительности 200 копий/мл и выше, т.к. они могут не выявить неполное подавление репликации ВИЧ, которое способствует пополнению латентных резервуаров ВИЧ и формированию резистентных к лечению штаммов ВИЧ, препятствует успешному восстановлению иммунной системы и может привести к прогрессированию заболевания [227 - 229].
- Рекомендуется считать вирусологической неудачей АРТ уровень РНК ВИЧ более 200 копий/мл в двух последовательных исследованиях с интервалом в 3 - 4 недели при строгом соблюдении режима приема препаратов минимум через 24 недели текущей схемы АРТ [225, 226, 230] (B1).
Комментарий: Под вирусологической неэффективностью (неудачей) АРТ понимают неполное подавление репликации ВИЧ (недостижение вирусологической супрессии) или рецидив ВН после достижения неопределяемых уровней, оцениваемые минимум через 24 недели от начала текущей схемы АРТ.
У детей с высокой ВН до начала АРТ возможно определение ВН > 200 копий после 24 недель АРТ. При использовании в схеме стартовой АРТ ингибиторов протеазы ВИЧ снижение ВН на 1,5 - 2,0 log10 (в 50 - 100 раз) по сравнению с фоновым уровнем позволяет продолжить ранее выбранную терапевтическую схему и усилить работу по повышению приверженности лечению. У детей, получающих в схеме стартовой АРТ ненуклеозидные ингибиторы обратной транскриптазы ВИЧ, отсутствие вирусологической супрессии может быть сопряжено с формированием лекарственной устойчивости, что потребует смены АРТ.
Кратковременное повышение ВН (как правило, до уровня 1.000 копий/мл) может быть связано с вакцинацией, введением глобулиновых фракций, интоксикацией, сопутствующим заболеванием, не связанным с ВИЧ, и не считается вирусологической неудачей, если уровень ВН через 1 месяц после купирования снизился до неопределяемого уровня (< 50 копий/мл).
- Не рекомендуется продолжать текущую схему АРТ при документированной вирусологической неудаче - следует изменить схему АРТ [231, 232] (C4).
Комментарий: При решении вопроса о смене стартовой схемы АРТ у детей первых лет жизни не следует торопиться - выбор препаратов у детей ограничен - но и не следует затягивать этот процесс, особенно если ребенок получает ННИОТ.
Решение о переходе на вторую линию АРТ принимается врачебной комиссией с учетом индивидуальных особенностей ребенка, после детальной оценки динамики ВН, приверженности лечению, клинической и иммунологической эффективности и лабораторных параметров и при получении убедительных доказательств в пользу того, что продолжение первой линии АРТ нецелесообразно.
Для выбора активных препаратов второй линии настоятельно рекомендуется провести исследование чувствительности ВИЧ к АРВП - молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1). В новую схему следует включить как минимум 2 АРВП с высокой активностью против ВИЧ.
Оценка клинической эффективности АРТ
- Рекомендуется считать критериями клинической неэффективности АРТ у детей [233, 234] (C4):
- прогрессирующее ухудшение неврологических показателей, включающее два и более признака из следующих: нарушение роста головного мозга, нарушение когнитивных функций, появление двигательных дисфункций;
- нарушение роста (несмотря на адекватное питание и в отсутствие других причин);
- прогрессирование болезни, определяемое как переход из одной клинической стадии в другую;
- появление новых или прогрессирование ранее выявленных вторичных инфекций/заболеваний.
Комментарий: Клиническая неэффективность лечения является наиболее неблагоприятной ввиду возможного быстрого прогрессирования ВИЧ-инфекции.
У детей, начавших АРТ на фоне низких показателей иммунного статуса, при быстрой положительной динамике CD4 и прогрессивном снижении ВН появление новых вторичных заболеваний в первые недели и месяцы лечения может свидетельствовать об эффективности лечения и развитии воспалительного синдрома восстановления иммунной системы, в структуре которого наиболее тяжело могут протекать туберкулезная инфекция и криптококковый менингит. Перед началом АРТ (особенно на фоне выраженного и тяжелого иммунодефицита) рекомендуется провести тщательное обследование ребенка на туберкулез и другие вторичные заболевания.
Если прогрессирование болезни не связано с неврологическими нарушениями или задержкой роста, при решении вопроса об изменении терапии следует учитывать иммунологические и вирусологические показатели.
Оценка иммунологической эффективности АРТ
- Не рекомендуется менять схему АРТ при достижении клинической и вирусологической эффективности, поскольку это, как правило, не приводит к значимым изменениям со стороны иммунного статуса [235] (B2).
Комментарий: Четкие иммунологические критерии неэффективности АРТ в настоящее время отсутствуют [225]. У большинства больных, получающих АРТ, в течение многих лет лечения происходит увеличение уровня CD4-лимфоцитов: при выраженном и тяжелом иммунодефиците на момент начала лечения восстановление иммунного статуса происходит очень медленно, а у части больных повышается незначительно.
Методов, направленных на стимулирование роста количества CD4-лимфоцитов, в настоящее время нет. Принято считать, что иммунологический эффект достигнут, если % содержание и/или абсолютное количество CD4-лимфоцитов превысило возрастные показатели тяжелого иммунодефицита. Повышение CD4 до уровня, безопасного в отношении развития оппортунистических инфекций (т.е. более 200 клеток/мм3), является приемлемым, а повышение более 350 клеток/мм3 - адекватным результатом лечения.
При наличии лимфопении следует провести анализ возможных причин и провести соответствующую коррекцию: заменить АРВП и препараты сопутствующей терапии, обладающие лейкопеническим действием, провести обследование с целью выявления вторичных и сопутствующих заболеваний и др.
Смена АРТ вследствие вирусологической неэффективности
Важнейшая задача при назначении терапии второй и последующих линий - добиться полной вирусологической супрессии.
- Рекомендуется при получении клинико-лабораторных данных, подтверждающих неэффективность проводимой терапии, провести молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) к АРВП-генотипирование [236 - 238] (C4).
Комментарий: Исследование резистентности проводится на фоне АРТ, в крайнем случае течение 2х недель после прекращения приема всех препаратов схемы (следует учитывать длительный период полувыведения ННИОТ). При ВН от 500 до 1.000 копий/мл плазмы мутации могут остаться невыявленными с помощью обычных методов (не высокочувствительных).
- Рекомендуется при выявлении мутаций резистентности к определенным препаратам произвести смену только этих препаратов: назначаются препараты, к которым ВИЧ сохранил высокую чувствительность [96, 237] (C5).
- Рекомендуется при выявлении резистентности к ненуклеозидному ингибитору обратной транскриптазы выбрать третьим препаратом бустированный ингибитор протеазы или ингибитор интегразы, см. таблицу 4 [96, 231, 232, 239] (C4).
- Рекомендуется при выявлении резистентности к ингибитору протеазы выбрать третьим препаратом ингибитор интегразы, или ненуклеозидный ингибитор обратной транскриптазы, или другой бустированный активный ингибитор протеазы с лучшей переносимостью, см. таблицу 4 [96, 231, 232, 239 - 245] (B2).
Комментарий: Ингибиторы протеазы ВИЧ обладают высоким барьером резистентности и при их применении редко формируется резистентность ВИЧ к АРВП, что позволяет использовать при вирусологической неудаче другой бустированный ингибитор протеазы с лучшей переносимостью. При замене ингибиторов протеазы препаратами других классов следует учитывать, что многие из них обладают более низким барьером резистентности, что требует высокой приверженности лечению [246 - 248].
- Рекомендуется по возможности сохранить в новой схеме АРТ ламивудин** (с учетом возрастных противопоказаний) или эмтрицитабин** (с учетом возрастных противопоказаний) вторым или третьим НИОТ, если к нему сформировалась мутация M184V/I (в сочетании с зидовудином** или тенофовиром** (с учетом возрастных противопоказаний) [249 - 251] (C4B3).
Комментарий: мутация M184V/I повышает антивирусную активность зидовудина** и тенофовира**. Следование данной рекомендации зависит от возраста ребенка, кратности приема препаратов, количества препаратов и таблеток/растворов, приверженности АРТ.
- Не рекомендуется повышать или снижать терапевтические дозы АРВП у детей, или экстраполировать на детский возраст дозировки, используемые у взрослых [252, 253] (C5).
- Рекомендуется при невозможности определить наличие мутаций резистентности ВИЧ к АРВП сменить всю схему целиком, ориентируясь на предшествующее лечение и результаты генотипирования в прошлом (что существенно ограничивает выбор препаратов в будущем) [254] (B3).
Таблица 4. Возможные варианты выбора схем АРТ при неэффективности предыдущей линии терапии
|
АРТ, подлежащая замене
|
Рекомендуемая новая схема
|
|
2 НИОТ плюс ННИОТ
|
2 НИОТ плюс ИП плюс ритонавир**
2 НИОТ плюс ИИ
|
|
2 НИОТ плюс ИП
|
2 НИОТ плюс ННИОТ
2 НИОТ плюс ИИ
2 НИОТ плюс ИП с другим профилем резистентности плюс ритонавир**
|
|
2 НИОТ плюс ИИ
|
2 НИОТ плюс ИП плюс ритонавир**
2 НИОТ плюс ННИОТ
|
|
Выявление множественной лекарственной устойчивости
|
Сочетание любых 3х и более препаратов, к которым сохранилась высокая чувствительность
|
- Рекомендуется при выявлении у ребенка прогрессирующего ухудшения неврологических показателей на фоне проводимой АРТ в новую схему терапии включить препараты, проникающие через гематоэнцефалический барьер [255, 256] (C4).
Комментарий: Показана связь между степенью проникновения АРВП в ЦНС и уровнем РНК ВИЧ в ЦНС, а также с частотой и выраженностью неврологических проявлений, включая ВИЧ-ассоциированную деменцию. Хорошей способностью к проникновению в ЦНС у детей обладают следующие АРВП: зидовудин**, невирапин**, эфавиренз**, абакавир**, атазанавир** + ритонавир**, ламивудин**, лопинавир + ритонавир**; более низкая способность к проникновению в ЦНС отмечена у тенофовира**, эмтрицитабина**. [255, 256]. Более подробная актуализированная информация представлена в табл. 21. Шкала оценки степени проникновения АРВП в ЦНС в Приложении А3. Справочные материалы.
- Рекомендуется при выборе АРВП у детей, особенно младшего возраста, учитывать их вкусовые качества, размер и количество таблеток, объемы растворов, кратность приемов в сутки и другие факторы, которые могут повлиять на приверженность АРТ [192, 193, 257] (A2).
3.3.2 Изменение схемы АРТ при развитии нежелательных реакций и лекарственных взаимодействий
Оценка безопасности проводимой АРТ предполагает профилактику и выявление нежелательных реакций при применении антиретровирусных препаратов, а также тактику ведения ребенка в случае их возникновения.
- Рекомендуется проводить регулярный мониторинг токсичности АРПВ на протяжении всего периода АРТ (см. таблицу 23 и таблицу 24 в разделе 7. Дополнительная информация) [136] (B2).
Комментарий: Выделяют следующие нежелательные реакции при проведении АРТ у детей:
- митохондриальная дисфункция (лактацидоз, гепатотоксичность, кардиотоксичность, панкреатит, периферическая нейропатия);
- метаболические нарушения (нарушения липидного обмена - липодистрофия, гиперлипидемия; гипергликемия и инсулинорезистентность;
- остеопения, остеопороз и остеонекроз,
- поражение почек;
- гематологические нарушения (анемия, нейтропения и тромбоцитопения);
- аллергические реакции (кожные высыпания и реакции гиперчувствительности).
Последние 2 группы НР относятся к быстрым (проявляются обычно в первые несколько недель лечения), остальные - к отсроченным.
- Рекомендуется, если терапия меняется по причине токсичности или непереносимости, заменить препарат, вызвавший нежелательные реакции, на препарат с другим профилем токсичности и переносимости [192, 193, 257] (A2).
- Рекомендуется при развитии угрожающих жизни нежелательных реакций немедленно прекратить АРТ; после исчезновения симптомов возобновить АРТ с заменой причинного препарата(ов) [192, 193, 257] (A2).
- Рекомендуется при развитии реакции гиперчувствительности к абакавиру** немедленно отменить его и никогда не назначать в будущем; следует забрать у пациента все оставшиеся лекарственные формы этого препарата [119, 258] (B2).
Комментарий: В ряде случаев (токсические эффекты, взаимодействие лекарств, отсутствие препарата и т.д.), может быть использован режим лечения, включающий временную отмену всех препаратов, входящих в комплекс АРТ (при отсутствии выраженной иммуносупрессии) во избежание селекции устойчивых штаммов ВИЧ. Достоверных сведений о длительности перерыва (без последствий для больного) нет, продолжение же приема только одного или двух препаратов может повысить репликативную активность вируса и способствовать формированию мутаций резистентности. Такой перерыв возможен в крайних случаях только под контролем CD4-лимфоцитов и вирусной нагрузки при умеренной иммуносупрессии у больного. Если в схему АРТ входил ННИОТ, после его отмены рекомендуется продолжить 2 НИОТ в течение 10 - 14 дней во избежание эффекта монотерапии и формирования лекарственной устойчивости ВИЧ к ННИОТ (период выведения ННИОТ значительно более длительный, чем у других АРВП, что приводит к поддержанию низких уровней ННИОТ - в отсутствие других АРВП - в зоне высокого селективного давления и образованию мутаций резистентности).
При выборе тактики временной отмены всех препаратов следует учитывать, что она сопряжена с быстрым увеличением ВН и возможным быстрым прогрессированием ВИЧ-инфекции.
При изменении схемы АРТ необходимо проанализировать прием больным всех других лекарств с учетом возможных взаимодействий между препаратами.
Тактика ведения ребенка при появлении признаков токсичности/непереносимости АРВП представлена в разделе 7. Дополнительная информация.
[1] Распоряжение Правительства Российской Федерации от 20 октября 2016 г. N 2203-р "Об утверждении Государственной стратегии противодействия распространению ВИЧ-инфекции в Российской Федерации на период до 2020 года и дальнейшую перспективу".
[2] Федеральный закон от 21 ноября 2011 г. N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации".
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Медицинская реабилитация - комплекс мероприятий медицинского и психологического характера, направленных на полное или частичное восстановление нарушенных и (или) компенсацию утраченных функций пораженного органа либо системы организма, поддержание функций организма в процессе завершения остро развившегося патологического процесса или обострения хронического патологического процесса в организме, а также на предупреждение, раннюю диагностику и коррекцию возможных нарушений функций поврежденных органов либо систем организма, предупреждение и снижение степени возможной инвалидности, улучшение качества жизни, сохранение работоспособности пациента и его социальную интеграцию в общество [304].
Медицинская реабилитация осуществляется в медицинских организациях и включает в себя комплексное применение природных лечебных факторов, лекарственной, немедикаментозной терапии и других методов [304]
Принцип медицинской реабилитации - комплексная реализация пациент-центрированного, проблемно-ориентированного и мультидисциплинарного подхода [305].
- Рекомендуется специалистам медицинской организации, ответственной за наблюдение ВИЧ-инфицированного ребенка, при выявлении патологических состояний направлять детей к специалистам соответствующего профиля для решения вопроса о проведении медицинской реабилитации, которая осуществляется на общих основаниях [406, 407] (B3).
Комментарий. У ВИЧ-инфицированных детей с высокой частотой выявляются патологические состояния, обусловленные ВИЧ-инфекцией - нейротропностью вируса иммунодефицита человека, длительным течением заболевания, хронической активацией иммунной системы, поздним началом антиретровирусной терапии, длительным применением препаратов с неблагоприятным метаболическим профилем, а также сопутствующими заболеваниями и состояниями. В патологический процесс при ВИЧ-инфекции вовлекаются все органы и системы и в первую очередь - центральная нервная, сердечно-сосудистая и дыхательная системы. В раннем детском возрасте ВИЧ-энцефалопатия проявляется задержкой психомоторного развития; у подростков на первый план выходят когнитивные расстройства (нарушения памяти, внимания, мышления), нарушения поведения и психические расстройства [306, 407]. Указанные патологические состояния приводят к нарушению формирования и поддержания медикаментозной приверженности у ребенка, снижению эффективности антиретровирусной терапии, развитию иммунного дефицита, прогрессированию ВИЧ-инфекции с наступлением неблагоприятного исхода.
Для проведения санаторно-курортного лечения у ВИЧ-инфицированных детей следует осуществлять отбор на общих основаниях [1]. ВИЧ-инфекция у ребенка не является прямым показанием для проведения санаторно-курортного лечения, однако, учитывая ее мультиморбидный характер, санаторно-курортное лечение призвано оказывать благоприятное воздействие на течение ВИЧ-инфекции и коморбидных заболеваний/состояний, способствовать интеграции детей в социальную среду, положительно влиять на приверженность наблюдению и лечению.
--------------------------------
[1] Приложение N 3 к Приказу Министерства здравоохранения Российской Федерации от 28 сентября 2020 г. N 1029н "Об утверждении перечней медицинских показаний и противопоказаний для санаторно-курортного лечения".
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
5.1. Профилактика передачи ВИЧ-инфекции от матери ребенку
Профилактика ВИЧ-инфекции у детей подразумевает, в первую очередь, соблюдение протокола ППМР, а также всего комплекса противоэпидемических мероприятий, предусмотренных санитарными правилами и законодательством Российской Федерации [1, 259 - 261].
Профилактика передачи ВИЧ-инфекции от матери ребенку - комплексная задача, решение которой зависит от успешного выполнения следующих этапов:
- первичной профилактики ВИЧ-инфекции у женщин репродуктивного возраста;
- раннего выявления ВИЧ-инфекции у женщин детородного возраста;
- назначения АРТ ВИЧ-инфицированным женщинам, планирующим беременность;
- назначения АРТ всем ВИЧ-инфицированным беременным;
- выбора способа родоразрешения в зависимости от показателей ВН у женщины перед родами;
- назначения АРТ в родах;
- назначения АРТ ребенку;
- отказа от грудного вскармливания;
- консультирования матери на всем протяжении беременности, во время родов и после рождения ребенка по вопросам профилактики передачи ВИЧ-инфекции от матери ребенку.
- Рекомендуется всем новорожденным с перинатальным контактом по ВИЧ назначать антиретровирусные препараты для снижения риска перинатальной передачи ВИЧ [318, 408] (A1).
- Рекомендуется врачам, ответственным за наблюдение беременных женщин, проводить химиопрофилактику перинатальной передачи ВИЧ новорожденному при наличии:
- ВИЧ-инфекции у матери [267 - 271, 408] (A1);
- положительного результата экспресс тестирования на ВИЧ-инфекцию у матери [267 - 271, 408] (A1);
- эпидемиологических показаний [264, 265] (C5).
Комментарий: Химиопрофилактика передачи ВИЧ от матери ребенку осуществляется путем назначения АРВП женщине в период беременности и родов, а также новорожденному. В исключительных случаях (если женщина, вопреки рекомендациям, не отказывается от грудного вскармливания ребенка) эти препараты назначают с профилактической целью матери и/или ребенку в период грудного вскармливания.
Эпидемиологическими показаниями являются:
- парентеральное употребление матерью наркотиков во время беременности,
- регулярные незащищенные половые контакты с ВИЧ-позитивным половым партнером, у которого определяемый или неизвестный уровень ВН ВИЧ.
- Рекомендуется начинать прием АРВП у новорожденных как можно быстрее после рождения, в пределах первых 4 - 6 часов [230, 307, 318 - 322, 360, 368] (B2).
Комментарий: Если с момента последнего возможного риска заражения ребенка (после родов или после последнего вскармливания грудным молоком) прошло более 72 часов (3-х дней), назначение химиопрофилактики нецелесообразно ввиду ее неэффективности [369], так как через 24 часа после внедрения ВИЧ в организм начинается его активная репликация в клетках [320].
- Период пребывания родильницы с положительным результатом экспресс-тестирования на ВИЧ и ее новорожденного ребенка в родильном доме рекомендовано продлевать до получения подтверждающих результатов обследования на ВИЧ-инфекцию с целью определения дальнейшей тактики ведения [1, 310, 311, 312] (B3).
Пересчет дозы АРВП у новорожденного следует производить не реже 1 раза в 10 дней.
Схема АРТ для новорожденных должна определяться с учетом факторов матери и ребенка, влияющих на риск перинатальной передачи ВИЧ
- Рекомендуется назначить новорожденному профилактическую схему АРТ в виде монотерапии зидовудином** на срок 4 недели при низком риске перинатального инфицирования [190, 230, 262, 263, 272, 281, 307 - 309] (A1), см. таблицу 5.
Таблица 5. Дозирование #зидовудина** при проведении химиопрофилактики по схеме монотерапии (пероральное или внутривенное введение) (230, 307)
|
Гестационный возраст ребенка, недель
|
Разовая доза
|
Количество приемов в сутки
|
|
|
пероральный раствор
|
раствор для внутривенного введения
|
||
|
> 35
|
4 мг/кг
|
3 мг/кг
|
2
|
|
>= 30 < 35
|
Первые 2 недели жизни:
|
||
|
2 мг/кг
|
1,5 мг/кг
|
2
|
|
|
Старше 2 недель:
|
|||
|
3 мг/кг
|
2,3 мг/кг
|
2
|
|
|
< 30
|
2 мг/кг
|
1,5 мг/кг
|
2
|
Комментарии. Критерии низкого риска передачи ВИЧ от матери ребенку:
- получение матерью АРТ во время беременности;
- вирусная супрессия у ВИЧ-инфицированной матери к 36 недели беременности и/или в течение 4 недель перед родами менее 50 копий/мл.
Дозирование зидовудина** приведено на основании результатов многолетнего исследования фармакокинетики, эффективности и безопасности зидовудина** у новорожденных, в том числе недоношенных, детей [190, 230, 281, 307, 354 - 358].
- Рекомендуется назначить новорожденным с высоким риском перинатального заражения ВИЧ предполагаемую терапию ВИЧ, включающую 3 АРВП - зидовудин** + #ламивудин** + невирапин**, если выявлен высокий риск ВИЧ-инфекции у ребенка, на срок 6 недель, см. таблицы 6, 7 [262 - 266, 272, 307 - 309] (A1).
Комментарий. Критерии высокого риска передачи ВИЧ от матери ребенку:
- мать не получала АРТ во время беременности;
- мать получала АРТ во время беременности, но не достигнута вирусная супрессия (РНК ВИЧ < 50 копий/мл) к 36 недели беременности и/или в течение 4 недель до родов, или данное обследование у матери не проведено или проведено не полностью;
- наличие у матери острой ВИЧ-инфекции во время беременности или во время грудного вскармливания;
- наличие ВИЧ-инфекции у кормящей матери;
- выявлен положительный экспресс-тест у матери во время родов (прием препаратов может быть в дальнейшем прекращен, если наличие ВИЧ-инфекции не будет подтверждено стандартным методом);
Одним из факторов, обеспечивших очень низкие показатели ПМР (< 1%), является высокая частота назначения комбинированной АРТ новорожденным с высоким риском ВИЧ-инфекции, в т.ч. недоношенным [273]. Предполагаемая терапия ВИЧ является, с одной стороны, началом АРТ у тех детей, у которых в дальнейшем подтверждается ВИЧ-инфекция, и с другой стороны она выполняет роль эффективной постконтактной профилактики у детей с высоким риском ВИЧ-инфекции, предотвращая заражение ребенка ВИЧ-инфекцией, поскольку известно, что большинство случаев передачи ВИЧ от матери ребенку происходит перед родами и в родах; грудное вскармливание значительно увеличивает вероятность заражения ребенка (на 16 - 30%).
У ВИЧ-инфицированных детей, начавших АРТ в первые часы после рождения, выявлено снижение размеров вирусных резервуаров, заболевание протекает благоприятнее, снижается риск поражения центральной нервной и сердечно-сосудистой систем, и удается достичь функционального излечения [321, 322].
Зидовудин**, #ламивудин** и невирапин** наиболее хорошо изучены и рекомендуются к применению в составе предполагаемой терапии у новорожденных, включая недоношенных детей, с высоким риском ВИЧ-инфекции.
Дозирование АРВП приведено на основании результатов многолетнего исследования фармакокинетики, эффективности и безопасности у новорожденных, в том числе недоношенных, детей #ламивудина** [190, 230, 281, 307, 341 - 346, 357 - 362]; зидовудина** [190, 230, 281, 307, 346, 354 - 362]; невирапина** [190, 230, 281, 307, 357 - 365].
Если ребенка прикладывали к груди или кормили молоком ВИЧ-инфицированной женщины, рекомендуется начать профилактику в течение первых 6 часов после отлучения от груди. При этом рекомендуется в кратчайшие сроки провести обследование ребенка на нуклеиновые кислоты ВИЧ (количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР; Определение ДНК вируса иммунодефицита человека методом ПЦР, качественное исследование) и продолжать профилактику только при получении отрицательных результатов обследования. При получении двух положительных результатов решить вопрос о начале АРТ у ребенка.
- #Абакавир** не рекомендуется как часть схемы предполагаемой терапии ВИЧ в рутинном порядке, но может быть использован в особых ситуациях [307 - 309] (C5).
Комментарий: в ситуациях, когда зидовудин** недоступен или у младенца имеется связанная с зидовудином** токсичность, абакавир** можно рассматривать как альтернативу зидовудину**. Эту замену следует рассматривать, когда может существовать повышенный риск токсичности зидовудина**, например, у детей раннего возраста с анемией или нейтропенией. В России абакавир** не одобрен для использования у детей младше 3 месяцев. Накоплено достаточное количество данных о безопасности #абакавира** у новорожденных и детей в возрасте до 3х месяцев [190, 230, 281, 307, 347 - 353]. ВОЗ одобрила применение #абакавира** у доношенных детей младше 1 месяца в дозе 2 мг/кг (разовая доза) с приемом два раза в сутки. До применения #абакавира** должен быть подтвержден отрицательный результат тестирования на аллель HLA-B5701 - определения антигена HLA-B27 методом проточной цитофлуориметрии (308, 309).
Таблица 6. Дозирование #зидовудина**, #ламивудина** и #невирапина** у детей при проведении курса предполагаемой терапии (комбинированная АРТ) <1> (230, 307)
|
Гестационный возраст ребенка, недель
|
Разовая доза
|
Суточная доза
|
|
#Зидовудин** (раствор для приема внутрь 10 мг/мл), прием 2РС. С рождения. Курс 6 недель. Независимо от приема пищи
|
||
|
>= 35 недель
|
4 мг/кг
|
8 мг/кг
|
|
>= 30 недель < 35 недель
|
С рождения до возраста 2 недели:
|
|
|
2 мг/кг
|
4 мг/кг
|
|
|
С 2 недель до 6 недель:
|
||
|
3 мг/кг
|
6 мг/кг
|
|
|
< 30 недель
|
С рождения до 4 недель:
|
|
|
2 мг/кг
|
4 мг/кг
|
|
|
С 4 недель до 6 недель:
|
||
|
3 мг/кг
|
6 мг/кг
|
|
|
#Ламивудин** (раствор для приема внутрь, 10 мг/мл), прием 2 РС. С рождения. Курс 6 недель. Независимо от приема пищи
|
||
|
>= 32 недель
|
С рождения до возраста 4 недели:
|
|
|
2 мг/кг
|
4 мг/кг
|
|
|
С 4 недель до 6 недель:
|
||
|
4 мг/кг
|
8 мг/кг
|
|
|
#Невирапин** (суспензия для перорального применения, 10 мг/мл), 2 РС. С рождения. Курс 6 недель. Независимо от приема пищи
|
||
|
>= 37 недель
|
С рождения до 4 недель:
|
|
|
6 мг/кг
|
12 мг/кг
|
|
|
С 4 недель до 6 недель:
|
||
|
200 мг/мм2
|
400 мг/мм2
|
|
|
>= 34 недель < 37 недель
|
С рождения до возраста 1 неделя:
|
|
|
4 мг/кг
|
8 мг/кг
|
|
|
С возраста 1 неделя до возраста 4 недели:
|
||
|
6 мг/кг
|
12 мг/кг
|
|
|
С 4 недель до 6 недель:
|
||
|
200 мг/мм2
|
400 мг/мм2
|
|
|
>= 32 недель < 34 недель
|
С рождения до возраста 2 недели:
|
|
|
2 мг/кг
|
4 мг/кг
|
|
|
С 2 недель до 4 недель:
|
||
|
4 мг/кг
|
8 мг/кг
|
|
|
С 4 недель до 6 недель:
|
||
|
6 мг/кг
|
12 мг/кг
|
|
|
#Абакавир** <2> (Раствор для приема внутрь 20 мг/1 мл) 2 РС. С рождения. Курс 6 недель.
|
||
|
>= 37 недель
|
С рождения до 4 недель:
|
|
|
2 мг/кг
|
4 мг/кг
|
|
|
С 4 недель до 6 недель:
|
||
|
4 мг/кг
|
8 мг/кг
|
|
Примечания:
<1> эти же дозы АРВП применяются при проведении АРТ у детей младше 4-х недель при получении положительных результатов обследования на НК ВИЧ.
<2> рекомендации по дозированию были получены с помощью моделирования фармакокинетики.
Таблица 7. Упрощенная схема назначения #зидовудина** 2 раза в сутки с фиксированной разовой дозой <1> (281, 307)
|
Гестационный возраст ребенка, недель
|
Масса тела ребенка при рождении, кг
|
Разовая доза
|
Суточная доза
|
|
>= 35 недель
|
от 2 до 3
|
10 мг (1,0 мл)
|
20 мг (2,0 мл)
|
|
от 3 до 4
|
15 мг (1,5 мл)
|
30 мг (3,0 мл)
|
|
|
от 4 до 5
|
20 мг (2,0 мл)
|
40 мг (4,0 мл)
|
Примечание: <1> Применяется при возникновении проблем с приверженностью лечению при проведении профилактического курса схемой предполагаемой АРТ.
- Рекомендуется у детей с высоким риском ВИЧ-инфекции продолжать курс предполагаемой терапии (3 АВП) в течение 6 недель с целью предотвращения формирования латентных резервуаров ВИЧ и улучшения отдаленных результатов [323, 359, 370, 371] (A2).
Комментарий: Важно провести обследование новорожденного в возрасте 21 - 28 дней, чтобы до окончания курса принять решение о переходе на терапевтические дозы АРТ (в случае положительного результата обследования на НК ВИЧ методом определения ДНК вируса иммунодефицита человека методом ПЦР, качественное исследование), либо об окончании курса в возрасте 6 недель (в случае отрицательного результата обследования на НК ВИЧ методом определения ДНК вируса иммунодефицита человека методом ПЦР, качественное исследование).
- Рекомендуется врачам, ответственным за наблюдение новорожденных детей, незамедлительно перевести новорожденного на терапевтическую схему АРТ, если в процессе проведения 4х-недельного профилактического курса зидовудином** у него получены положительные результаты обследования на НК ВИЧ [195, 198, 272, 321, 322, 328, 340] (A1).
- #зидовудин** продолжать в назначенной дозе (см. таблицу 6) до возраста 4 недели, а затем перейти на дозы, представленные в таблице 8;
- #ламивудин** назначить в дозе, представленной в таблице 6, до возраста 4 недели, а затем перейти на дозы, представленные в таблице 8;
- #невирапин** назначить в дозе, представленной в таблице 6, до возраста 2 недели, а затем перейти на дозы, представленные в таблице 8.
- возможно произвести замену #невирапина** на лопинавир + ритонавир** у доношенных новорожденных с 14 дней жизни (42 недели гестации).
Комментарий: Следует модифицировать дозы АРВП соответственно возрасту и с учетом срока гестации.
- Рекомендуется врачам, ответственным за наблюдение новорожденных детей, продолжить терапию, если в процессе проведения ППМР комбинированной схемой (см. таблицу 6) у ребенка получены положительные результаты обследования на НК ВИЧ [195, 198, 272, 321, 322, 328, 340] (A1):
- #зидовудином** и #ламивудином** - до возраста 4 недели, а затем перейти на дозы, представленные в таблице 8;
- #невирапином** - до возраста 2 недели, а затем перейти на дозы, представленные в таблице 8, или на прием лопинавира + ритонавира**.
Комментарий: Непосредственный переход с предполагаемой терапии у ребенка с высоким риском ВИЧ-инфекции на лечение ВИЧ-инфекции при подтверждении ВИЧ-инфекции играет драматическую роль, так как обеспечивает стойкое подавление ВИЧ, способствует уменьшению вирусных резервуаров и препятствует образованию новых резервуаров, что приводит к благоприятному течению ВИЧ-инфекции (328). Перерыв между профилактическим курсом АРТ и началом лечения приводит к неконтролируемой активации репликативной активности ВИЧ, быстрому увеличению вирусной нагрузки, формированию лекарственной устойчивости к ННИОТ.
Дозирование АРВП приведено на основании результатов многолетнего исследования фармакокинетики, эффективности и безопасности у новорожденных, в том числе недоношенных, детей ламивудина** (190, 203, 230, 281, 307, 341 - 346, 357 - 362); зидовудина** (190, 230, 281, 307, 346, 354 - 362); невирапина** (190, 230, 281, 307, 357 - 365) с учетом Распоряжения Правительства Российской Федерации 16.05.2022 г. N 1180-р (в редакции Распоряжения Правительства Российской Федерации от 01.08.2023 N 2064-р) об утверждении Перечня заболеваний или состояний (групп заболеваний или состояний), при которых допускается применение лекарственного препарата в соответствии с показателями (характеристиками) лекарственного препарата, не указанными в инструкции по его применению.
Следует модифицировать дозы АРВП соответственно возрасту и с учетом срока гестации.
Таблица 8. Дозирование #зидовудина**, #ламивудина** и #невирапина**, лопинавира+ритонавира** у детей с подтвержденной ВИЧ-инфекцией при проведении лечения схемой комбинированной АРТ (230, 307)
|
Возраст ребенка
|
Разовая доза
|
Суточная доза
|
|
|
#Зидовудин** (раствор для приема внутрь 10 мг/мл), 2 раза в сутки. Независимо от приема пищи
|
|||
|
Срок гестации >= 35 недель
Возраст > 4 недель
|
12 мг/кг
|
24 мг/кг
|
|
|
Срок гестации
>= 30 недель < 35 недель
|
|||
|
Возраст 4 - 8 недель
|
3 мг/кг
|
6 мг/кг
|
|
|
Возраст > 8 недель
|
12 мг/кг
|
24 мг/кг
|
|
|
Срок гестации < 30 недель
|
|||
|
Возраст 4 - 10 недель
|
3 мг/кг
|
6 мг/кг
|
|
|
Возраст > 10 недель
|
12 мг/кг
|
24 мг/кг
|
|
|
#Ламивудин** (раствор для приема внутрь, 10 мг/мл), 2 раза в сутки. Независимо от приема пищи
|
|||
|
Срок гестации >= 32 недель
Возраст > 4 недель
|
4 мг/кг
|
8 мг/кг
|
|
|
#Невирапин** (суспензия для перорального применения, 10 мг/мл), 2 раза в сутки. Независимо от приема пищи
|
|||
|
Срок гестации >= 37 недель
|
|||
|
Возраст 2 - 4 недели
|
6 мг/кг
|
12 мг/кг
|
|
|
Возраст > 4 недель
|
200 мг/м2 ПТ
|
400 мг/м2 ПТ
|
|
|
Срок гестации >= 34 недель < 37 недель
|
|||
|
Возраст 2 - 4 недели
|
6 мг/кг
|
12 мг/кг
|
|
|
Возраст > 4 недель
|
200 мг/м2 ПТ
|
400 мг/м2 ПТ
|
|
|
Лопинавир+ритонавир** (Раствор для приема внутрь 80/20 мг/1 мл, 2 раза в сутки
|
|||
|
Срок гестации >= 42 недель
Возраст > 14 дней
|
300 мг/75 мг на м2
(~ 16/4 мг/кг)
|
600 мг/150 мг на м2
(~ 32/8 мг/кг)
|
|
Вскармливание детей ВИЧ-инфицированных матерей
- НЕ рекомендуется прикладывать к груди и кормить материнским молоком детей, рожденных ВИЧ-инфицированными женщинами с целью профилактики заражения ребенка [274 - 276] (B3).
Комментарий: Прикладывание ребенка к груди или вскармливание молоком ВИЧ-инфицированной женщины увеличивает риск его заражения ВИЧ. Дополнительными факторами риска при грудном вскармливании служат трещины сосков, абсцесс молочной железы у матери, стоматит у ребенка. Для предотвращения заражения детей, рожденных ВИЧ-инфицированными женщинами, после рождения необходимо переводить на исключительно искусственное вскармливание. По согласованию с женщиной проводятся мероприятия по прекращению лактации.
- Рекомендуется врачам, ответственным за наблюдение детей, с целью профилактики заражения ребенка:
о пролонгировать профилактический курс АРВП до 6 недель у ребенка, получающего грудное вскармливание (УДД 2 УУР B) [268, 273, 281, 366, 367];
о назначить #невирапин** ребенку, получающему грудное вскармливание, на весь период грудного вскармливания плюс 7 дней после его полного прекращения, если мать не получает АРТ [268, 273, 281, 366, 367] (B2), см. таблицу 9.
Таблица 9. Профилактическая доза #невирапина** у ребенка, получающего грудное вскармливание [281]
|
Возраст
|
Суточная доза
|
|
С 6 недель до 6 месяцев
|
20 мг 1 раз в сутки
|
|
С 6 месяцев до 9 месяцев
|
30 мг 1 раз в сутки
|
|
С 9 месяцев до окончания грудного вскармливания
|
40 мг 1 раз в сутки
|
5.2. Профилактика пневмоцистной пневмонии и других оппортунистических инфекций
Первичная и вторичная профилактика вторичных инфекций различаются сроками проведения и объемом мероприятий (см. таблицу 15. Профилактика первого эпизода оппортунистических инфекций у ВИЧ-инфицированных детей, таблицу 16. Профилактика рецидива оппортунистических инфекций у ВИЧ-инфицированных детей в разделе 7. Дополнительная информация).
- Рекомендуется врачам, ответственным за наблюдение детей [101, 230, 277 - 279, 281, 294] (C5):
о всем детям, рожденным ВИЧ-инфицированными матерями с возраста 6 недель и до исключения инфицирования ВИЧ назначать ко-тримоксазол (Сульфаметоксазол + Триметоприм)** в профилактической дозировке с целью предотвращения заболеваний, связанных с простейшими (пневмоцисты и токсоплазмы) и бактериями (неспецифические респираторные и кишечные возбудители);
о у детей с подтвержденной ВИЧ-инфекцией применять профилактический прием ко-тримоксазола (Сульфаметоксазол + Триметоприм)** с 6 недель до 12 месяцев, в дальнейшем - при снижении CD4 до показателей, соответствующих тяжелому иммунодефициту (продолжать до повышения CD4 соответственно до 2й или 1й иммунной категории).
Комментарий: Универсальным методом профилактики и улучшения прогноза при лечении вторичных заболеваний и оппортунистических инфекций является своевременное назначение АРТ. Различают первичную профилактику вторичных инфекций - назначается для предотвращения первого эпизода инфекции, и вторичную профилактику - назначается после купирования острого состояния, связанного с вторичным заболеванием, с целью предотвращения повторного эпизода. Показанием к назначению профилактики вторичных инфекций служит снижение CD4-лимфоцитов, соответствующее критерию тяжелого иммунодефицита в зависимости от возраста ребенка. Следует учитывать, что у детей первого года жизни частота развития оппортунистических инфекций (в частности, пневмоцистной пневмонии), не коррелирует с показателями CD4.
5.3. Постконтактная профилактика ВИЧ-инфекции: выбор АРВП у детей
Под постконтактной профилактикой у детей понимается комплекс мероприятий, назначаемых для предотвращения заражения ВИЧ-инфекцией, в данном контексте при контактах, не связанных с возможностью передачи ВИЧ-инфекции от матери плоду и ребенку [280]. Постконтактная профилактика является надежным методом снижения риска заражения при соблюдении высокой приверженности приему препаратов.
При проведении постконтактной профилактики руководствоваться Санитарными правилами и нормами СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", утвержденными 28 января 2021 года [1].
- Рекомендуется врачам, ответственным за наблюдение детей, в качестве постконтактной профилактики:
о назначить ребенку антиретровирусные препараты в течение первых двух часов после контакта и не позднее 72 часов [1, 281, 282, 320, 372 - 376] (C5);
о провести 28-дневный курс АРТ схемой, состоящей из трех АРВП [1, 281, 282, 372 - 376] (B2);
о детям 12 лет и старше назначить: в качестве предпочтительной основы схемы - #TDF** + #3TC** или TDF+FTC [281, 282, 372, 373, 375, 376] (B2); в качестве предпочтительного третьего препарата - #LPV+#/r** [281, 282, 372, 373, 375, 376] (B2) или #DTG** [281] (C5), в качестве альтернативного третьего препарата - #DRV** + #/r** или #ATV** + #/r** или #RAL** [281, 282, 372, 373, 375, 376] (B2) при условии доступности и отсутствии возрастных ограничений;
о детям в возрасте младше 12 лет назначить предпочтительную схему АРТ #ZDV** + #3TC** + #LPV+r** [281, 372 - 374, 376] (B3) или #ZDV** + #3TC** + #DTG** [281] (C5); в качестве альтернативного третьего препарата - #NVP [373, 374] (B3) или #ATV** + #/r** [282] (B2) или #DRV** + #/r** [282] (B2) или #RAL** [281, 372 - 376] (C5) в зависимости от возраста ребенка (см. табл. 3).
Комментарий: При наличии показаний ПКП должна быть начата насколько возможно раньше после состоявшегося контакта. При назначении ПКП ВИЧ-инфекции пациент информируется о препаратах, производится оценка сопутствующей патологии и возможных межлекарственных взаимодействий. При появлении дополнительной информации схема корректируется. При назначении ПКП ВИЧ-инфекции проводится работа по повышению приверженности лечению и наблюдению.
Применение абакавира** ограничено необходимостью проведения исследования выявление аллели 5701 локуса B главного комплекса гистосовместимости человека (HLA B*5701).
5.4. Диспансерное наблюдение
Диспансерному наблюдению подлежат дети с риском заражения ВИЧ-инфекцией, а также дети с подтвержденным диагнозом ВИЧ-инфекция.
Организация ДН осуществляется в соответствии с группой учета.
I группа ДУ
Контингенты:
Диспансерному наблюдению в I группе подлежат дети, серопозитивные в ИФА, ИХЛА, но с отрицательным или неопределенным ИБ, исключая детей с перинатальным контактом, рожденных ВИЧ-серопозитивными матерями, и детей, у матерей которых выявлена ВИЧ-инфекция.
Подробную информацию см. в СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", раздел VI "Профилактика ВИЧ-инфекции" [1].
II группа ДУ
Контингенты:
Диспансерному наблюдению во II группе подлежат дети с контактом по ВИЧ-инфекции, при котором имелся риск заражения ВИЧ-инфекцией, исключая детей с перинатальным контактом, рожденных ВИЧ-серопозитивными матерями, и детей, у матерей которых выявлена ВИЧ-инфекция.
Выбор АРВП для проведения ПКП - см. выше. Подробную информацию см. в СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", раздел VI "Профилактика ВИЧ-инфекции" [1].
III группа ДУ
Контингенты:
Диспансерному наблюдению в III группе подлежат дети с подтвержденным диагнозом ВИЧ-инфекция.
Целью диспансерного наблюдения ВИЧ-инфицированных детей является увеличение продолжительности и сохранение качества их жизни. Основные задачи - формирование приверженности диспансерному наблюдению и антиретровирусной терапии, своевременное выявление у больных показаний к назначению химиопрофилактики и лечению вторичных заболеваний, обеспечение оказания им своевременной медицинской помощи, в том числе психологической поддержки и лечения сопутствующих заболеваний.
После установления ребенку диагноза ВИЧ-инфекции специалистами территориальных центров по профилактике и борьбе со СПИДом заполняется учетная форма N 311/у "Донесение о подтверждении диагноза у ребенка, рожденного ВИЧ-инфицированной матерью". Ответственность за достоверность заполнения несут главные врачи территориальных центров по профилактике и борьбе со СПИДом. В течение 10 дней учетная форма N 311/у направляется в адрес ФКУ "РКИБ" Минздрава России. В дальнейшем форма направляется каждые 6 месяцев [6].
Место наблюдения: Центр СПИД или его филиал.
Специалист, осуществляющий ДН: врач-педиатр Центра СПИД/или филиала, при его отсутствии - врач-инфекционист Центра СПИД/или филиала.
Длительность ДН: пожизненно.
Объем ДН:
Диспансерное наблюдение детей с ВИЧ-инфекцией включает:
- клинико-лабораторное обследование при взятии под наблюдение и в декретированные сроки для оценки течения ВИЧ-инфекции;
- назначение и проведение АРТ;
- исследование эффективности и безопасности АРТ;
- выявление, лечение и профилактика вторичных и сопутствующих заболеваний;
- мероприятия по повышению приверженности ДН и АРТ.
Клинико-лабораторное и инструментальное обследование изложено в разделе 2. Диагностика заболевания или состояния, медицинские показания и противопоказания к применению методов диагностики и Приложении Б. Алгоритмы действий врача.
Исследование эффективности и безопасности АРТ изложено в разделах 2. Диагностика заболевания или состояния, медицинские показания и противопоказания к применению методов диагностики и 7. Дополнительная информация.
Проведение АРТ изложено в разделах: 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения; 7. Дополнительная информация, Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата; Приложение Б. Алгоритмы действий врача.
Профилактика пневмоцистной пневмонии изложена в п. 5.2 данного раздела.
Мероприятия по повышению приверженности ДН и АРТ и их оценке изложены в разделах: 2. Диагностика заболевания или состояния, медицинские показания и противопоказания к применению методов диагностики; 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения, 7. Дополнительная информация; Приложениях Г1 - Г4. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях.
Плановые осмотры пациента врачом, ответственным за наблюдение ВИЧ-инфицированного ребенка, в рамках диспансерного наблюдения ВИЧ-инфицированных детей осуществляются:
- при отсутствии АРТ: не реже 1 раза в 3 месяца;
- на фоне АРТ: через 2 и 4 - 8 недель после начала АРТ, затем каждые 3 месяца;
- на фоне АРТ в фазе ремиссии при достижении клинического, вирусологического и иммунологического эффектов в течение 2-х и более лет: не реже 1 раза в 6 месяцев (см. таблицу 23 и таблицу 24) [1, 10, 19, 101, 202, 203].
Решение о начале проведения АРТ принимается:
- врачебной комиссией по назначению АРТ территориального центра СПИД;
- с учетом возраста ребенка, результатов клинико-лабораторного и инструментального исследования и консультирования родителей/лиц, осуществляющих уход за ребенком (см разделы: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики; 3. Лечение, 7. Дополнительная информация);
- при письменном согласии ребенка или его родителей (см. разделы: 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения; Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата).
IV группа ДУ
Контингенты:
Диспансерному наблюдению в IV группе подлежат дети, рожденные ВИЧ-инфицированными матерями, серопозитивными во время беременности и родов.
После рождения ребенка у ВИЧ-серопозитивной матери в течение 10 дней в адрес территориального Центра СПИД направляется учетная форма N 309/у "Извещение о новорожденном, рожденном ВИЧ-инфицированной матерью", заполненная врачами акушерами-гинекологами в учреждениях родовспоможения. Территориальный центр по профилактике и борьбе со СПИДом в течение 3 дней направляет учетную форму N 309/у в адрес ФКУ "РКИБ" Минздрава России [6].
При получении документированного подтверждения отсутствия ВИЧ-инфекции в течение 10 дней после снятия диагноза в адрес ФКУ "РКИБ" Минздрава России направляется учетная форма N 310/у "Донесение о снятии с диспансерного наблюдения ребенка, рожденного ВИЧ-инфицированной матерью", заполненная специалистами территориальных центров по профилактике и борьбе со СПИДом. Данная форма также заполняется при убытии ребенка из региона или в случае его смерти (в пункте 13 указывается причина смерти ребенка).
Ответственность за достоверность заполнения несут главные врачи территориальных центров по профилактике и борьбе со СПИДом [6].
При получении документированного подтверждения наличия ВИЧ-инфекции - см. III группа ДУ. Диспансерное наблюдение детей с подтвержденным диагнозом ВИЧ-инфекция.
Место наблюдения: поликлиника по месту жительства совместно с Центром СПИД или его филиалом.
Специалист, осуществляющий ДН: врач-педиатр участковый совместно с врачом-педиатром Центра СПИД/или филиала, при его отсутствии - врачом-инфекционистом Центра СПИД/или филиала.
Длительность ДН: до исключения диагноза ВИЧ-инфекция, но не менее 6 месяцев, либо до подтверждения диагноза ВИЧ-инфекция с последующим переводом в III группу ДН для пожизненного наблюдения.
Объем ДН:
Диспансерное наблюдение детей, рожденных ВИЧ-инфицированными матерями, серопозитивными во время беременности и родов, включает:
- проведение профилактики перинатальной передачи ВИЧ у ребенка;
- клинико-лабораторное обследование в декретированные сроки, направленное на раннее выявление ВИЧ-инфекции и раннее начало АРТ либо на исключение ВИЧ-инфекции;
- профилактика пневмоцистной пневмонии у детей младше 12 месяцев;
- снятие с ДН детей с документированным отсутствием ВИЧ-инфекции либо перевод в группу III ДУ при документированном подтверждении ВИЧ-инфекции.
Проведение профилактики перинатальной передачи ВИЧ у ребенка изложено в п. 5.1. Профилактика передачи ВИЧ-инфекции от матери ребенку.
Клинико-лабораторное обследование изложено в разделах: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики и Приложение Б. Алгоритмы действий врача.
Профилактика пневмоцистной пневмонии изложена в п. 5.2 данного раздела.
При диспансерном наблюдении детей, рожденных ВИЧ-инфицированными матерями, серопозитивными во время беременности и родов, осуществляется:
- осмотр и физикальное обследование: проводится в течение 5 рабочих дней после выписки из учреждения родовспоможения, затем каждые 10 дней при перерасчете доз АРВП, затем при каждом визите с целью проведения обследования на ВИЧ-инфекцию;
- консультирование по вопросам приверженности ДН и АРТ: проводится при каждом контакте с матерью/лицом, осуществляющим уход за ребенком;
- консультирование по вопросам вскармливания: проводится в учреждении родовспоможения, в дальнейшем (при продолжающемся грудном вскармливании) - при каждом контакте с матерью, при необходимости с привлечением медицинских психологов и равных консультантов.
Решение о документированном отсутствии ВИЧ-инфекции принимается:
- врачебной комиссией по снятию с диспансерного наблюдения территориального центра СПИД;
- с учетом возраста ребенка, результатов клинико-лабораторного исследования и способа вскармливания.
Снятие с ДН:
1) Дети ВИЧ-инфицированных серопозитивных матерей, обследованные молекулярными методами в декретированные сроки, получавшие с рождения исключительно искусственное вскармливание
Снятие ребенка с ДУ осуществляется решением врачебной комиссии по совокупности данных, подтверждающих отсутствие ВИЧ-инфекции и отсутствие риска ВИЧ-инфекции [1, 10, 19, 101, 202, 203]:
- возраст ребенка старше 6 месяцев;
- плюс получены минимум 2 отрицательных результата обследования на НК ВИЧ при молекулярно-биологическом исследовании крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в декретированные сроки (первый результат получен в возрасте не ранее 6 недель, второй - не ранее 4х месяцев);
- плюс получены два и больше отрицательных результата исследований на АТ/АГ ВИЧ методом ИФА/ИХЛА (исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2, антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови) с интервалом не менее 1 месяца, выполненных в возрасте старше 6 месяцев (при этом отсутствует выраженная гипогаммаглобулинемия на момент исследования крови на антитела к ВИЧ);
- плюс отсутствуют клинические проявления, которые могут быть расценены как проявления ВИЧ-инфекции;
- плюс ребенок не прикладывался к груди ВИЧ-инфицированной женщины и исключен риск артифициальной трансмиссии.
2) Дети ВИЧ-инфицированных серопозитивных матерей, не обследованные молекулярными методами, получавшие с рождения исключительно искусственное вскармливание
Снятие ребенка с ДУ осуществляется решением врачебной комиссии по совокупности данных, подтверждающих отсутствие ВИЧ-инфекции и отсутствие риска ВИЧ-инфекции [1, 10, 19, 101, 202, 203]:
- возраст ребенка старше 18 месяцев;
- плюс получены два или больше отрицательных результата обследований на АТ/АГ ВИЧ методом ИФА/ИХЛА (исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2, антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови) с интервалом не менее 1 месяца, выполненных в возрасте старше 18 месяцев (при этом отсутствует выраженная гипогаммаглобулинемия на момент исследования крови на антитела к ВИЧ);
- плюс отсутствуют клинические проявления, которые могут быть расценены как проявления ВИЧ-инфекции;
- плюс ребенок не прикладывался к груди ВИЧ-инфицированной женщины и исключен риск артифициальной трансмиссии.
3) Дети ВИЧ-инфицированных серопозитивных матерей, получавшие грудное вскармливание
Снятие ребенка с ДУ осуществляется решением врачебной комиссии по совокупности данных, подтверждающих отсутствие ВИЧ-инфекции и отсутствие риска ВИЧ-инфекции [1, 10, 19, 101, 202, 203]:
- ребенок не прикладывался к груди и не получал грудное молоко ВИЧ-инфицированной женщины в течение последних 9 месяцев;
- плюс у ребенка в возрасте младше 18 месяцев получены отрицательные результаты при молекулярно-биологическом исследовании крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) через 4 - 6 недель, 3 месяца, 6 месяцев после прекращения грудного вскармливания и получены как минимум 2 отрицательных результата обследования на АТ/АГ ВИЧ (исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2, антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови) (с интервалом не менее 1 месяца и при отсутствии выраженной гипогаммаглобулинемии), проведенные минимум через 6 месяцев после полного прекращения грудного вскармливания
или
- у ребенка в возрасте старше 18 месяцев получены отрицательные результаты обследования на АТ/АГ ВИЧ методом ИФА/ИХЛА (исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2, антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови) через 4 - 6 недель, 3 месяца, 6 месяцев после прекращения грудного вскармливания (при этом отсутствует выраженная гипогаммаглобулинемия на момент исследования крови на антитела к ВИЧ);
- плюс отсутствуют клинические проявления, которые могут быть расценены как проявления ВИЧ-инфекции;
- плюс исключен риск артифициальной трансмиссии.
Протокол заседания врачебной комиссии по снятию ребенка с перинатальным контактом по ВИЧ-инфекции с диспансерного учета должен содержать: паспортные данные матери и данные ребенка (фамилия, имя, отчество, дата рождения, место жительства, эпидемиологический номер); данные о характере проведенной ППМР; описание вида вскармливания; данные об отсутствии клинических проявлений и лабораторных отклонений, которые могут быть расценены как проявления ВИЧ-инфекции; результаты обследования на НК ВИЧ (не менее двух); результаты обследования на антитела к ВИЧ (не менее двух); результаты обследований, подтверждающих отсутствие гипогаммаглобулинемии; примечания и рекомендации; решение.
V группа ДУ
Контингенты:
Диспансерному наблюдению в V группе подлежат дети любого возраста, у матерей которых выявлена ВИЧ-инфекция.
Как правило, такая ситуация возможна при заражении матери ВИЧ-инфекцией на поздних сроках беременности или во время грудного вскармливания, что сопряжено с высоким риском инфицирования плода или ребенка.
Место наблюдения: поликлиника по месту жительства совместно с Центром СПИД или его филиалом.
Специалист, осуществляющий ДН: врач-педиатр участковый совместно с врачом-педиатром Центра СПИД/или филиала, при его отсутствии - врачом-инфекционистом Центра СПИД/или филиала.
Длительность ДН: до момента документированного исключения ВИЧ-инфекции с последующим снятием с ДУ или документированного подтверждения диагноза ВИЧ-инфекция с последующим переводом в группу III ДУ.
Объем ДН:
Диспансерное наблюдение детей, у матерей которых выявлена ВИЧ-инфекция, включает:
- если ребенок получает грудное вскармливание - немедленное его прекращение и незамедлительное назначение 6-недельного курса превентивной терапии с применением 3х АРВП (ребенок относится к группе высокого риска заражения ВИЧ-инфекцией), выбор препаратов осуществляется в соответствии с возрастом ребенка, см. п. 5.3. Постконтактная профилактика ВИЧ-инфекции: выбор АРВП у детей и раздел 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения;
- клинико-лабораторное обследование, направленное на выявление ВИЧ-инфекции и начало АРТ, либо на исключение ВИЧ-инфекции;
- профилактика пневмоцистной пневмонии у детей младше 12 месяцев;
- снятие с ДУ детей с документированным отсутствием ВИЧ-инфекции либо перевод в группу III ДУ при документированном подтверждении ВИЧ-инфекции.
Клинико-лабораторное обследование изложено в разделах: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики и Приложение Б. Алгоритмы действий врача.
Профилактика пневмоцистной пневмонии изложена в п. 5.2 данного раздела.
Обследование на ВИЧ-инфекцию:
- если ребенок младше 18 месяцев, то исследования на ВИЧ-инфекцию назначаются как и у детей серопозитивных матерей - с использованием молекулярных методов диагностики (молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1)) и с учетом грудного вскармливания;
- если ребенок старше 18 месяцев и с момента последнего получения материнского грудного молока прошло более 6 месяцев, то обследование на антитела к ВИЧ стандартными методами ИФА/ИХЛА (исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2, антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови) проводится однократно (и если ребенок младше 3х лет, рекомендуется провести обследование на антитела к ВИЧ в возрасте 3 года).
Решение о документированном отсутствии ВИЧ-инфекции принимается:
- врачебной комиссией по снятию с диспансерного наблюдения территориального центра СПИД;
- с учетом возраста, результатов клинико-лабораторного исследования и вида вскармливания ребенка.
Порядок снятия с ДН - см. соответствующую ситуацию в разделе IV группа ДУ. Диспансерное наблюдение детей с перинатальным контактом, рожденных ВИЧ-инфицированными серопозитивными матерями.
6. Организация оказания медицинской помощи
Первичная специализированная медико-санитарная помощь детям оказывается врачами-инфекционистами и/или врачами педиатрами центра СПИД на основе взаимодействия с врачами-педиатрами первичного звена здравоохранения.
Специализированная медицинская помощь при ВИЧ-инфекции в стационарных условиях детям с ВИЧ-инфекцией и детям, рожденным от ВИЧ-инфицированных матерей, оказывается в стационаре акушерско-гинекологического, педиатрического профилей, а также в стационаре медицинской организации, оказывающей специализированную медицинскую помощь по профилю "инфекционные болезни" на выделенных для этих целей койках.
Показаниями к оказанию специализированной медицинской помощи по профилю "инфекционные болезни" (госпитализации пациента) при ВИЧ-инфекции являются:
- необходимость диагностики и лечения вторичных заболеваний, в случае невозможности лечения в амбулаторных условиях, в том числе требующих изоляции больного (за исключением туберкулеза, гематологических и онкологических заболеваний) - стадии 2В, 4Б, 4В (фаза прогрессирования), 5;
- назначение или коррекция схемы АРТ при тяжелой иммуносупрессии с высоким риском развития тяжелого "воспалительного синдрома восстановления иммунной системы");
- необходимость проведения исследований, которые не могут быть осуществлены в амбулаторных условиях, в том числе инструментальных (инвазивных, лучевых) при установлении стадии ВИЧ-инфекции;
- проведение дифференциальной диагностики вторичных и соматических заболеваний, организация медико-социальной экспертизы;
- состояния, требующие медицинской помощи в связи с развитием тяжелых нежелательных явлений на фоне приема АРТ;
- необходимость контроля и повышения приверженности наблюдению и лечению, с проведением комплексной оценки и коррекции поражений ЦНС и психосоциальной сферы, в том числе нейровизуальных диагностических исследований, клинико-психологического нейропсихологического и социального обследования; разработки и осуществления комплексных реабилитационных мероприятий, направленных на психокоррекцию когнитивных параметров, поведенческих нарушений, социализацию детей и подростков;
- наличие иных, в том числе социальных показаний (дети, оставшиеся без попечения родителей до оформления в дом ребенка, беременные женщины с целью обеспечения приверженности трехэтапной профилактике и др.).
Детям с ВИЧ-инфекцией специализированная медицинская помощь, связанная с манифестацией ВИЧ-инфекции (при вторичных заболеваниях), оказывается в стационарных условиях врачами-инфекционистами во взаимодействии с врачами-педиатрами на основе клинических рекомендаций (протоколов лечения), а также с учетом стандартов и порядков медицинской помощи.
Показаниями к выписке пациента являются выполнение задач, поставленных при госпитализации, либо обоснованное решение о нецелесообразности дальнейшего пребывания в условиях стационара:
1. достижение ремиссии или стабилизации течения ВИЧ-инфекции;
2. завершение дифференциальной диагностики и определение тактики лечения либо излечение вторичного/сопутствующего заболевания;
3. купирование нежелательных явлений, связанных с АРТ;
4. выполнение курса мероприятий, направленных на психокоррекцию когнитивных и поведенческих нарушений и социализацию с формированием рекомендаций по дальнейшей маршрутизации пациента;
5. завершение проведения запланированной медико-социальной экспертизы;
6. решение о нецелесообразности дальнейшего пребывания в стационарных условиях, принятое врачебной комиссией.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
7.1. Особенности АРТ у детей
Выделяют две цели АРТ у детей: первая - увеличение продолжительности жизни и улучшение ее качества путем создания условий для формирования, сохранения и восстановления иммунной системы и предотвращения клинического прогрессирования заболевания, вторая - профилактика передачи ВИЧ-инфекции в популяции.
Снижение СПИД-связанной летальности. До настоящего времени ВИЧ-инфекция остается неизлечимым заболеванием и добиться элиминации вируса не удается. Единственным специфическим методом лечения ВИЧ-инфекции на сегодняшний день является пожизненное применение АРТ. Антиретровирусные препараты блокируют размножение ВИЧ, что проявляется снижением содержания вируса в крови вплоть до неопределяемого уровня. Это приводит к восстановлению субпопуляции CD4-лимфоцитов и/или предотвращению развития иммунодефицита и, как следствие, к предотвращению появления или облегчению течения вторичных заболеваний. В результате улучшается качество и увеличивается продолжительность жизни пациента. АРТ проводится пожизненно, без плановых перерывов или прекращения приема препарата.
Снижение заболеваемости. Не менее важной задачей АРТ является предотвращение распространения ВИЧ-инфекции горизонтальным путем, а также вертикальным - от матери ребенку.
АРТ состоит из комбинации антиретровирусных препаратов, нарушающих жизненный цикл вируса. ВИЧ обладает высокой репликативной активностью и изменчивостью, т.е. способностью варьировать свою РНК и таким образом вырабатывать жизнеспособные мутации в присутствии АРВП. Эффективным способом длительного подавления размножения ВИЧ и преодоления формирования резистентности к АРВП является назначение комбинированных схем АРТ, формирование у пациента высокой приверженности лечению без пропусков и нарушения режима приема доз препаратов, отслеживание нежелательных эффектов терапии, которые могут привести к отказу пациента от терапии.
В настоящее время для лечения ВИЧ-инфекции у детей в России используются следующие классы АРВП:
- нуклеозиды и нуклеотиды - ингибиторы обратной транскриптазы. Действуют на ранней стадии репликации вируса, препятствуют синтезу вирусной ДНК: абакавир**, зидовудин**, ламивудин**, эмтрицитабин**, тенофовир дизопроксил фумарат**, тенофовир алафенамид (в составе препарата с фиксированными комбинациями доз), фосфазид**;
- ненуклеозидные ингибиторы обратной транскриптазы: невирапин**, эфавиренз**, этравирин**, рилпивирин (** в составе препарата с фиксированными комбинациями доз);
- ингибиторы интегразы ВИЧ. Препятствуют встраиванию ДНК ВИЧ в генетический материал клетки: ралтегравир**, долутегравир**, элвитегравир** (в составе препарата с фиксированными комбинациями доз), биктегравир** (в составе препарата с фиксированными комбинациями доз);
- ингибиторы протеаз. Действуют на поздней стадии репликации вируса, препятствуют созреванию вирусной мРНК: атазанавир**, дарунавир**, лопинавир**, ритонавир**, фосампренавир**.
Правила расчета доз и выработка режима приема АРВП у детей
АРВП назначаются детям строго в терапевтической дозе, соответствующей возрасту, либо производится расчет разовой и суточной дозы для каждого препарата по массе тела (мг/кг) или поверхности тела ребенка (мг/м2). Важно придерживаться стандартного метода расчета доз, чтобы сделать удобной возможную коррекцию.
Для детей расчет дозы препарата на квадратный метр поверхности тела является более точным и проводится с использованием номограмм для вычисления поверхности тела по массе и росту по формуле Мостеллера:
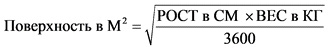
Дозы АРВП следует корректировать (не превышая допустимых терапевтических) при изменении массы тела на 10% и более, в противном случае фармакокинетика препаратов со временем станет недостаточно эффективной, что может привести к возникновению резистентных штаммов ВИЧ.
Необходимо четко установить часы, в которые будут даваться лекарства (отдельно для каждого препарата): при 1-кратном приеме препарат дается каждые 24 часа, при 2-кратном - каждые 12 часов.
При подозрении на возможные нарушения режима приема препаратов или при выявлении недостаточной приверженности АРТ следует отдавать предпочтение простым схемам с небольшими количествами лекарственных препаратов, их высоким барьером резистентности и минимально возможными побочными действиями.
Несвоевременный прием препарата или пропуск приема препарата являются недопустимыми. Подбор препаратов с одинаковыми часами приема способствует повышению приверженности лечению.
При назначении АРВП детям необходимо учитывать особенности дачи препаратов в связи с приемами пищи (так, ИП необходимо давать ребенку во время еды). Некоторые АРВП нельзя давать вместе; некоторые - нельзя принимать вместе с антацидами, противотуберкулезными препаратами. Большинство АРВП нельзя запивать соком грейпфрута. Перед назначением АРВП необходимо тщательно изучить инструкции и рекомендации по их применению.
Повторный прием АРВП допускается при рвоте, которая является частым побочным действием большинства АРВП у детей (особенно раннего возраста) в первые дни (иногда недели) лечения. Это побочное действие не должно явиться причиной немедленной отмены лечения. Как показывает практика, со временем дети хорошо адаптируются к приему АРВП даже с неприятными вкусовыми качествами. Если рвота возникает менее, чем через 30 минут после приема препарата, необходимо повторно дать полную разовую дозу.
В первые дни лечения следует давать АРВП (с возможным одновременным приемом) с интервалом примерно 30 минут, затем, по мере привыкания ребенка, сокращать интервал между приемом разных препаратов до нескольких минут. Нельзя смешивать в одной емкости разные жидкие и порошковые формы АРВП!
Ведение дневника, особенно в первые месяцы лечения, в котором сам ребенок или его родители, или лица, осуществляющие уход, фиксируют все принятые дозы АРВП и отмечают все побочные эффекты терапии, существенно помогает лечащему врачу оценить безопасность и эффективность терапии и при необходимости провести своевременную коррекцию.
Преимущества и недостатки АРВП разных классов
Таблица 10. Преимущества и недостатки различных АРВП
|
АРВП
|
Преимущества
|
Недостатки
|
|
Классы АРВП
|
||
|
Ингибиторы интегразы (J05AJ)
|
- Мало лекарственных взаимодействий
- Хорошая переносимость
|
- Ограниченные данные по дозированию и безопасности у детей
|
|
Ненуклеозидные ингибиторы обратной транскриптазы
(J05AF)
|
- Длинный период полувыведения
- Более низкий риск дислипидемии и липодистрофии, чем у ИП
- Более низкая лекарственная нагрузка, легче применять чем ИП
|
- 1 мутация может приводить к резистентности, в т.ч. перекрестной (EFV** и NVP**)
- Редкие, но тяжелые и жизнеугрожаемые случаи лекарственной сыпи и гепатотоксичности
- Возможность множественных лекарственных взаимодействий (метаболизм печеночными ферментами)
|
|
Ингибиторы протеаз (J05AE)
|
- Доказанная эффективность
- Высокий барьер резистентности
- В сочетании с 2мя НИОТ - воздействие на 2 фазы репликации ВИЧ
|
- Метаболические нарушения
- Возможность множественных лекарственных взаимодействий (метаболизм печеночными ферментами)
- Высокая лекарственная нагрузка
- Низкие вкусовые качества жидких форм
- Требуется бустирование
|
|
Комбинации НИОТ
|
||
|
ABC**+3TC**
ABC**+FTC**
|
- Хороший вкус растворов
- Можно давать с пищей
- ФКД
|
- Риск РГЧ к ABC**, необходимость скрининга
|
|
FTC**+TAF**
|
- 1 РС
- Маленькая таблетка
- Низкий риск почечной и костной токсичности
- ФКД
|
- Ограниченные данные по эффективности и безопасности у детей
- Повышение уровня липидов
|
|
TDF**+3TC**
TDF**+FTC**
|
- Медленное развитие резистентности
- Низкий риск митохондриальной токсичности
- Можно давать с пищей
- ФКД
|
- Ограниченный опыт использования у детей
- Потенциальная почечная и костная токсичность
- Множественные лекарственные взаимодействия с другими АРВП (LPV+r**, ATV**, RTV**)
|
|
ZDV**+3TC**
ZDV**+FTC**
|
- Большой опыт применения у детей
- Хороший вкус растворов
- Можно давать с пищей
|
- Костномозговая токсичность (ZDV**)
- Липоатрофия (ZDV**)
|
|
ZDV**+ABC**
|
- Хороший вкус растворов
- Можно давать с пищей
|
- Риск РГЧ к ABC**, необходимость скрининга
- Костномозговая токсичность и липоатрофия (ZDV**)
|
Неэффективность АРТ у детей
При оценке причин неэффективности АРТ у детей, в отличие от взрослых, необходимо учитывать следующие факторы: зависимость от взрослых; органолептические свойства АРВП; неустойчивую фармакокинетику; трудности в достижении высокой приверженности, особенно в подростковом возрасте. Выявленная неэффективность на фоне недостаточной приверженности АРТ не всегда сопровождается формированием резистентности: выработка высокой приверженности лечению может позволить сохранить текущую схему АРТ. Подтвержденная неэффективность проводимой терапии является причиной перехода на схему АРТ следующей линии.
Основные причины вирусологической неэффективности АРТ
1. Связанные с приверженностью АРТ:
- наличие состояний/заболеваний, снижающих способность соблюдать режим АРТ (ментальные расстройства, нейро-когнитивные нарушения, поражение слизистых желудочно-кишечного тракта, нарушение глотания и др.);
- психосоциальные факторы;
- недоступность АРВП (невозможность вовремя получить, отсутствие и др.);
- нежелательные реакции АРВП;
- нежелательные явления;
- большая лекарственная нагрузка или частота приемов.
2. Связанные с ВИЧ:
- заражение штаммом ВИЧ, резистентным к АРВП;
- предшествующая неудача АРТ;
- природная устойчивость штамма ВИЧ к АРВП;
- высокая ВН до начала АРТ и неадекватно подобранная схема АРТ.
3. Связанные с АРТ:
- суб-оптимальная фармакокинетика, часто отмечаемая у детей младшего возраста;
- недостаточная антиретровирусная активность схемы АРТ;
- низкий барьер резистентности АРВП;
- поэтапное добавление препаратов в схему АРТ;
- несоблюдение пищевых ограничений;
- несоблюдение временн'ых интервалов между приемами АРВП;
- межлекарственные взаимодействия;
- неправильно рассчитанные дозы.
Снижение риска нежелательных реакций на фоне АРТ у детей
Дифференциальная диагностика осложнений, возникающих у детей в процессе проведения АРТ, является сложной ввиду комплексного характера их развития (в частности, влияние самого вируса иммунодефицита человека, токсическое воздействие препаратов, врожденные аномалии и заболевания, отсутствие четких диагностических критериев, недостаток данных, накопленных при использовании у детей АРВП последних поколений). Тем не менее, можно выделить факторы, способствующие снижению риска развития побочных эффектов АРТ:
- выявление предрасполагающих факторов;
- выявление и оценка течения сопутствующих и вторичных ВИЧ-связанных заболеваний;
- тщательный подбор АРВП с учетом возраста ребенка и указанных выше параметров;
- назначение препаратов из категории предпочтительных;
- правильный подбор дозы и кратности приема препаратов;
- оценка возможных лекарственных взаимодействий;
- клинический и лабораторный мониторинг безопасности АРТ и сопутствующей терапии;
- клинико-иммунологический и вирусологический мониторинг эффективности проводимой АРТ.
Перед началом АРТ проводится консультирование родителей/лиц, осуществляющих уход за ребенком, и самих детей по вопросам возможных побочных эффектов терапии и возможности развития воспалительного синдрома восстановления иммунитета:
- объясняется, что в начале терапии все АРВП обычно оказывают преходящие побочные действия: тошноту, рвоту, диарею;
- разъясняются причины возможных побочных эффектов и основные меры борьбы: симптоматическая терапия, коррекция режима приема препаратов, психологическая поддержка;
- обсуждаются симптомы возможных тяжелых побочных реакций, угрожаемых жизни, и тактика в случае их появления у ребенка.
Тактика ведения ребенка при появлении признаков токсичности/непереносимости АРВП
- При возникновении угрожающих жизни побочных эффектов все препараты немедленно отменяют (одновременно). Настоятельно рекомендуется госпитализировать ребенка в отделение интенсивной терапии. После полного исчезновения симптомов АРТ может быть возобновлена; препарат, с которым связана реакция, необходимо заменить на препарат с другим профилем токсичности. При развитии реакции гиперчувствительности этот препарат никогда нельзя назначать в дальнейшем.
- При возникновении умеренных нежелательных реакций терапия может быть продолжена до установления причинно-следственных связей, после чего меняется препарат, вызвавший побочную реакцию.
- При возникновении легких нежелательных реакций назначается симптоматическое лечение, АРТ может быть продолжена.
- До принятия решения о смене препарата рекомендуется пересчитать дозу препарата, назначенную ребенку, и убедиться, что она лежит в терапевтическом диапазоне. Если невозможно установить, какой именно препарат вызывает выраженное побочное действие, следует поменять всю схему. При смене терапии рекомендуется избегать комбинаций препаратов, вызывающих сходные побочные реакции. В целях предотвращения побочных действий АРВП или при их появлении не следует снижать возрастную терапевтическую дозу.
7.2. Приверженность АРТ и наблюдению и оценка приверженности АРТ
Высокая эффективность АРТ обусловлена мощным антиретровирусным потенциалом современных препаратов, используемых для лечения ВИЧ-инфекции: схемы высокоактивной АРТ поддерживают ВН ниже определяемого уровня у 95% пациентов в течение 4х лет и более [283]. При снижении приверженности АРТ менее 95% частота формирования мутаций устойчивости к АРВП может достигать 50% [283]. Полный и устойчивый эффект АРТ возможен только при соблюдении высокого уровня приверженности лечению и наблюдению [284 - 287].
Приверженность - это "степень, в которой поведение пациента - прием лекарств, следование диете, изменение образа жизни - соответствует согласованным с пациентом рекомендациям медицинских работников" [288].
Понятие приверженности при ВИЧ-инфекции включает:
- приверженность АРТ - готовность и возможность пациента начать и осуществлять прием всех препаратов назначенной схемы АРТ в установленное время, с установленной частотой и выполнением всех необходимых требований приема АРВП, как предписано лечащим врачом;
- приверженность лечению - степень участия пациента в процессе собственного лечения;
- комплаентность - степень соответствия поведения пациента клиническим рекомендациям.
Наиболее низкий уровень приверженности наблюдению и АРТ выявлен у подростков, что требует особых подходов и усилий от персонала МО, оказывающих помощь ВИЧ-инфицированным детям, т.к. следствием низкой приверженности являются низкие темпы снижения заболеваемости у подростков и рост летальности [284 - 287]. Для подростков важное значение имеют факторы повседневной жизни, психо-социальные и медицинские [289].
Последствиями сниженной и, в особенности, низкой приверженности АРТ являются:
- недостаточные уровни АРВП, в присутствии которых происходит размножение вируса и формируются устойчивые к АРВП вирусные варианты;
- повышение частоты госпитализаций;
- снижение эффективности лечения;
- нарастание иммунодефицита, повышение вероятности прогрессирования ВИЧ-инфекции и наступления летального исхода;
- необходимость назначения второй и последующих линий АРТ, стоимость которых, как правило, существенно превышает стоимость схемы стартовой терапии;
- продолжающееся распространение ВИЧ в популяции.
Наиболее важной в жизни пациента является первая линия АРТ, которая при внимательном подборе препаратов и постоянной работе с пациентом над приверженностью может стать успешной на долгие годы. При выборе стартовой схемы АРТ у детей следует отдавать предпочтение препаратам с однократным приемом в сутки и хорошими вкусовыми качествами, комбинированным препаратам, препаратам с удобными для ребенка лекарственными формами, что способствует увеличению длительности приема этой схемы [290].
Факторы, влияющие на приверженность
Существует большое количество факторов, которые могут влиять на уровень приверженности АРТ как в сторону нарушения, так и в сторону ее повышения.
Повышение приверженности АРТ и удержание под наблюдением требуют выявления и понимания всех возможных препятствий, с которыми может столкнуться пациент, а также разработки методов и способов преодоления этих препятствий. При проведении АРТ у детей следует оценивать приверженность как со стороны самого ребенка, так и со стороны лиц, осуществляющих уход за ним.
Достоверный (p = 0.001) положительный эффект на приверженность АРТ оказывают следующие факторы:
- выраженный эффект - самоконтроль приверженности;
- умеренный эффект - доверие медицинскому работнику и понимание пациентом необходимости и выгодности АРТ, а также социальная поддержка;
- несущественный эффект - возраст и мужской пол.
Достоверный (p = 0.001) отрицательный эффект на приверженность АРТ оказывают следующие факторы:
- умеренный эффект - использование наркотиков, настороженное отношение пациента к АРТ, симптомы депрессии и стигма;
- маленький эффект - наличие ингибиторов протеазы в схеме АРТ, частота приема АРВП, финансовые ограничения пациента;
- несущественный эффект - лекарственная нагрузка и длительность заболевания.
Не оказывали достоверно значимого влияния на приверженность АРТ количество CD4 (p = 0,64) и длительность АРТ (p = 0,92) [291].
Таким образом, предикторами приверженности АРТ являются разнообразные факторы, лежащие в трех основных сферах: биомедицинской, социо-экономической и индивидуальной психологической.
Диагностика и методы оценки приверженности и факторов, влияющих на приверженность
Используемые на практике методы оценки приверженности лечению имеют свои преимущества и недостатки. Наиболее достоверным методом является оценка вирусной нагрузки, однако, таким образом зачастую выявляются последствия нарушенной приверженности, иногда уже поздно, когда сформировалась устойчивость к АРВП. В таблице 11 представлены особенности различных методов оценки приверженности АРТ [286].
Таблица 11. Особенности применения различных методов оценки приверженности лечению
|
Метод
|
Преимущества
|
Недостатки
|
Вектор потенциальной оценки
|
Сравнительная точность
|
|
Самоотчет пациента (анкета)
|
Простота, дешевизна
|
Субъективность; точность может быть снижена при нарушениях памяти, невозможности контролировать точное время приема и при указании ложных сведений
|
Переоценка
|
Значимая связь с ВН
|
|
Подсчет таблеток
|
Простота, объективность
|
Точность может быть нарушена при выбрасывании пациентом остатков таблеток перед подсчетом, невозможностью достоверно определить, кто принимал таблетки и в какое время
|
Переоценка
|
Умеренная связь с ВН и количеством CD4; внезапный подсчет таблеток более предиктивный в отношении ВН, чем самоотчет
|
|
Данные аптеки/фармацевта
|
Простота, дешевизна, объективность
|
Необходимо, чтобы пациент приносил все бутылки с препаратами; невозможность достоверно определить, кто принимал таблетки и в какое время
|
Переоценка
|
Связь с ВН, количеством CD4 и СПИД-связанной летальностью - от умеренной до высокой
|
|
Исследование ВН
|
Объективность
|
Дороговизна; технические трудности; инвазивность (трудновыполнимо в условиях ограниченных ресурсов)
|
Переоценка или недооценка
|
Может варьировать в зависимости от резистентности, предшествующей неудачи лечения, или нарушенной абсорбции лекарств
|
Частота нейрокогнитивных нарушений у ВИЧ-инфицированных детей составляет до 37% в стадии легких и умеренных проявлений ВИЧ-инфекции и до 60% в стадии выраженных клинических проявлений/СПИДа. Психологическое обследование проводится лечащим врачом, медицинским психологом, психотерапевтом и включает обязательную диагностику тревоги/депрессии, когнитивных расстройств и оценку уровня качества жизни либо у самого ребенка, либо у законного представителя ребенка (см. таблицу 12). После выполнения коррекционного курса, включающего оказание медицинской (в т.ч. психиатрической) помощи, психологическую коррекцию и социальную адаптацию, проводятся повторные измерения (см. разделы: 2.5. Иные диагностические исследования; Приложение Б. Алгоритмы действий врача; Приложения Г1 - Г4. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента).
При отсутствии тревоги и депрессии следует 1 раз в 6 месяцев проводить комплексное клинико-психологическое нейропсихологическое обследование, направленное на выявление нарушений таких познавательных функций как внимание, память, мышление, речь, у ВИЧ-инфицированных детей в возрасте 11 лет и старше, или у законных представителей детей в возрасте младше 11 лет.
Таблица 12. Возрастные особенности использования психологических тестов у детей
|
Вид обследования
|
< 8 лет
|
8 - 10 лет
|
11 - 14 лет
|
15 - 17 лет
|
|
Количественная оценка приверженности лечению
Опросник КОП-25
|
Не проводится
|
Проводится у ребенка
|
||
|
Количественная оценка приверженности лечению
Тест Мориски-Грин
|
Проводится у законного представителя ребенка
|
Проводится у ребенка
|
Не проводится
|
|
|
Госпитальная шкала оценки тревоги и депрессии
HADS
|
Проводится у ребенка
|
|||
|
Оценка уровня качества жизни с помощью теста PedsQL
|
Не проводится
|
Проводится у ребенка
|
||
|
Любое исследование
|
Проводится с согласия и в присутствии законного представителя ребенка
|
Проводится с согласия ребенка
|
||
Классификация ВИЧ-ассоциированных нейрокогнитивных расстройств (ВАНКР) (Критерии "Фраскати" 2007) [292, 293]
I. Асимптомные нейрокогнитивные расстройства (АНКР)
1. Приобретенное когнитивное нарушение величиной как минимум 1 SD (стандартное отклонение) ниже средне-демографического нормативного показателя по крайней мере в 2-х когнитивных областях (доменах):
- Внимание/рабочая память;
- Вербальность/язык;
- Абстракция/исполнение;
- Сложные перцептивные моторные навыки;
- Память, включая обучение и отдачу;
- Простые моторные навыки или сенсорные способности восприятия;
- Скорость обработки информации.
2. КР не влияют на повседневную активность
3. КР не отвечают критериям делирия или деменции
4. Не выявлено других причин
II. Легкие нейрокогнитивные расстройства (ЛНКР)
1. Приобретенное когнитивное нарушение величиной как минимум 1 SD (стандартное отклонение) ниже средне-демографического нормативного показателя по крайней мере в 2-х когнитивных областях (доменах):
- Внимание/рабочая память;
- Вербальность/язык;
- Абстракция/исполнение;
- Сложные перцептивные моторные навыки;
- Память, включая обучение и отдачу;
- Простые моторные навыки или сенсорные способности восприятия
- Скорость обработки информации.
2. КР реализуются в по крайней мере легком нарушении повседневной активности (как минимум 1 из следующего):
- Самоотчет о снижении ментальных возможностей, неполноценность в профессиональной деятельности, выполнении домашней работы, социализации
- Данные со стороны других людей о снижении у пациента ментальных возможностей, приводящем к неполноценности в профессиональной деятельности, выполнении домашней работы, социализации.
3. КР не отвечают критериям делирия или деменции
4. Не выявлено других причин
III. ВИЧ-ассоциированная деменция (ВАД)
1. Выраженное приобретенное КР с вовлечением как минимум 2-х доменов (обычно нарушения в нескольких доменах, особенно усвоение новой информации, замедление информационных процессов, нарушение внимания/концентрации). КР д.б. исследованы нейропсихологическими тестами и показывать >= 2 SD (стандартное отклонение) ниже средне-демографического нормативного показателя по крайней мере в 2-х когнитивных областях (доменах):
- Внимание/рабочая память;
- Вербальность/язык;
- Абстракция/исполнение;
- Сложные перцептивные моторные навыки;
- Память, включая обучение и отдачу;
- Простые моторные навыки или сенсорные способности восприятия
2. КР реализуются в значительном нарушении повседневной активности (работа, домашняя жизнь, социальная активность)
3. КР не отвечают критериям делирия или деменции
4. Не выявлено других причин
Методы повышения приверженности АРТ и наблюдению
ВИЧ-инфекция - это хроническое заболевание, требующее пожизненного лечения, в процессе которого практически неизбежно наступает усталость. Высокая приверженность лечению - это не результат, а процесс, требующий постоянной работы как со стороны пациента, так и со стороны лиц, оказывающих медицинскую помощь, психологическое сопровождение, а также другие виды помощи. В таблице 13 перечислены основные практические методы преодоления барьеров приверженности [294], в таблице 14 - стратегии, направленные на формирование, поддержание и коррекцию приверженности лечению [294].
Таблица 13. Практические методы преодоления барьеров приверженности АРТ
|
Барьеры
|
Методы с доказанной эффективностью в рандомизированных исследованиях
|
|
Забывчивость
|
СМС, напоминающие устройства
|
|
Путешествия
|
Органайзеры для таблеток
|
|
Токсичность
|
Схемы АРТ с низкой токсичностью
|
|
Расстояние до клиники
|
Децентрализация, снижение частоты визитов
|
|
Депрессия
|
Психологический скрининг и коррекция
|
|
Аддикции
|
Консультирование
|
|
Вкус
|
Коррекция вкусовых качеств детских форм
|
|
Лекарственная нагрузка
|
Фиксированные комбинации доз, режимы в 1 таблетке
|
Методы повышения приверженности лекарственной терапии, медицинскому сопровождению и модификации образа жизни в зависимости уровня исследованной приверженности - см. раздел XIX. Приложение Г2. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях.
Таблица 14. Стратегии, направленные на привлечение и удержание под наблюдением, на повышение приверженности АРТ [294]
|
Стратегия
|
Примеры
|
|
Обеспечить доступную, надежную мультидисциплинарную помощь, атмосферу принятия
|
- Врачи, медицинские сестры, социальные работники, фармацевты, медицинские психологи
|
|
Усилить мероприятия по раннему взятию под наблюдение и удержанию под наблюдением
|
- Стимулировать участие мультидисциплинарной команды в привлечении к наблюдению и удержанию под наблюдением
|
|
Оценить знания пациента о ВИЧ-инфекции, профилактике и лечении и на основе этой оценки предоставить информацию
|
- Учитывая текущую базу знаний пациента, предоставить информацию о течении у него ВИЧ-инфекции, включая вирусную нагрузку и уровень CD4, об ожидаемых клинических исходах, а также терапевтических и эпидемиологических последствиях низкой приверженности и о важности находиться под наблюдением
|
|
Выявлять потенциальные барьеры приверженности и навыки приема АРВП - как до начала АРТ, так и на постоянной основе
|
- Оценить когнитивные способности и нарушения
- Оценить поведенческие и психосоциальные проблемы, включая депрессию, психические заболевания, уровень социальной поддержки, характер потребления алкоголя и использование в настоящее время запрещенных препаратов, разглашение пациентом его ВИЧ-статуса и степень стигматизации
- Выявить и устранить проблемы языка и грамотности
- Оценить отношение к АРТ и ожидания пациента от лечения (например, влияние на здоровье, побочные эффекты, последствия низкой приверженности)
- Оценить проблемы с приемом лекарств и возможные проблемы с приверженностью (например, трудности с выполнением предыдущих назначений, побочные действия при приеме других лекарств, успехи и проблемы при лечении других болезней и состояний, необходимость напоминающих устройств и органайзеров)
- Оценить организационные проблемы, включая отсутствие постоянного жилья и дохода, непредсказуемый распорядок дня, отсутствие непрерывного доступа к лекарствам, транспортные проблемы
|
|
Предоставлять необходимые ресурсы
|
- Предоставить лечение или направить пациента для лечения психических заболеваний и зависимостей
- Обеспечить бесперебойную выдачу АРВП
- Предоставить ресурсы для решения жилищных, транспортных и продовольственных проблем
|
|
Вовлечь пациента в выбор режима АРТ
|
- Обсудить потенциальные НЯ, дозировки, частоту приема, лекарственную нагрузку, условия хранения АРВП, пищевые ограничения и последствия несоблюдения режима приема АРВП
- Оценить повседневную активность и адаптировать режим АРТ к образу жизни пациента
- Выберите АРВП с высоким барьером резистентности, если предвидите низкую приверженность
- Обсудите влияние наркотиков на возможность соблюдать приверженность лечению
|
|
Оценивать приверженность при каждом визите
|
- Контролировать ВН как важный биологический маркер приверженности
- Использовать простые шкалы для самооценки поведенческих особенностей и приверженности
- Использовать структурированный подход, который нормализует или поддерживает высокую приверженность и минимизирует социальные проблемы
- Убедиться, что другие члены мультидисциплинарной команды также оценивают и поддерживают приверженность лечению
|
|
Использовать позитивное подкрепление для улучшения достигнутого успеха
|
- Информировать пациентов о низких или неопределяемых уровнях ВН и увеличении CD4 клеток
- Благодарить пациентов за выполнение назначений
|
|
Определить причины снижения приверженности и возможные пути для ее повышения
|
- Неспособность пациента понять режим дозирования
- Сложность режима АРТ (много таблеток, крупные, сложное дозирование, пищевые ограничения, полипрагмазия)
- Отвращение к таблеткам или усталость от их приема
- Побочные эффекты
- Непонимание лекарственной устойчивости и ее связи с приверженностью
- Пациенту не объяснили, как принимать препараты, или он не в состоянии выполнить назначения
- Депрессия, прием наркотиков и алкоголя, бездомность, нищета
- Стигматизация в отношении приема лекарств или выполнении назначений, связанных с ВИЧ
- Неразглашение ВИЧ-статуса, ведущее к пропуску приема АРВП, несвоевременному получению препаратов, невыполнению назначений
|
|
Выбрать методы повышения приверженности из числа доступных и эффективных
|
- Использовать дополнительные инструменты, повышающие соблюдение режима АРТ, в дополнение к образованию и консультированию (например, текстовые СМС-сообщения, таблетницы, таймеры)
- Использовать ресурсы сообщества для поддержания приверженности (например, патронажные медсестры, социальные работники, члены семьи, равные консультанты, транспортное сопровождение)
- Использовать программы помощи пациентам (например, со стороны неправительственных организаций)
- Использовать мотивационные беседы
- Обсудить положительную клиническую динамику, наступившую в результате высокой приверженности
- Шире использовать возможности для привлечения пациентов к диспансерному наблюдению и удержанию под наблюдением (звонки-напоминания, гибкий график приема пациентов, свободный доступ, повышение удовлетворенности пациентов)
|
|
Систематический мониторинг удержания под наблюдением
|
- Регистрировать все визиты и отслеживать пропущенные визиты
|
7.3 Профилактика вторичных инфекций у ВИЧ-инфицированных детей
- Рекомендовано всем ВИЧ-инфицированным пациентам проводить профилактику первого эпизода оппортунистических инфекций в соответствии с табл. 15 (С5) [101]
Таблица 15. Профилактика первого эпизода оппортунистических инфекций у ВИЧ-инфицированных детей [101]
|
Заболевание
|
Критерии назначения и отмены
|
Предпочтительные препараты
|
Альтернативные препараты
|
|
Пневмоцистная пневмония
|
Назначение:
- Дети 1 - 12 месяцев, ВИЧ(+) или с неопределенным ВИЧ-статусом
- ВИЧ(+) дети 1 - 5 лет: CD4 < 500/мкл или < 15%
- ВИЧ(+) дети 6 - 12 лет: CD4 < 200/мкл или < 15%
Отмена:
- Не отменять ВИЧ(+) детям < 1 года
- После >= 6 мес. АРТ и CD4 в теч. > 3 мес.: 1 - 6 лет - >= 15% или >= 500.; >= 6 лет - >= 15% или >= 200
|
- #Ко-тримоксазол [Сульфаметоксазол+Триметоприм]**: TMP 2,5 - 5 мг/кг и SMX 12,5 - 25 мг/кг x 2 РС, TMP не более 320 мг в день и SMX не более 1600 мг в день. Варианты назначения: ежедневно или 2 - 3 дня в неделю в последовательные или альтернативные дни
- Можно: 1 раз в день из расчета по TMP 5 - 10 мг/кг x 1 РС ежедневно
|
- #Дапсон**: детям > 1 месяца - 2 мг/кг x 1 РС (не более 100 мг) или 4 мг/кг (не более 200 мг) x 1 раз в неделю
|
|
Туберкулез (см. соответствующие российские рекомендации)
|
Назначение:
- Внутрикожная проба с туберкулезным антигеном (Р. Манту):
p > 5 мм или (+) тест IGRA
- Вираж туб. проб
- Тесный контакт с больным
- Отсутствие активного туберкулеза
Отмена
При тяжелых нежелательных реакциях
|
- #Изониазид** 10 - 15 мг/кг (не более 300 мг) перорально ежедневно 9 месяцев
Добавочная профилактика м.б. назначена детям, получающим грудное вскармливание, при дефиците белка в диете, при расстройствах питания, при продвинутых стадиях ВИЧ-инфекции, при беременности: пиридоксин** 1 - 2 мг/кг x 1 РС (не более 25 - 50 мг в день)
|
- #Изониазид**: 20 - 30 мг/кг (не более 900 мг) перорально 2 раза в неделю 9 месяцев
- Изониазид** 10 - 15 мг/кг (не более 300 мг в сутки) плюс рифампицин** 10 - 20 мг/кг (не более 600 мг в сутки) 3 - 4 месяца
- #Рифампицин** 10 - 20 мг/кг (не более 600 мг) в сутки 4 - 6 месяцев
|
|
Плановая вакцинация
|
- Дети с перинатальным контактом по ВИЧ
- ВИЧ(+) дети
|
Согласно национальному календарю
|
-
|
|
Токсоплазмоз
|
Назначение:
- Выявление антител к токсоплазме класса IgG у детей с CD4: < 6 лет - < 15%, >= 6 лет - < 100
Отмена:
- Не отменять у детей < 1 года
- После >= 6 мес. АРТ плюс CD4 > 3 месяцев: дети > 1 < 6 лет - >= 15%, >= 6 лет - > 200
Возобновление:
- Дети > 1 < 6 лет: CD4 < 15%
Дети >= 6 лет: CD4 < 200
|
- # Ко-тримоксазол [Сульфаметоксазол+Триметоприм]** 150/750 мг/м2 ПТ x 1 РС. Варианты назначения: ежедневно или 3 раза в неделю в последовательные или альтернативные дни
# Ко-тримоксазол [Сульфаметоксазол+Триметоприм]** 75/375 мг/м2 ПТ x 2 РС. Варианты назначения: ежедневно или 3 раза в неделю в последовательные или альтернативные дни
|
#Дапсон**: детям > 1 месяца 2 мг/кг или 15 мг/м2 ПТ (не более 25 мг) x 1 РС плюс #кальция фолинат** 5 мг 1 раз в 3 дня
|
|
ЦМВ-инфекция
|
Назначение:
- АТ к ЦМВ + тяжелый ИД (CD4 < 50 у детей >= 6 лет; < 5% у детей < 6 лет)
Отмена:
CD4 > 100 у детей >= 6 лет; > 10% у детей < 6 лет
|
- Подростки, которые могут получать взрослые дозы: #валганцикловир** 900 мг x 1 РС с едой
- Дети 4 мес - 16 лет: раствор #валганцикловира** 50 мг/мл: 7 x ППТ x Клиренс креатинина = кол-во мг (не более 900 мг/сутки) x 1 РС с пищей
|
-
|
- Всем пациентам с ВИЧ-инфекцией рекомендована профилактика гриппа A и B (С5) [101] в следующем режиме:
- Назначение и отмена доконтактной профилактики - детям с 3 и 4 ИК по эпидемиологическим показаниям
- Назначение постконтактной профилактики:
- Детям с 3 и 4 ИК
- Детям с 1 и 2 ИК, если невозможна вакцинация
- Препараты
- #Осельтамивир**: > 3 мес < 1 г: 3 мг/кг x 1 РС (# для детей в возрасте младше 1 года) [409]; >= 1 г - 12 лет: <= 15 кг - 30 мг x 1 РС, > 15 - 23 кг - 45 мг x 1 РС, > 23 - 40 кг - 60 мг x 1 РС, > 40 кг - 75 мг x 1 РС; > 13 лет: 75 мг x 1 РС
- Занамивир: >= 5 лет - 10 мг (2 ингаляции) x 1 РС
- Начать в течение 48 часов после контакта
- Продолжать 7 дней после домашнего контакта, 14 дней после контакта в коллективе
- Если после контакта введена вакцина, химиопрофилактику продолжать 2 недели после вакцинации.
- Рекомендовано всем ВИЧ-инфицированным пациентам проводить профилактику рецидива оппортунистических инфекций в соответствии с табл. 16 [101] (С5).
Таблица 16. Профилактика рецидива оппортунистических инфекций у ВИЧ-инфицированных детей [101]
|
Заболевание
|
Критерии назначения и отмены
|
Предпочтительные препараты
|
Альтернативные препараты
|
|
Криптококкоз
|
Назначение:
- Документированное заболевание
Отмена - если соблюдены все критерии:
- Возраст >= 6 лет
- плюс отсутствие симптомов через 12 и более месяцев вторичной профилактики
- плюс CD4 >= 100 и ВН на фоне АРТ ниже уровня определения в течение > 3 мес.
Возобновление:
- CD4 < 100
Вторичная профилактика также является поддерживающей терапией или супрессивной терапией.
|
- Флуконазол** 6 мг/кг (не более 200 мг) x 1 РС ежедневно
|
|
|
Пневмоцистная пневмония
|
Назначение:
- После перенесенного заболевания
Отмена и возобновление:
- Как и при первичной профилактике
|
- #Ко-тримоксазол [Сульфаметоксазол+Триметоприм]**: TMP 2,5 - 5 мг/кг и SMX 12,5 - 25 мг/кг x 2 РС. TMP не более 320 мг в день и SMX не более 1600 мг в день.
Варианты назначения: ежедневно или 2 - 3 дня в неделю в последовательные или альтернативные дни
- Можно: 1 раз в день из расчета по TMP 5 - 10 мг/кг x 1 РС ежедневно
|
· #Дапсон**: детям > 1 месяца - 2 мг/кг х 1 РС (не более 100 мг) или 4 мг/кг (не более 200 мг) х 1 раз в неделю
|
|
Токсоплазмоз (супрессивная терапия)
|
Назначение:
- После перенесенного токсоплазменного энцефалита (ТЭ)
Отмена - если соблюдены все критерии:
- АРТ в течение >= 6 мес.
- плюс закончен курс лечения ТЭ
- плюс отсутствуют симптомы ТЭ
- плюс CD4 в течение >= 6 мес.: дети 1 < 6 лет - >= 15%; дети >= 6 лет - > 200
Возобновление:
- Дети 1 < 6 лет: CD4 < 15%
- Дети >= 6 лет: CD4 < 200
|
- #Клиндамицин** 7 - 10 мг/кг x 3 РС плюс #кальция фолинат** 5 мг x 1 раз в 3 дня
- #Ко-тримоксазол [Сульфаметоксазол+Триметоприм]** 150/750 мг/м2 ПТ x 1 РС плюс #Кальция фолинат** 5 мг 1 раз в 3 дня
|
|
|
Цитомегаловирусная
инфекция
|
Назначение:
- После перенесенного заболевания в виде диссеминированных форм, ретинита, неврологических форм, рецидива поражения ЖКТ
Отмена - если соблюдены все критерии:
- АРТ >= 6 мес.
- плюс проведена консультация врача-офтальмолога (при ретините)
- плюс CD4 в теч. > 6 месяцев: < 6 лет - >= 15%, >= 6 лет - > 100
При наличии ретинита - рутинное наблюдение врачом-офтальмологом каждые 3 - 6 мес.
Возобновление:
- CD4 у детей < 6 лет - < 15%, >= 6 лет - < 100
|
- #Ганцикловир** 5 мг/кг в/в ежедневно
- #Валганцикловир**: дети, которые могут принимать дозы взрослых, - 900 мг x 1 РС с пищей; дети 4 мес. - 16 лет - раствор 50 мг/мл из расчета 7 x ППТ x Клиренс креатинина = кол-во мг (не более 900 мг/сутки) x 1 РС с пищей
|
-
|
Критерии оценки качества медицинской помощи
Критерии оценки качества первичной медико-санитарной помощи детям при ВИЧ-инфекции у детей (коды по МКБ-10: B20, B21, B22, B23, B24, R75, Z21, Z20.6)
|
N п/п
|
Критерии оценки качества
|
Оценка выполнения
|
|
1
|
Проведена химиопрофилактика перинатальной передачи ВИЧ у новорожденного при наличии ВИЧ-инфекции у матери
|
Да/Нет
|
|
2
|
Проведено обследование ребенка на ВИЧ-инфекцию:
- при выявлении ВИЧ-инфекции у матери (и/или отца);
- при выявлении ВИЧ-инфекции у кормящей матери;
- при отсутствии перинатального контакта по ВИЧ-инфекции при выявлении факторов риска инфицирования или клинико-лабораторных признаков ВИЧ-инфекции;
- детей, оставшихся без попечения родителей.
|
Да/Нет
|
|
3
|
Выполнено определение ДНК вируса иммунодефицита человека методом ПЦР (качественное исследование) или количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР (у новорожденных, рожденных ВИЧ-инфицированными матерями, серопозитивными во время беременности и родов, в течение второго месяца жизни)
|
Да/Нет
|
|
4
|
Плановые осмотры пациента врачом, ответственным за наблюдение ВИЧ-инфицированного ребенка, в рамках диспансерного наблюдения ВИЧ-инфицированных детей выполнены:
- при отсутствии АРТ: не реже 1 раза в 3 месяца;
- на фоне АРТ: через 2 и 4 - 8 недель после начала АРТ, затем каждые 3 месяца;
на фоне АРТ в фазе ремиссии при достижении клинического, вирусологического и иммунологического эффектов в течение 2-х и более лет: не реже 1 раза в 6 месяцев
|
Да/Нет
|
|
5
|
При постановке ребенка, инфицированного ВИЧ, на диспансерный учет, проведены исследования:
- исследование CD4+ лимфоцитов с определением процентного содержания и абсолютного количества CD4-лимфоцитов и оценкой степени поражения иммунной системы в соответствии с иммунными категориями в зависимости от возраста ребенка, для выявления показаний к быстрому началу АРТ
- исследование CD8+ лимфоцитов с определением процентного содержания и абсолютного количества CD8-лимфоцитов и вычислением иммунорегуляторного индекса - соотношения абсолютных показателей CD4/CD8 для определения прогноза
|
Да/Нет
|
|
6
|
Выполнено количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР (при взятии пациента на диспансерное наблюдение и не реже 1 раза в 6 месяцев при диспансерном наблюдении)
|
Да/Нет
|
|
7
|
Выполнено семейное клинико-психологическое консультирование или индивидуальное клинико-психологическое консультирование по вопросам приверженности (перед началом антиретровирусной терапии и далее не реже 1 раза в 6 месяцев).
|
Да/Нет
|
|
8
|
Выполнено быстрое начало АРТ (в течение 2х недель от момента постановки на диспансерный учет):
1. детям с подтвержденной ВИЧ-инфекцией в возрасте младше 1 года;
- детям с подтвержденной ВИЧ-инфекцией в возрасте >= 1 года < 6 лет с выраженными клиническими проявлениями (стадии 2В, 4Б, 4В по РК, а также проявления СПИД-индикаторных заболеваний) и/или с тяжелым иммунодефицитом (CD4 <= 500 клеток/мм3);
- детям в возрасте 6 лет и старше с выраженными клиническими проявлениями (стадии 2В, 4Б, 4В по РК, а также проявления СПИД-индикаторных заболеваний) и/или с выраженными иммунными нарушениями (CD4 <= 200 клеток/мм3)
|
Да/Нет
|
|
9
|
У детей 0 - 17 лет, состоящих на диспансерном учете, проведено углубленное неврологическое обследование с целью выявления неврологических нарушений не реже 1 раза в 6 месяцев.
|
Да/Нет
|
|
10
|
Выполнено молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) (при наличии признаков неэффективности антиретровирусной терапии и исключении неприверженности к антиретровирусной терапии)
|
Да/Нет
|
Критерии оценки качества специализированной медицинской помощи детям при ВИЧ-инфекции у детей (коды по МКБ-10: B20, B21, B22, B23, B24, R75, Z21, Z20.6)
|
N п/п
|
Критерии оценки качества
|
Оценка выполнения
|
|
1
|
Профилактический курс антиретровирусной терапии начат в первые 4 - 6 часов после рождения (у новорожденных, рожденных ВИЧ-инфицированными матерями, серопозитивными во время беременности и родов) (при отсутствии противопоказаний к назначению препаратов)
|
Да/Нет
|
|
2
|
Выполнен прием (осмотр, консультация) врача-инфекциониста Центра по профилактике и борьбе со СПИД (или его филиала) или уполномоченной медицинской организации федерального уровня
|
|
|
3
|
Выполнено исследование CD4+ лимфоцитов
|
Да/Нет
|
|
4
|
Выполнено количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР
|
Да/Нет
|
|
5
|
Выполнено назначение антиретровирусной терапии в течение 14 дней от установления диагноза ВИЧ-инфекции (при отсутствии противопоказаний)
|
Да/Нет
|
|
6
|
Выполнено молекулярно-генетическое исследование плазмы крови на наличие мутаций лекарственной резистентности в РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) (при наличии признаков неэффективности антиретровирусной терапии и исключении неприверженности к антиретровирусной терапии)
|
Да/Нет
|
Список литературы
1. Санитарные правила и нормы СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", утвержденные 28 января 2021 года.
2. Годовая форма федерального государственного статистического наблюдения N 61 "Сведения о контингентах, больных ВИЧ-инфекцией".
3. Покровский В.В., Ладная Н.Н., Соколова Е.В., Буравцова Е.В. ВИЧ-инфекция. Информационный бюллетень N 43. - М: 2018, - 55 с.
4. Ладная Н.Н., Покровский В.В., Дементьева Л.А., Соколова Е.В., Козырина Н.В., Нарсия Р.С. ВИЧ-инфекция в Российской Федерации в 2018 г. Международная научно-практическая конференция "Актуальные вопросы ВИЧ-инфекции": Материалы конференции. - СПб: Человек и его здоровье, 2019. - с. 3 - 12.
5. Латышева И.Б., Воронин Е.Е. ВИЧ-инфекция у детей в Российской Федерации. Международная научно-практическая конференция "Актуальные вопросы ВИЧ-инфекции. Охрана здоровья детей с ВИЧ-инфекцией в рамках реализации программы "Десятилетие детства в России". Материалы конференции. - СПб.: Человек и его здоровье, 2018. - с. 9 - 12.
6. Приказ Министерства здравоохранения Российской Федерации от 16 сентября 2003 г N 442 "Об утверждении учетных форм для регистрации детей, рожденных ВИЧ-инфицированными матерями".
7. Форма N 311/у "Донесение о подтверждении диагноза у ребенка, рожденного ВИЧ-инфицированной матерью". Приложение N 5 к приказу Минздрава России от 16.09.03. N 442 "Об утверждении учетных форм для регистрации детей, рожденных ВИЧ-инфицированными матерями".
8. Приказ Министерства здравоохранения Российской Федерации N 170 от 27 мая 1997 года "О переходе органов и учреждений здравоохранения Российской Федерации на Международную статистическую классификацию болезней и проблем, связанных со здоровьем X пересмотра".
9. Овчаров В.К., Максимова М.В. (ред.). Международная статистическая классификация болезней и проблем, связанных со здоровьем: МКБ-10. - Медицина, 1995.
10. Покровский В.В., Юрин О.Г., Кравченко А.В., Беляева В.В., Ермак Т.Н., Шахгильдян В.И., Шахгильдян В.И., Буравцова В.В., Деулина М.О., Ефремова О.С., Канестри В.Г., Козырина Н.В., Ладная Н.Н., Нарсия Р.С., Большенко Н.В., Куимова У.А., Покровская А.В., Попова А.А., Хохлова О.Н., Шилов А.М., Коннов В., Воронин Е.Е., Афонина Л.Ю., Минаева С.В., Зимина В.Н., Вознесенский С.Л. Рекомендации по лечению ВИЧ-инфекции и связанных с ней заболеваний, химиопрофилактике заражения ВИЧ. Эпидемиология и инфекционные болезни. Актуальные вопросы. - 2023. - N 4. Т. 13. - 112 с.
11. Клиническая классификация ВИЧ-инфекции. Приложение к Инструкции по заполнению годовой формы государственного федерального статистического наблюдения N 61 "Сведения о контингентах больных ВИЧ-инфекцией", утвержденной Приказом Минздравсоцразвития России от 17 марта 2006 г. N 166.
12. ВИЧ-инфекция и СПИД: Национальное руководство/под ред. акад. В.В. Покровского. - М.: ГЭОТАР-Медиа, 2013. - 608 с.
13. Centers for Disease Control and Prevention. 1994 Revised classification system for human immunodeficiency virus infection in children less than 13 years of age; Official authorized addenda: human immunodeficiency virus infection codes and official Guidelines for Coding and Reporting ICD-9-CM MMWR September 30, 1994/Vol. 43/No. RR-12, 1 - 10.
14. WHO case definitions of HIV for surveillance and revised clinical staging and immunological classification of HIV-related disease in adults and children. WHO, Geneva, 2007.
15. Selik R.M., Mokotoff E.D., Branson B., Owen S.M., Whitmore S., Hall H.I. Revised Surveillance Case Definition for HIV Infection - United States, 2014. MMWR 2014; 63 (RR No. 3) April 11, 2014; 1 - 13.
16. Panel on Antiretroviral Therapy and Medical Management of HIV-Infected Children. Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection, 2019. Available at http://aidsinfo.nih.gov/contentfiles/lvguidelines/pediatricguidelines.pdf.
17. The European Collaborative Study. Age-related standards for T-lymphocyte subsets based on uninfected children born to human immunodeficiency virus-1-infected women. Pediatr Infect Dis J 1992; 11: 1018 - 26.
18. Hecht F.M., Busch M.P., Rawal B., Rosenberg E., Swanson M., Chesney M., Anderson J., Levy J., Kahn J.O. Use of laboratory tests and clinical symptoms for identification of primary HIV infection. AIDS. 2002; 16(8): 1119 - 29.
19. Воронин Е.Е., Афонина Л.Ю., Фомин Ю.А. Антиретровирусная терапия у детей. Учебное пособие для врачей/под ред. акад. Ю.В. Лобзина. - М.: ООО "Бионика Медиа". - 2014. - 31 с.
20. Справка "ВИЧ-инфекция в Российской Федерации в 2018 году", Федеральный научно-методический центр по профилактике и борьбе со СПИДом ФБУН ЦНИИЭ Роспотребнадзора.
21. Tovo P. A. et al. Prognostic factors and survival in children with perinatal HIV-1 infection//The Lancet. - 1992. - Т. 339. - N. 8804. - С. 1249 - 1253.
22. Махмудова Р.У., Закирова К.А. Распространенность оппортунистических инфекций-туберкулеза, сочетанного с ВИЧ-инфекцией, среди детей и проблемы раннего выявления//Научно-практический журнал ТИППМК. - 2014. - N. 4. - С. 72 - 73.
23. Садовникова В.Н. Заболеваемость и распространенность ВИЧ-инфекции среди женщин и детей//Инфекционные болезни. - 2009. - Т. 7. - N. 3. - С. 12 - 17.
24. Воронин Е.Е., Афонина Л.Ю., Байбарина Е.Н., Чумакова О.В., Садовникова В.Н. Раннее выявление ВИЧ-инфекции у детей. Методические рекомендации. - 2018. М: МЗ РФ. - 11 с.
25. Афонина Л.Ю., Воронин Е.Е. Совершенствование ранней диагностики ВИЧ-инфекции у детей. Международная научно-практическая конференция "Актуальные вопросы ВИЧ-инфекции. Охрана здоровья детей с ВИЧ-инфекцией в рамках реализации программы "Десятилетие детства в России". Материалы конференции. - СПб.: Человек и его здоровье, 2018. - с. 13 - 17. в России". Материалы конференции. - СПб.: Человек и его здоровье, 2018. - с. 13 - 17.
26. Goga AE. Impact of breastfeeding, maternal antiretroviral treatment and health service factors on 18-month vertical transmission of HIV and HIV-free survival: results from a nationally representative HIV-exposed infant cohort, South Africa. J Epidemiol Community Health 2020; 0: 1 - 9.
27. Ngbapai J.G., Izudi J., Okoboi S. Cessation of breastfeeding and associated factors in the era of elimination of mother to child transmission of HIV at Ndejje health center, Uganda: a retrospective cohort study. International Breastfeeding Journal. 2020 Sep 7; 15(1): 78.
28. Tess B.H. et al. Breastfeeding, genetic, obstetric and other risk factors associated with mother-to-child transmission of HIV-1 in Sao Paulo State, Brazil//Aids. - 1998. - T. 12. - N. 5. - С. 513 - 520.
29. Pizzo P.A. et al. Markers and determinants of disease progression in children with HIV infection//The Pediatric AIDS Siena Workshop. - 1995. - T. 8. - N. 1. - С. 30 - 44.
30. Pahwa S. Human immunodeficiency virus infection in children: nature of immunodeficiency, clinical spectrum and management//The Pediatric infectious disease journal. - 1988. - T. 7. - N. 5 Suppl. - С. S61 - 71.
31. Barnhart H.X. et al. Natural history of human immunodeficiency virus disease in perinatally infected children: an analysis from the Pediatric Spectrum of Disease Project//Pediatrics. - 1996. - T. 97. - N. 5. - С. 710 - 716.
32. Cooper E.R. et al. Encephalopathy and progression of human immunodeficiency virus disease in a cohort of children with perinatally acquired human immunodeficiency virus infection//The Journal of pediatrics. - 1998. - T. 132. - N. 5. - С. 808 - 812.
33. Clemens, S.L., Macneal, K. D., Alons, C. L., & Cohn, J. E. (2020). Screening Algorithms to Reduce Burden of Pediatric HIV Testing: A Systematic Review and Meta-analysis. Pediatr Infect Dis J. 2020 Oct; 39(10): e303 - e309.
34. Calis J. C. J. et al. HIV-associated anemia in children: a systematic review from a global perspective//Aids. - 2008. - T. 22. - N. 10. - С. 1099 - 1112.
35. Ziegler J.L., Katongole-Mbidde E. Kaposi's sarcoma in childhood: an analysis of 100 cases from Uganda and relationship to HIV infection//International Journal of Cancer. - 1996. - T. 65. - N. 2. - С. 200 - 203.
36. Granovsky M.O. et al. Cancer in human immunodeficiency virus-infected children: a case series from the Children's Cancer Group and the National Cancer Institute//Journal of clinical oncology. - 1998. - T. 16. - N. 5. - С. 1729 - 1735.
37. Mueller B.U. Cancers in human immunodeficiency virus-infected children//JNCI Monographs. - 1998. - T. 1998. - N. 23. - С. 31 - 35.
38. B-Lajoie M.R. et al. Incidence and prevalence of opportunistic and other infections and the impact of antiretroviral therapy among HIV-infected children in low-and middle-income countries: a systematic review and meta-analysis. Clin Infect Dis. 2016 Jun 15; 62(12): 1586 - 1594.
39. Diaconu I.A. et al. Diagnosing HIV-associated cerebral diseases - The importance of neuropathology in understanding HIV//Rom J Morphol Embryol. - 2016. - T. 57. - N. 2 Suppl. - С. 745 - 50.
40. Mikol J. et al. The epidemiology of cerebral lymphoma in AIDS//Journal of Neuroradiology= Journal de Neuroradiologie. - 1995. - T. 22. - N. 3. - С. 204 - 206.
41. Chitsike I. et al. Childhood cancers in Zimbabwe: a 10 year review of the Zimbabwe National cancer registry data//Central African Journal of Medicine. - 2014. - T. 60. - N. 1. - С. 1 - 8.
42. Marx, Jean L. Human T-Cell Leukemia Virus Linked to AIDS.-Science. (May 20, 1983): 20, (4599) 806 - 809.
43. Hesseling A. C. et al. High incidence of tuberculosis among HIV-infected infants: evidence from a South African population-based study highlights the need for improved tuberculosis control strategies//Clinical Infectious Diseases. - 2009. - T. 48. - N. 1.
44. Palme I. B. et al. Impact of human immunodeficiency virus 1 infection on clinical presentation, treatment outcome and survival in a cohort of Ethiopian children with tuberculosis//The Pediatric infectious disease journal. - 2002. - T. 21. - N. 11. - С. 1.
45. Dodd P.J. et al. The impact of HIV and antiretroviral therapy on TB risk in children: a systematic review and meta-analysis//Thorax. - 2017. - T. 72. - N. 6. - С. 559 - 575.
46. Chandwani S. et al. Cytomegalovirus infection in human immunodeficiency virus type 1-infected children//The Pediatric infectious disease journal. - 1996. - T. 15. - N. 4. - С. 310 - 314.
47. Weinberg A. et al. Immune correlates of herpes zoster in HIV-infected children and youth//Journal of virology. - 2012. - T. 86. - N. 5. - С. 2878 - 2881.
48. Brandt C.D. et al. Epstein-Barr virus DNA in the blood of infants, young children, and adults by age and HIV status//Journal of acquired immune deficiency syndromes and human retrovirology: official publication of the International Retrovirology Association. 1998 Jan 1; 17(1): 69 - 72.
49. Pollock B.H. et al. Risk factors for pediatric human immunodeficiency virus-related malignancy//Jama. - 2003. - T. 289. - N. 18. - С. 2393 - 2399.
50. Gona P. et al. Incidence of opportunistic and other infections in HIV-infected children in the HAART era//Jama. - 2006. - T. 296. - N. 3. - С. 292 - 300.
51. Brennan A.T. et al. A meta-analysis assessing diarrhea and pneumonia in HIV-exposed uninfected compared with HIV-unexposed uninfected infants and children//JAIDS Journal of Acquired Immune Deficiency Syndromes. - 2019. - T. 82. - N. 1. - С. 1 - 8.
52. Likasitwattanakul S., Poneprasert B., Sirisanthana V. Cryptococcosis in HIV-infected children//Headache. - 2004. - T. 13. - N. 16. - С. 81.
53. Makni F., Cheikrouhou F., Ayadi A. Parasitoses and immunodepression//Archives de l'Institut Pasteur de Tunis. - 2000. - T. 77. - N 1 - 4. - С. 51 - 54.
54. Arango M. et al. Histoplasmosis: results of the Colombian national survey, 1992 - 2008//Biomedica. - 2011. - T. 31. - N. 3. - С. 344 - 356.
55. Wilmshurst J.M. et al. Specific neurologic complications of human immunodeficiency virus type 1 (HIV-1) infection in children//Journal of child neurology. - 2006. - T. 21. - N. 9. - С. 788 - 794.
56. Korir A. et al. Developing clinical strength-of-evidence approach to define HIV-associated malignancies for cancer registration in Kenya//PLoS One. - 2014. - T. 9. - N. 1. - С. e85881.
57. Harris, C., Mills, R., Seager, E., Blackstock, S., Hiwa, T., Pumphrey, J., Kennedy, N. (2018). Paediatric deaths in a tertiary government hospital setting, Malawi. Paediatrics and International Child Health, 1 - 9. doi:10.1080/20469047.2018.1536873.
58. Sabbagh P. et al. The global and regional prevalence, burden, and risk factors for methicillin-resistant Staphylococcus aureus colonization in HIV-infected people: a systematic review and meta-analysis. American Journal of Infection Control. 2019. Mar; 47(3): 323 - 333.
59. Huson M. A. M. et al. Community-acquired bacterial bloodstream infections in HIV-infected patients: a systematic review//Clinical infectious diseases. - 2014. - T. 58. - N. 1. - С. 79 - 92.
60. Oldham S.A. et al. HIV-associated lymphocytic interstitial pneumonia: radiologic manifestations and pathologic correlation//Radiology. - 1989. - T. 170. - N 1. - С. 83 - 87.
61. Sharland M., Gibb D. M., Holland F. Respiratory morbidity from lymphocytic interstitial pneumonitis (LIP) in vertically acquired HIV infection//Archives of disease in childhood. - 1997. - T. 76. - N. 4. - С. 334 - 336.
62. Ford N. et al. Causes of hospital admission among people living with HIV worldwide: a systematic review and meta-analysis//The lancet HIV. - 2015. - T. 2. - N. 10. - С. e438 - e444.
63. Sonego M. et al. Risk factors for mortality from acute lower respiratory infections (ALRI) in children under five years of age in low and middle-income countries: a systematic review and meta-analysis of observational studies//PloS one. - 2015. - T. 10.
64. Becquet R. et al. Children who acquire HIV infection perinatally are at higher risk of early death than those acquiring infection through breastmilk: a meta-analysis//PloS one. - 2012. - T. 7. - N. 2. - С. e28510.
65. Read J.S. et al. Diagnosis of HIV-1 infection in children younger than 18 months in the United States//Pediatrics. - 2007. - T. 120. - N. 6. - С. e1547 - e1562.
66. Cohn, J., Whitehouse, K., Tuttle, J., Lueck, K., & Tran, T. (2016). Paediatric HIV testing beyond the context of prevention of mother-to-child transmission: a systematic review and meta-analysis. The Lancet HIV, 3(10), e473 - e481. doi:10.1016/s2352-3018(16) 30050-9.
67. Bispo S. et al. Postnatal HIV transmission in breastfed infants of HIV-infected women on ART: a systematic review and meta-analysis//Journal of the International AIDS Society. - 2017. - T. 20. - N. 1. - С. 21251.
68. Leroy V. et al. International multicentre pooled analysis of late postnatal mother-to-child transmission of HIV-1 infection//The Lancet. - 1998. - T. 352. - N. 9128. - С. 597 - 600.
69. Schmid J., Chiba J. (2017). The intersection of abandonment, HIV-positive status and residential care for a group of perinatally infected adolescents. African Journal of AIDS Research, 16(1), 47 - 56. doi:10.2989/16085906.2017.1296476.
70. Read J. S. et al. Quantification of human immunodeficiency virus type 1 p24 antigen and antibody rivals human immunodeficiency virus type 1 RNA and CD4+ enumeration for prognosis//The Pediatric infectious disease journal. - 2000. - T. 19. - N. 6. - С. 54.
71. Claassen M. et al. Pitfalls with rapid HIV antibody testing in HIV-infected children in the Western Cape, South Africa//Journal of clinical virology. - 2006. - T. 37. - N. 1. - С. 68 - 71.
72. Urassa W. et al. Evaluation of the WHO human immunodeficiency virus (HIV) antibody testing strategy for the diagnosis of HIV infection//Clinical and diagnostic virology. - 1994. - T. 2. - N. 1. - С. 1 - 6.
73. Nielsen K., Bryson Y. J. Diagnosis of HIV infection in children//Pediatric Clinics of North America. - 2000. - T. 47. - N. 1. - С. 39 - 63.
74. Burgard M. et al. Performance of HIV-1 DNA or HIV-1 RNA tests for early diagnosis of perinatal HIV-1 infection during anti-retroviral prophylaxis//The Journal of pediatrics. - 2012. - T. 160. - N. 1. - С. 60 - 66. e1.
75. Rouet F. et al. Early diagnosis of paediatric HIV-1 infection among African breast-fed children using a quantitative plasma HIV RNA assay//Aids. - 2001. - T. 15. - N. 14. - С. 1849 - 1856.
76. Weintrub P.S. et al. Use of polymerase chain reaction for the early detection of HIV infection in the infants of HIV-seropositive women//AIDS (London, England). - 1991. - T. 5. - N. 7. - С. 881 - 884.
77. Updated recommendations on first-line and second-line antiretroviral regimens and post-exposure prophylaxis and recommendations on early infant diagnosis of HIV: interim guidance. Geneva: World Health Organization; 2018 (WHO/CDS/HIV/18.18). License: CC BY.
78. Gulia J., Kumwenda N., Li Q., Taha T.E. HIV seroreversion time in HIV-1-uninfected children born to HIV-1-infected mothers in Malawi. J Acquir Immune Defic Syndr. 2007; 46(3): 332 - 337.
79. Alcantara K.C., Pereira G.A., Albuquerque M., Stefani M.M. Seroreversion in children born to HIV-positive and AIDS mothers from Central West Brazil. Trans R Soc Trop Med Hyg. 2009; 103(6): 620 - 626.
80. Sohn A.H., Thanh T.C., Thinh le Q., et al. Failure of human immunodeficiency virus enzyme immunoassay to rule out infection among polymerase chain reaction-negative Vietnamese infants at 12 months of age. Pediatr Infect Dis J.2009; 28(4): 273 - 276.
81. Bamford A., Turkova A., Lyall H., Foster C., Klein N., Bastiaans D., Burger D., Bernadi S., Butler K., Chiappini E., Clayden P., Della Negra M., Giacomet V., Giaquinto C., Gibb D., Galli L., Hainaut M., Koros M., Marques L., Nastouli E., Niehues T., Noguera-Julian A., Rojo P., Rudin C., Scherpbier H., Tudor-Williams G., Welch S. and PENTA Steering Committee (2015), Paediatric European Network for Treatment of AIDS (PENTA) guidelines for treatment of paediatric HIV-1 infection 2015: optimizing health in preparation for adult life. British HIV Association HIV Medicine (2015).
82. Rogers M.F., Ou C.Y., Rayfield M., et al. Use of the polymerase chain reaction for early detection of the proviral sequences of human immunodeficiency virus in infants born to seropositive mothers. New York City Collaborative Study of Maternal HIV Transmission and Montefiore Medical Center HIV Perinatal Transmission Study Group. N Engl J Med. 1989 Jun 22; 320(25): 1649 - 54.
83. Fiscus S.A., McMillion T., Nelson J.A., Miller W.C. Validation of the gen-probe aptima qualitative HIV-1 RNA assay for diagnosis of human immunodeficiency virus infection in infants. J Clin Microbiol. 2013; 51(12): 4137 - 4140.
84. Technau K.G., Mazanderani A.H., Kuhn l., et al. Prevalence and outcomes of HIV-1 diagnostic challenges during universal birth testing - an Sous African observational cohort. J Int AIDS Soc. 2017; 20 (Suppl 6): 217 - 61.
85. Jendis J.B., Tomasik Z., Hunziker Jourdain Jourdain U., et al. Evaluation of diagnostic tests for HIV infection in infants born to HIV-infected mothers in Switzerland. AIDS. 1988; 2(4): 273 - 9.
86. Donovan M., Palumbo P. Diagnosis of HIV: challenges and strategies for HIV prevention and detection among pregnant women and their infants. Clin Perinatol. 2010; 37(4): 751 - 763, viii.
87. Luzuriaga K., Sullivan J.L. DNA polymerase chain reaction for the diagnosis of vertical HIV infection. JAMA.1996; 275 (17): 1360 - 1361.
88. Read J.S., Committee on Pediatric AIDS, American Academy of Pediatrics. Diagnosis of HIV-1 infection in children younger than 18 months in the United States. Pediatrics. 2007; 120(6): e1547 - 1562.
89. Arikawa S. et al. Mortality risk and associated factors in HIV-exposed, uninfected children//Tropical Medicine & International Health. - 2016. - T. 21. - N. 6. - С. 720 - 734.
90. Veloso V. G. et al. HIV rapid testing as a key strategy for prevention of mother-to-child transmission in Brazil//Revista de saude publica. - 2010. - T. 44. - N. 5. - С. 803 - 811.
91. Cassol S. et al. Rapid screening for early detection of mother-to-child transmission of human immunodeficiency virus type 1//Journal of clinical microbiology. - 1994. - T. 32. - N. 11. - С. 2641 - 2645.
92. Mallampati D. et al. Performance of virological testing for early infant diagnosis: a systematic review//JAIDS Journal of Acquired Immune Deficiency Syndromes. - 2017. - T. 75. - N. 3. - С. 308 - 314.
93. Brown E. et al. Determining an optimal testing strategy for infants at risk for mother-to-child transmission of HIV-1 during the late postnatal period//AIDS (London, England). - 2008. - T. 22. - N. 17. - С. 2341.
94. Frange P. et al. Late postnatal HIV infection in children born to HIV-1-infected mothers in a high-income country//Aids. - 2010. - T. 24. - N. 11. - С. 1771 - 1776.
95. Coutsoudis A. et al. Breastfeeding and IIV International Transmission Study Group: Late postnatal transmission of HIV-1 in breast-fed children: an individual patient data meta-analysis//J Infect Dis. - 2004. - T. 189. - N. 12. - С. 2154 - 2166.
96. World Health Organization. Updated recommendations on first-line and second-line antiretroviral regimens and post-exposure prophylaxis and recommendations on early infant diagnosis of HIV: interim guidelines: supplement to the 2016 consolidated guidlines.
97. Gibb D.M. et al. Markers for predicting mortality in untreated HIV-infected children in resource-limited settings: a meta-analysis//AIDS (London, England). - 2008. - T. 22. - С. 97 - 105.
98. Mugglin C. et al. Retention in care of HIV-infected children from HIV test to start of antiretroviral therapy: systematic review//PLoS One. - 2013. - T. 8. - N. 2. - С. e56446.
99. Study H.I. V. P. P. M. C. Use of total lymphocyte count for informing when to start antiretroviral therapy in HIV-infected children: a meta-analysis of longitudinal data//The Lancet. - 2005. - T. 366. - N. 9500. - С. 1868 - 1874.
100. Hughes R.A., May M.T., Tilling K., et al. Long terms trends in CD4+ cell counts, CD8+ cell counts, and the CD4+: CD8+ ratio. AIDS. 2018 Jun 19; 32(10): 1361 - 1367.
101. Panel on Opportunistic Infections in HIV-Exposed and HIV-Infected Children. Guidelines for the Prevention and Treatment of Opportunistic Infections in HIV-Exposed and HIV-Infected Children. Department of Health and Human Services. 2024. Guidelines for the Prevention and Treatment of Opportunistic Infections in Children with and Exposed to HIV (nih.gov).
102. O'Gorman M. R. G., Zijenah L. S. CD4 T cell measurements in the management of antiretroviral therapy - A review with an emphasis on pediatric HIV-infected patients. Cytometry Part B: 2008; 74B (Suppl. 1): S19 - S26, 2008
103.  S. et al. Prognostic factors of a lower CD4/CD8 ratio in long term viral suppression HIV infected children//PloS one. - 2019. - T. 14. - N. 8. - С. e0220552.
S. et al. Prognostic factors of a lower CD4/CD8 ratio in long term viral suppression HIV infected children//PloS one. - 2019. - T. 14. - N. 8. - С. e0220552.
104. Ray K., Gupta S.M., Bala M., Muralidhar S., Kumar J. CD4/CD8 lymphocyte counts in healthy, HIV-positive individuals & AIDS patients. - Indian J Med Res 124, September 2006, pp 319 - 330.
105. Trickey A., May M.T., Schommers P., et al. CD4:CD8 ratio and CD8 count as prognostic markers for mortality in human immunodeficiency virus-infected patients on antiretroviral therapy: the Antiretroviral Therapy Cohort Collaboration (ART-CC). Clin Infect Dis. 2017 Sep 15; 65(6): 959 - 966.
106. Mussini C., Lorenzini P., Cozzi-Lepri A., et al. CD4/CD8 ratio normalization and non-AIDS related events in individuals with HIV who achieved viral load suppression on antiretroviral therapy: an observational cohort study. Lancet HIV. 2015; 2: e98 - 106.
107. Serrano-Villar S., Saiz T., Sulggi A.L., et al. HIV infected individuals with low CD4/CD8 ratio despite effective antiretroviral therapy exhibit altered T cell subsets, heightened CD8+T cell activation and increased risk of non-AIDS morbidity and mortality. Randomized Controlled Trial. PLoS Pathog. 2014 May 15;10(5):e1004078.
108. Serrano-Villar S., Moreno S., Fuentes-Ferrer M. et al. The CD4:CD8 ratio is associated with markers of age-associated disease in virally suppressed HIV-infected patients with immunological recovery. HIV Med. 2014; 15: 40 - 49.
109. Hema M.N., Ferry T., Dupon M., et al. Low CD4/CD8 ratio is associated with non-AIDS-defining cancers in patients on antiretroviral therapy: ANRS CO8(Aproco/copilote) prospective cohort study. PLoS One. 2016; 11: e0161594.
110. Triplette M., Attia E.F., Akgun K.M., et al. A low peripheral blood CD4/CD8 ratio is associated with pulmonary emphysema in HIV. PLoS One. 2017; 12: e0170857.
111. Chereau F., Madec Y., Sabin C., Obel N., Ruiz-Mateos E., Chrysos G., Fidler S., Lehmann C., Zangerle Robert., Wittkop L., Reiss P., Hamouda O., Estrada Perez V., The HIV Controllers Project Working Group for the Collaboration of Observational HIV Epidemiological Research Europe (COHERE) in EuroCOORD. Impact of CD4 and CD8 dynamics and viral rebounds on loss of virological control in HIV controllers. PLoS One. 2017 Apr 5; 12(4): e0173893.
112. Gibellini L., Pecorini S., De Biasi S., Bianchini E., Digaetano M., Pinti M. et al. HIV-DNA content in different CD4+T-cell subsets correlates with CD4+cell: CD8+ cell ratio or length of efficient treatment. AIDS. 2017 Jun 19; 31(10): 1387 - 1392.
113. Mofenson L.M. et al. The relationship between serum human immunodeficiency virus type 1 (HIV-1) RNA level, CD4 lymphocyte percent, and long-term mortality risk in HIV-1-infected children//Journal of Infectious Diseases. - 1997. - T. 175. - N. 5. - С. 10.
114. Adetifa I.M. O. et al. Haematological abnormalities associated with paediatric HIV/AIDS in Lagos//Annals of tropical paediatrics. - 2006. - T. 26. - N. 2. - С. 121 - 125.
115. Ruhinda E. N., Bajunirwe F., Kiwanuka J. Anaemia in HIV-infected children: severity, types and effect on response to HAART//BMC pediatrics. - 2012. - T. 12. - N. 1. - С. 1 - 6.
116. Strehlau R. et al. Lipid profiles in young HIV-infected children initiating and changing antiretroviral therapy//Journal of acquired immune deficiency syndromes (1999). - 2012. - T. 60. - N. 4. - С. 369.
117. Manglani M.V. et al. HLA-B* 5701 allele in HIV-infected Indian children and its association with Abacavir hypersensitivity//Indian pediatrics. - 2018. - T. 55. - N. 2. - С. 140 - 141.
118. Puthanakit T. et al. Prevalence of human leukocyte antigen-B* 5701 among HIV-infected children in Thailand and Cambodia: implications for abacavir use//The Pediatric infectious disease journal. - 2013. - T. 32. - N. 3. - С. 252.
119. Jesson J. et al. Adverse events associated with abacavir use in HIV-infected children and adolescents: a systematic review and meta-analysis//The Lancet HIV. - 2016. - T. 3. - N. 2. - С. e64 - e75.
120. Cargnin, S., Jommi, C., Canonico, P. L., Genazzani, A. A., & Terrazzino, S. (2014). Diagnostic accuracy of HLA-B*57:01 screening for the prediction of abacavir hypersensitivity and clinical utility of the test: a meta-analytic review. Pharmacogenomics, 2014 May; 15(7): 963 - 76.
121. Hammond E. et al. External quality assessment of HLA-B* 5701 reporting: an international multicentre survey//Antiviral therapy. - 2007. - T. 12. - N. 7. - С. 1027 - 1032.
122. Esezobor C. I. et al. Prevalence of proteinuria among HIV-infected children attending a tertiary hospital in Lagos, Nigeria//Journal of tropical pediatrics. - 2010. - T. 56. - N. 3. - С. 187 - 190.
123. Eke F.U. et al. Microalbuminuria in children with human immunodeficiency virus (HIV) infection in Port Harcourt, Nigeria//Nigerian Journal of Medicine. - 2010. - T. 19. - N. 3.
124. Telatela S. P., Matee M. I., Munubhi E. K. Seroprevalence of hepatitis B and C viral co-infections among children infected with human immunodeficiency virus attending the paediatric HIV care and treatment center at Muhimbili National Hospital in Dar-es-Salaam, Tanzania. BMC Public Health. 2007 Nov 22: 7: 338.
125. Campos F. A. et al. Incidence of congenital toxoplasmosis among infants born to HIV-coinfected mothers: case series and literature review//Brazilian Journal of Infectious Diseases. - 2014. - T. 18. - N. 6. - С. 609 - 617.
126. Suri D. et al. Cytomegalovirus Disease in HIV-infected Children-A Single-Centre Clinical Experience over 23 Years//Journal of Tropical Pediatrics. - 2018. - T. 64. - N. 3. - С. 215 - 224.
127. Aggerbeck H. et al. C-Tb skin test to diagnose Mycobacterium tuberculosis infection in children and HIV-infected adults: A phase 3 trial//PloS one. - 2018. - T. 13. - N. 9. - С. e0204554.
128. Ford N., Shubber Z., Meintjes G., Grinsztejn B., Eholie S., Mills E. J. et al. (2015). Causes of hospital admission among people living with HIV worldwide: a systematic review and meta-analysis. The Lancet HIV, 2(10), e438 - e444. doi:10.1016/.
129. Gonzalez C.E. et al. Cryptococcosis in human immunodeficiency virus-infected children//The Pediatric infectious disease journal. - 1996. - T. 15. - N. 9. - С. 796 - 800.
130. Marcy O. et al. Performance of Xpert MTB/RIF and alternative specimen collection methods for the diagnosis of tuberculosis in HIV-infected children//Clinical Infectious Diseases. - 2016. - T. 62. - N. 9. - С. 1161 - 1168.
131. Mendez H. Ambulatory care of HIV-seropositive infants and children//The Journal of pediatrics. - 1991. - T. 119. - N. 1. - С. S14 - S17.
132. StudyM H. I. V. P. P. M. C. Predictive value of absolute CD4 cell count for disease progression in untreated HIV-1-infected children//Aids. - 2006. - T. 20. - N. 9. - С. 1289 - 1294.
133. Tetali S. et al. Virus load as a marker of disease progression in HIV-infected children//AIDS research and human retroviruses. - 1996. - T. 12. - N. 8. - С. 669 - 675.
134. KalishLA. Evaluation of Human Immunodeficiency Virus (HIV) Type 1 Load, CD4 T Cell Level, and Clinical Class as Time-Fixed and Time-Varying Markers of Disease Progression in HIV-1-Infected Children//J. Infect. Dis. 1999. Vol. 180, N 5. P. 1514 - 1520.
135. Palumbo P. E. et al. Predictive value of quantitative plasma HIV RNA and CD4+ lymphocyte count in HIV-infected infants and children//Jama. - 1998. - T. 279. - N. 10. - С. 756 - 761.
136. ARROW Trial Team et al. Routine versus clinically driven laboratory monitoring and first-line antiretroviral therapy strategies in African children with HIV (ARROW): a 5-year open-label randomised factorial trial//The Lancet. - 2013. - T. 381. - N. 9875.
137.  F. V. F. et al. Renal abnormalities in a cohort of HIV-infected children and adolescents//Pediatric Nephrology. - 2016. - T. 31. - N. 5. - С. 773 - 778.
F. V. F. et al. Renal abnormalities in a cohort of HIV-infected children and adolescents//Pediatric Nephrology. - 2016. - T. 31. - N. 5. - С. 773 - 778.
138. Adetokunboh O. O. et al. The burden of vaccine-preventable diseases among HIV-infected and HIV-exposed children in sub-Saharan Africa: a systematic review and meta-analysis//Human Vaccines & Immunotherapeutics. - 2019. - T. 15. - N. 11. - С. 2590 - 2605.
139. Gil A.C. M. et al. Hepatotoxicity in HIV-infected children and adolescents on antiretroviral therapy//Sao Paulo Medical Journal. - 2007. - T. 125. - N. 4. - С. 205 - 209.
140. Fokunang C. N. et al. Evaluation of hepatotoxicity and nephrotoxicity in HIV patients on highly active anti-retroviral therapy//Journal of AIDS and HIV Research. - 2010. - T. 2. - N. 3. - С. 046 - 057.
141.  M. et al. Prevalence and predictors of liver disease in HIV-infected children and adolescents//Scientific Reports. - 2017. - T. 7. - N. 1. - С. 1 - 8.
M. et al. Prevalence and predictors of liver disease in HIV-infected children and adolescents//Scientific Reports. - 2017. - T. 7. - N. 1. - С. 1 - 8.
142. Geffriaud C. et al. Hepatic involvement in HIV 1 virus infection//Gastroenterologie clinique et biologique. - 1988. - T. 12. - N. 5. - С. 465.
143. Palchetti, C. Z., Szejnfeld, V. L., de Menezes Succi, R. C., Patin, R. V., Teixeira, P. F., Machado, D. M., & Oliveira, F. L. C. (2015). Impaired bone mineral accrual in prepubertal HIV-infected children: a cohort study. The Brazilian Journal of Infectiou.
144. Sogni P.,  D., Podevin P. Management of cirrhosis complications in HIV patients coinfected with hepatitis B or C virus//Presse medicale (Paris, France: 1983). - 2005. - T. 34. - N. 20 Pt 2. - С. 1579.
D., Podevin P. Management of cirrhosis complications in HIV patients coinfected with hepatitis B or C virus//Presse medicale (Paris, France: 1983). - 2005. - T. 34. - N. 20 Pt 2. - С. 1579.
145. Sigel K. et al. Cancer screening in patients infected with HIV//Current Hiv/aids Reports. - 2011. - T. 8. - N. 3. - С. 142 - 152.
146. Walenda C. et al. Morbidity in HIV-1-Infected children treated or not treated with highly active antiretroviral therapy (HAART), Abidjan, Cote d'Ivoire, 2000-04//Journal of tropical pediatrics. - 2009. - T. 55. - N. 3. - С. 170 - 176.
147. Berteloot L. et al. Value of chest x-ray in TB diagnosis in HIV-infected children living in resource-limited countries: the ANRS 12229-PAANTHER 01 study//The International Journal of Tuberculosis and Lung Disease. - 2018. - T. 22. - N. 8. - С. 844 - 850.
148. Rylance S. et al. Effect of antiretroviral therapy on longitudinal lung function trends in older children and adolescents with HIV-infection//PloS one. - 2019. - T. 14. - N. 3. - С. e0213556.
149. Norton K.I. et al. Chronic radiographic lung changes in children with vertically transmitted HIV-1 infection//American Journal of Roentgenology. - 2001. - T. 176. - N. 6. - С. 1553 - 1558.
150. Luginbuhl L.M. et al. Cardiac morbidity and related mortality in children with HIV infection//Jama. - 1993. - T. 269. - N. 22. - С. 2869 - 2875.
151. Mantegazza C. et al. Assessment of HIV infection status in children and adolescents through bowel ultrasound//Digestive and Liver Disease. - 2013. - T. 45. - С. e282 - e283.
152. Unsal A.B. et al. Effect of antiretroviral therapy on bone and renal health in young adults infected with HIV in early life//The Journal of Clinical Endocrinology & Metabolism. - 2017. - T. 102. - N. 8. - С. 2896 - 2904.
153. Zambrano P.O. et al. Renal compromise in HIV/AIDS in patients attended at a chilean children hospital//Revista chilena de infectologia: organo oficial de la Sociedad Chilena de Infectologia. - 2009. - T. 26. - N. 1. - С. 21 - 25.
154. Sigaloff K.C.E. et al. HIV-1-resistance-associated mutations after failure of first-line antiretroviral treatment among children in resource-poor regions: a systematic review//The Lancet infectious diseases. - 2011. - T. 11. - N. 10. - С. 769 - 779.
155. Phillips N. et al. HIV-associated cognitive impairment in perinatally infected children: a meta-analysis//Pediatrics. - 2016. - T. 138. - N. 5. - С. e20160893.
156. Фомина М.Ю., Титова М.А. Цереброавскулярные расстройства у детей с перинатальной ВИЧ-инфекцией: клинические и лучевые аспекты.//Журнал инфектологии. - том 10, N 4, 2018. - с. 72 - 77.
157. Jahanshad N. et al. Brain imaging and neurodevelopment in HIV-uninfected Thai children born to HIV-infected mothers//The Pediatric infectious disease journal. - 2015. - T. 34. - N. 9. - С. e211.
158. Dean O. et al. Brain magnetic resonance imaging findings associated with cognitive impairment in children and adolescents with human immunodeficiency virus in Zambia//Pediatric Neurology. - 2020. - T. 102. - С. 28 - 35.
159. Yadava S.K., Guptab R.K., Gargc R.K., Venkateshd V., Guptab P.K., Singhc A.K., Hashema S., Al-Sulaitia A., Kaurae D., Wanga E., Marincolaa F.M., Haris M. Altered structural brain changes and neurocognitive performance in pediatric HIV. NeuroImage: Clinical. 14 (2017) 316 - 322.
160. Wade B.S.C., Valcour V.G., Puthanakit T., Saremi A., Gutmanf B.A., Nir T.M. et al. Mapping abnormal subcortical neurodevelopment in a cohort of Thai children with HIV. NeuroImage: Clinical 23 (2019) 101810.
161. Hoare J., Fouche J.-P., Phillips N., Joska J.A., Myer L., Zar H.J., Stein D.J. Structural brain changes in perinatally HIV infected young adolescents in South Africa. Running head: Brain Imaging in adolescents living with HIV. AIDS, 2018 November 28; 32(18): 2707 - 2718.
162. Загайнова А.И., Афонина Л.Ю., Воронин Е.Е., Епоян Т.А./Под ред. Загайновой А.И. Книга для настоящих и будущих родителей (информационное пособие для родителей и опекунов детей, затронутых эпидемией ВИЧ-инфекции. - М., 2010. - 187 стр.
163. Van Elsland S.L., Peters R.P.H., Grobbelaar C., Ketelo P., Kok M.O., Cotton M.F., van Furth A.M. Disclosure of human immunodeficiency virus status to children in South Africa: A comprehensive analysis. S Afr J HIV Med. 2019; 20(1), a884.
164. Kim S.H., Gerver S.M., Fidler S., Ward H. Adherence to antiretroviral therapy in adolescents living with HIV: systematic review and meta-analysis. AIDS. 2014; 28(13): 1945 - 1956.
165. Saberi P., Neilands T.B., Vittinghoff E., Johnson M.O., Chesney M., Cohn S.E. Barriers to Antiretroviral Therapy Adherence and Plasma HIV RNA Suppression Among AIDS Clinical Trials Group Study Participants. AIDS Patient Care STDS. 2015 Mar 1; 29(3): 111 - 1.
166. Первый Российский консенсус по количественной оценке приверженности к лечению: основные положения, алгоритмы и рекомендации - одобрен XII Национальным конгрессом терапевтов (Москва, 22 - 24 ноября 2017 г.).//Медицинский вестник Северного Кавказа, 2018, т. 13.
167. Николаев Н.А. Доказательная гипертензиология: пациенториентированная антигипертензивная терапия: монография. - М.: Издательский дом Академии Естествознания, 2015. - 178 с.
168. Morisky D.E., Green L.W., Levine D.M. Concurrent and Predictive Validity of a Self-Reported Measure of Medication Adherence. Medical Care. 1986 Jan; Vol. 24, No. 1, pp. 67 - 74.
169. Al-Hassany L., Kloosterboer S.M., Dierckx B., Koch B.C. Assessing methods of measuring medication adherence in chronically ill children-a narrative review. Patient Prefer Adherence. 2019; 13: 1175 - 1189.
170. Gopakumar, K.G., Bhat, K.G., Baliga, S., Joseph, N., Mohan, N., Shetty, A.K. Impact of care at foster homes on the health-related quality of life of HIV-infected children and adolescents: A cross-sectional study from India. Quality of Life Research, 2018 Apr; 27940: 871 - 877.
171. Lyon M.E., Garvie P.A., Briggs L., He, J., Malow R., D'Angelo L.J., McCarter R. Is it safe? Talking to teens with HIV/AIDS about death and dying: A 3-month evaluation of Family Centered Advance Care (FACE) planning - Anxiety, depression, quality of life. HIV/AIDS - Research and Palliative Care 2010: 227 - 37.
172. Xu T., Wu Z., Yan Z., Rou K., Duan S. Measuring health-related quality of life in children living in HIV/AIDS-affected families in rural areas in Yunnan, China: Preliminary reliability and validity of the Chinese version of PedsQL 4.0 Generic Core Scales.
173. Bomba M., Nacinovich R., Oggiano S., Cassani M., Baushi L., Bertulli C., Longhi D., Coppini S., Parrinello G., Plebani A., Badolato R. Poor health-related quality of life and abnormal psychosocial adjustment in Italian children with perinatal HIV infection receiving highly active antiretroviral treatment. AIDS Care. 2010 Jul; 22(7): 858 - 65.
174. Williams P. L. et al. Predictors of adherence to antiretroviral medications in children and adolescents with HIV infection//Pediatrics. - 2006. - T. 118. - N. 6. - С. e1745 - e1757.
175. Wood S.M., Shah S.S., Steenhoff A.P., Rutstein R.M. The impact of AIDS diagnoses on long-term neurocognitive and psychiatric outcomes of surviving adolescents with perinatally acquired HIV AIDS 2009, 23: 1859 - 1865.
176. Bucek A., Leu C.-S., Benson S., Warne P., Abrams E.J., Elkington K.S. et al. Psychiatric Disorders, Antiretroviral Medication Adherence, and Viremia in a Cohort of Perinatally HIV-Infected Adolescents and Young Adults. Pediatr Infect Dis J. 2018 July; 37(7): 673 - 677.
177. Lwidiko A., Kibusi S.M., Nyundo A., Mpondo B.C.T. Association between HIV status and depressive symptoms among children and adolescents in the Southern Highlands Zone, Tanzania: A case-control study. PLoS ONE 2018; 13(2): e0193145.
178. Laughton B., Cornell M., Kidd M., Springer P.E., Dobbels E.F.M.-T., Van Rensburg A.J. et al. Five year neurodevelopment outcomes of perinatally HIV-infected children on early limited or deferred continuous antiretroviral therapy. Journal of the International AIDS Society 2018, 21: e25106.
179. Смулевич А.Б. Депрессии в общей медицине. Руководство для врачей. М., Медицинское информационное агентство, 2007 г., - 256 с.
180. Bjelland I.; Dahl A.A., Haug T., Tangen D., Neckelmann D. The validity of the Hospital Anxiety and Depression Scale. An updated literature review. Journal of Psychosomatic Research. 2002; 52 (2): 69 - 77.
181. Chan Y.-F., Leung D.Y.P., Fong D.Y.T., Leung C.-M., Lee A.M. Psychometric evaluation of the Hospital Anxiety and Depression Scale in a large community sample of adolescents in Hong Kong. Qual Life Res. 2010; 19: 865 - 873.
182. Ochigbo S.O., Torty C., Oparah S. Predictors of Anxiety and Depression Among Caregivers of Human Immunodeficiency Virus Positive Children in Calabar, Nigeria. International Journal of HIV/AIDS Prevention, Education and Behavioural Science. 2018; Vol. 4, N.
183. Savard J., Laberge B., Gauthier J.G., Ivers H., Bergeron M.G. Evaluating anxiety and depression in HIV-infected patients. J Pers Assess. 1998; Dec; 71(3): 349 - 67.
184. Brown L.K., Kennard B.D., Emslie G.J., Mayes T.L., Whiteley L.B., Bethel J., Xu J., Thornton S., Tanney M.R., Hawkins L.A, Garvie P.A., Subramaniam G.A., Worrell C.J., Stoff L.W., and Adolescent Trials Network for HIV/AIDS Interventions. Effective Treatment of Depressive Disorders in Medical Clinics for Adolescents and Young Adults Living With HIV: A Controlled Trial. J Acquir Immune Defic Syndr. 2016 Jan 1; 71(1): 38 - 46.
185. Shaw S, Amico KR. Antiretroviral therapy adherence enhancing interventions for adolescents and young adults 13 - 24 Years of Age: a review of the evidence base. J Acquir Immune Defic Syndr. 2016; 72(4): 387 - 399.
186. MacPherson P, Munthali C, Ferguson J, et al. Service delivery interventions to improve adolescents' linkage, retention and adherence to antiretroviral therapy and HIV care. Trop Med Int Health. 2015; 20(8): 1015 - 1032.
187. Casale M, Carlqvist A, Cluver L. Recent interventions to improve retention in HIV Care and adherence to antiretroviral treatment among adolescents and youth: a systematic review. AIDS Patient Care STDS. 2019; 33(6): 237 - 252.
188. Беляева В.В., Афонина Л.Ю., Дмитриева Е.В., Рюмина И.И., Фролов С.А., Шухов В.С., Нилл Макки. Коммуникация и консультирование в области ВИЧ-инфекции. Пособие для медицинских работников. Москва, 2008. - 109 с.
189. Афонина Л.Ю., Воронин Е.Е. Приверженность антиретровирусной терапии в разрезе биомедицинской сферы. Международная научно-практическая конференция "Актуальные вопросы ВИЧ-инфекции": Материалы конференции. - СПб: Человек и его здоровье, 2019. - с. 16 - 35.
190. The European AIDS Clinical Society (EACS) Guidelines Version 12.0 October 2023. 123p. http://www.eacsociety.org.
191. Епифанов А.Ю. Комплексная оценка и коррекция приверженности ВААРТ. Международная научно-практическая конференция "Актуальные вопросы ВИЧ-инфекции": Материалы конференции. - СПб: Человек и его здоровье, 2019. - с. 83 - 89.
192. Biadgilign S. et al. Barriers and facilitators to antiretroviral medication adherence among HIV-infected paediatric patients in Ethiopia: A qualitative study//SAHARA-J: Journal of Social Aspects of HIV/AIDS. - 2009. - T. 6. - N. 4. - С. 148 - 154.
193. Shubber Z. et al. Patient-reported barriers to adherence to antiretroviral therapy: a systematic review and meta-analysis//PLoS medicine. - 2016. - T. 13. - N. 11. - С. e1002183.
194. Rueda S. et al. Patient support and education for promoting adherence to highly active antiretroviral therapy for HIV/AIDS//Cochrane database of systematic reviews. - 2006. - N. 3.
195. Poorolajal J. et al. Survival rate of AIDS disease and mortality in HIV-infected patients: a meta-analysis//Public Health. - 2016. - T. 139. - С. 3 - 12.
196. Cotton M. F. et al. Early time-limited antiretroviral therapy versus deferred therapy in South African infants infected with HIV: results from the children with HIV early antiretroviral (CHER) randomised trial//The Lancet. - 2013. - T. 382. - N. 9904. -.
197. Violari A. et al. Early antiretroviral therapy and mortality among HIV-infected infants//New England Journal of Medicine. - 2008. - T. 359. - N. 21. - С. 2233 - 2244.
198. Penazzato M. et al. Optimisation of antiretroviral therapy in HIV-infected children under 3 years of age//Cochrane Database of Systematic Reviews. - 2014. - N. 5.
199. Puthanakit T. et al. Early versus deferred antiretroviral therapy for children older than 1 year infected with HIV (PREDICT): a multicentre, randomised, open-label trial//The Lancet infectious diseases. - 2012. - T. 12. - N. 12. - С. 933 - 941.
200. Johnson S. et al. Rapid initiation of antiretroviral therapy for people living with HIV//The Cochrane database of systematic reviews. - 2018. - T. 2018. - N. 2.
201. Lawn S.D.,  M. E., Wood R. Optimum time to start antiretroviral therapy during HIV-associated opportunistic infections//Current opinion in infectious diseases. - 2011. - T. 24. - N. 1. - С. 34.
M. E., Wood R. Optimum time to start antiretroviral therapy during HIV-associated opportunistic infections//Current opinion in infectious diseases. - 2011. - T. 24. - N. 1. - С. 34.
202. Consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV-infection. Recommendation for the public health approach. WHO, 2nd edition, Geneva, 2016. 480p. http://www.who.int/hiv.
203. Foster C., Bamford A., Turkova A., Welch S. and Klein N. On behalf of the PENTA Guidelines Writing Group and PENTA steering committee. Paediatric European Network for Treatment of AIDS. Treatment Guideline 2016 update: antiretroviral therapy recommended for all children living with HIV. HIV Med. 2017 Feb; 18(2): 133 - 134.
204. Mbuagbaw L. C. E. et al. Efavirenz or nevirapine in three-drug combination therapy with two nucleoside-reverse transcriptase inhibitors for initial treatment of HIV infection in antiretroviral-naive individuals//Cochrane Database of Systematic Reviews. 2016 Dec 10; 12(12): CD004246.
205. Spaulding A., Rutherford G. W., Siegfried N. Stavudine or zidovudine in three-drug combination therapy for initial treatment of HIV infection in antiretroviral-naive individuals//Cochrane Database of Systematic Reviews. - 2010. - N. 8.
206. Spaulding A., Rutherford G.W., Siegfried N. Tenofovir or zidovudine in three-drug combination therapy with one nucleoside reverse transcriptase inhibitor and one non-nucleoside reverse transcriptase inhibitor for initial treatment of HIV infection in antiretrovirals-naive individuals. Cochrane Database Syst Rev. 2010 Oct 6:(10):CD008740.
207. Penazzato M. et al. Effectiveness of antiretroviral therapy in HIV-infected children under 2 years of age//Cochrane Database of Systematic Reviews. - 2012. - N. 7.
208. Kanters S. et al. Comparative efficacy and safety of first-line antiretroviral therapy for the treatment of HIV infection: a systematic review and network meta-analysis//The lancet HIV. - 2016. - T. 3. - N. 11. - С. e510 - e520.
209. Kityo C. et al. Raltegravir-intensified initial antiretroviral therapy in advanced HIV disease in Africa: A randomised controlled trial//PLoS medicine. - 2018. - T. 15. - N. 12. - С. e1002706.
210. Fowler M.G. et al. Efficacy and safety of an extended nevirapine regimen in infants of breastfeeding mothers with HIV-1 infection for prevention of HIV-1 transmission (HPTN 046): 18-month results of a randomized, double-blind, placebo-controlled trial. J Acquir Immune Defic Syndr. 2014 Mar 1; 65(3): 366 - 74.
211. Barlow-Mosha L. et al. Nevirapine-versus lopinavir/ritonavir-based antiretroviral therapy in HIV-infected infants and young children: long-term follow-up of the IMPAACT P1060 randomized trial//Clinical Infectious Diseases. - 2016. - T. 63. - N. 8. - С. 1.
212. Денисенко В.Б., Симованьян Э.Н. Совершенствование антиретровирусной терапии у детей с ВИЧ-инфекцией//Детские инфекции. - 2018. - T. 17. - N. 2.
213. Cotton M. F. et al. Safety and efficacy of atazanavir powder and ritonavir in HIV-1-infected infants and children from 3 months to < 11 years of age: the PRINCE-2 study//The Pediatric infectious disease journal. - 2018. - T. 37. - N. 6. - С. e149 - e156.
214. Frange P. et al. Similar efficacy and safety of dolutegravir between age groups of HIV-1-infected paediatric and young adult patients aged 5 years and older//HIV medicine. - 2019. - T. 20. - N. 8. - С. 561 - 566.
215. Paediatric European Network for the Treatment of AIDS (PENTA et al. Lamivudine/abacavir maintains virological superiority over zidovudine/lamivudine and zidovudine/abacavir beyond 5 years in children//Aids. - 2007. - T. 21. - N. 8. - С. 947 - 955.
216. Ciaranello A.L. et al. Effectiveness of pediatric antiretroviral therapy in resource-limited settings: a systematic review//Clinical Infectious Diseases. - 2009. - T. 49. - N. 12. - С. 1915 - 1927.
217. Funk M.B. et al. Effect of first line therapy including efavirenz and two nucleoside reverse transcriptase inhibitors in HIV-infected children//European journal of medical research. - 2005. - T. 10. - N. 12. - С. 503.
218. Ross L.L. et al. Treatment-Emergent Mutations and Resistance in HIV-Infected Children Treated with Fosamprenavir-Containing Antiretroviral Regimens//The open AIDS journal. - 2015. - T. 9. - С. 38.
219. Hakim J.G. et al. Lopinavir plus nucleoside reverse-transcriptase inhibitors, lopinavir plus raltegravir, or lopinavir monotherapy for second-line treatment of HIV (EARNEST): 144-week follow-up results from a randomised controlled trial//The Lancet Infect Dis. 2018 Jan; 18(1): 47 - 57.
220. Национальная ассоциация специалистов в области ВИЧ/СПИДа Клинические рекомендации. ВИЧ-инфекция у детей [Электронный ресурс]//URL: http://rushiv.ru/wp-content/uploads/2019/03/kr459.pdf (Дата последнего обращения: 07.07.2020).
221. Gaur A.H., Kizito H., Prasitsueubsai W. et al. Safety, efficacy, and pharmacokinetics of a single-tablet regimen containing elvitegravir, cobicistat, emtricitabine, and tenofovir alafenamide in treatment-naive, HIV-infected adolescents: a single arm, open-label trial. Lancet HIV. 2016 Dec; 3(12): e561 - e568.
222. Falcon-Neyra L. et al. Off-label use of rilpivirine in combination with emtricitabine and tenofovir in HIV-1-infected pediatric patients: A multicenter study//Medicine. - 2016. - T. 95. - N. 24.
223. Van Dyke R.B. et al. Toxicities associated with dual nucleoside reverse-transcriptase inhibitor regimens in HIV-infected children//The Journal of infectious diseases. - 2008. - T. 198. - N. 11. - С. 1599 - 1608.
224. Tudor-Williams G. et al. Etravirine in treatment-experienced, HIV-1-infected children and adolescents: 48-week safety, efficacy and resistance analysis of the phase II PIANO study//HIV medicine. - 2014. - T. 15. - N. 9. - С. 513 - 524.
225. Rutherford G.W. et al. Predicting treatment failure in adults and children on antiretroviral therapy: a systematic review of the performance characteristics of the 2010 WHO immunologic and clinical criteria for virologic failure//Aids. - 2014. - T. 28.
226. Davies M. A. et al. The role of targeted viral load testing in diagnosing virological failure in children on antiretroviral therapy with immunological failure//Tropical Medicine & International Health. - 2012. - T. 17. - N. 11. - С. 1386 - 1390.
227. Grennan J.T., Loutfy M.R., Su D., et al. Magnitude of virologic blips is associated with a higher risk for virologic rebound in HIV-infected individuals: a recurrent events analysis. J Infect Dis. 2012; 205(8): 1230 - 1238.
228. Vandenhende M.A., Perrier A., Bonnet F., et al. Risk of virological failure in HIV-1-infected patients experiencing lowlevel viraemia under active antiretroviral therapy (ANRS C03 cohort study). Antivir Ther. 2015; 20(6): 655 - 60.
229. Ribaudo H.J., Lennox J., Currier J., et al. Virologic failure endpoint definition in clinical trials: is using HIV-1 RNA threshold < 200 copies/mL better than < 50 copies/mL? an analysis of ACTG Studies. Abstract 580. Presented at: Conference on Retroviruses and Opportunistic Infections; 2009. Montreal, Canada.
230. Panel on Antiretroviral Therapy and Medical Management of HIV-Infected Children. Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection. Guidelines for the Use of Antiretroviral Agents in Pediatric HIV Infection (Last Updated: January 31, 2024; Last Reviewed: January 31, 2024) [Электронный ресурс]. Available at http://aidsinfo.nih.gov/contentfiles/lvguidelines/pediatricguidelines.pdf. Accessed 11.03.2024.
231. Collins I.J. et al. Incidence of switching to second-line antiretroviral therapy and associated factors in children with HIV: an international cohort collaboration//The Lancet HIV. - 2019. - T. 6. - N. 2. - С. e105 - e115.
232. Goetghebuer T. et al. Time to switch to second-line antiretroviral therapy in children with human immunodeficiency virus in Europe and Thailand//Clinical Infectious Diseases. - 2018.
233. Govender R. et al. Neurologic and neurobehavioral sequelae in children with human immunodeficiency virus (HIV-1) infection//Journal of child neurology. - 2011. - T. 26. - N. 11. - С. 1355 - 1364.
234. Bacha T., Tilahun B., Worku A. Predictors of treatment failure and time to detection and switching in HIV-infected Ethiopian children receiving first line anti-retroviral therapy//BMC infectious diseases. - 2012. - T. 12. - N. 1. - С. 197.
235. Westley B.P. et al. Prediction of treatment failure using 2010 World Health Organization Guidelines is associated with high misclassification rates and drug resistance among HIV-infected Cambodian children//Clinical Infectious Diseases. - 2012. - T. 55.
236. Mullen J. et al. Antiretroviral drug resistance among HIV-1 infected children failing treatment//Journal of medical virology. - 2002. - T. 68. - N. 3. - С. 299 - 304.
237. Agwu A. L., Fairlie L. Antiretroviral treatment, management challenges and outcomes in perinatally HIV-infected adolescents//Journal of the International AIDS Society. - 2013. - T. 16. - N. 1. - С. 18579.
238. Obasa A. E. et al. Drug resistance mutations against protease, reverse transcriptase and integrase inhibitors in people living with HIV-1 receiving boosted protease inhibitors in South Africa//Frontiers in Microbiology. - 2020. - T. 11. - С. 438.
239. Patten G. et al. What should we do when HIV-positive children fail first-line combination antiretroviral therapy? a comparison of 4 ART management strategies//The Pediatric infectious disease journal. - 2019. - T. 38. - N. 4. - С. 400.
240. Ramos J.T., De Jose M.I., Duenas J., et al. Safety and antiviral response at 12 months of lopinavir/ritonavir therapy in human immunodeficiency virus-1-infected children experienced with three classes of antiretrovirals. Pediatr Infect Dis J. 2005; 24(10): 867 - 73.
241. Resino S., Bellon J.M., Munoz-Fernandez M.A., Spanish Group of HIV Infection. Antiretroviral activity and safety of lopinavir/ritonavir in protease inhibitor-experienced HIV-infected children with severe-moderate immunodeficiency. J Antimicrob Chemother. 2006 Mar; 57(3): 579 - 82.
242. Violari A., Bologna R., Kumarasamy N., et al. Safety and efficacy of darunavir/ritonavir in treatment-experienced pediatric patients: week 48 results of the ARIEL trial. Pediatr Infect Dis J. 2015; 34(5): e132 - 137.
243. Blanche S., Bologna R., Cahn P., et al. Pharmacokinetics, safety and efficacy of darunavir/ritonavir in treatment experienced children and adolescents. AIDS. 2009; 23(15): 2005 - 2013.
244. Viani R.M., Alvero C., Fenton T., et al. Safety, Pharmacokinetics and efficacy of dolutegravir in treatment-experienced HIV-1 infected adolescents: 48-week results from IMPAACT P1093. Pediatr Infect Dis J. 2015; 34(11): 1207 - 13.
245. Zheng Y., Hughes M.D., Lockman S., et al. Antiretroviral therapy and efficacy after virologic failure on first-line boosted protease inhibitor regimens. Clin Infect Dis. 2014; 59(6): 888 - 896.
246. Harrison L., Melvin A., Fiscus S., et al. HIV-1 drug resistance and second-line treatment in children randomized to switch at low versus higher RNA thresholds. J Acquir Immune Defic Syndr. 2015; 70(1): 42 - 53.
247. Meyers T., Sawry S., Wong J.Y., et al. Virologic failure among children taking lopinavir/ritonavir-containing first-line antiretroviral therapy in South Africa. Pediatr Infect Dis J. 2015; 34(2): 175 - 179.
248. Galan I., Jimenez J.L., Gonzalez-Rivera M., et al. Virological phenotype switches under salvage therapy with Lopinavir/ritonavir in heavily pretreated HIV-1 vertically infected children. AIDS. 2004; 18(2): 247 - 255.
249. Frange P., Chaix M. L., Blanche S. Preserving future therapeutic options: should we limit the lamivudine use in young HIV-1 infected children initiating first-line HAART?//Aids. - 2013. - T. 27. - N. 2. - С. 151 - 154.
250. Lu X. et al. HIV-1 drug-resistant mutations and related risk factors among HIV-1-positive individuals experiencing treatment failure in Hebei Province, China//AIDS research and therapy. - 2017. - T. 14. - N. 1. - С. 4.
251. Zhong M. et al. Analysis of HIV genotypic drug resistance among pediatric HIV/AIDS cases with virological failure after free antiretroviral therapy in Yunnan province//Zhonghua yi xue za zhi. - 2014. - T. 94. - N. 12. - С. 884 - 888.
252. McNamara, J. (2005). Clinical trials for HIV-infected children. In S. Zeichner & J. Read (Eds.), Textbook of Pediatric HIV Care (pp. 635 - 642). Cambridge: Cambridge University Press. doi:10.1017/CBO9780511544798.046.
253. World Health Organization et al. Antiretroviral therapy of HIV infection in infants and children: towards universal access: recommendations for a public health approach-2010 revision. - World Health Organization, 2010.
254. Rojas Sanchez P., Holguin A. Drug resistance in the HIV-1-infected paediatric population worldwide: a systematic review//Journal of Antimicrobial Chemotherapy. - 2014. - T. 69. - N. 8. - С. 2032 - 2042.
255. Patel K. et al. Impact of HAART and CNS-penetrating antiretroviral regimens on HIV encephalopathy among perinatally infected children and adolescents//AIDS (London, England). - 2009. - T. 23. - N. 14. - С. 1893.
256. Van den Hof M. et al. CNS penetration of ART in HIV-infected children//Journal of Antimicrobial Chemotherapy. - 2018. - T. 73. - N. 2. - С. 484 - 489.
257. Kanters S. et al. Interventions to improve adherence to antiretroviral therapy: a systematic review and network meta-analysis//The lancet HIV. - 2017. - T. 4. - N. 1. - С. e31 - e40.
258. Clay P.G. The abacavir hypersensitivity reaction: a review. Clin Ther. 2002 Oct; 24(10): 1502 - 14.
259. Федеральный закон от 30 марта 1995 г. N 38-ФЗ "О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)".
260. Распоряжение Правительства Российской Федерации от 20 октября 2016 г N 2203-р "Об утверждении Государственной стратегии противодействия распространению ВИЧ-инфекции в Российской Федерации на период до 2020 года и дальнейшую перспективу".
261. Федеральный закон от 21 ноября 2011 г. N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации", Федеральный закон от 29.11.2010 N 326-ФЗ "Об обязательном медицинском страховании в Российской Федерации."
262. Suksomboon N., Poolsup N., Ket-Aim S. Systematic review of the efficacy of antiretroviral therapies for reducing the risk of mother-to-child transmission of HIV infection//Journal of clinical pharmacy and therapeutics. - 2007. - T. 32. - N. 3. - С. 293 - 3.
263. Siegfried N. et al. Antiretrovirals for reducing the risk of mother-to-child transmission of HIV infection//Cochrane database of systematic reviews. - 2011. - N. 7.
264. Адамян Л.В., Афонина Л.Ю., Баранов И.И., Воронин Е.Е., Кан Н.Е., Кузьмин В.Н., Козырина Н.В., Покровский В.В., Садовникова В.Н., Тютюнник В.Л., Юрин О.Г. Применение антиретровирусных препаратов в комплексе мер, направленных на профилактику передачи ВИЧ от матери ребенку. Клинические рекомендации (протокол лечения). Эпидемиол. и инфекц. болезни. Актуал. вопр. 2015; 3 (приложение). 24 с.
265. Panel on Treatment of Pregnant Women with HIV Infection and Prevention of Perinatal Transmission. Recommendations for Use of Antiretroviral Drugs in Transmission in the United States, 2019.
266. Katz I.T., Shapiro D.E., Tuomala R. Factors associated with lack of viral suppression at delivery. Ann Intern Med. 2015; 162(12): 874 - 875.
267. RitchieLMP. What interventions are effective in improving uptake and retention of HIV-positive pregnant and breastfeeding women and their infants in prevention of mother to child transmission care programmes in low-income and middle-income countries//BMJ open. - 2019. - T. 9. - N. 7. - С. e024907.
268. Horvath T. et al. Interventions for preventing late postnatal mother-to-child transmission of HIV//Cochrane database of systematic reviews. - 2009. - N. 1.
269. Chiappini E. et al. Use of combination neonatal prophylaxis for the prevention of mother-to-child transmission of HIV infection in European high-risk infants//Aids. - 2013. - T. 27. - N. 6. - С. 991 - 1000.
270. Kovalchik S.A. Mother's CD4+ count moderates the risk associated with higher parity for late postnatal HIV-free survival of breastfed children: an individual patient data meta-analysis of randomized controlled trials//AIDS and Behavior. - 2012. - T. 16.
271. Kassa G.M. Mother-to-child transmission of HIV infection and its associated factors in Ethiopia: a systematic review and meta-analysis//BMC infectious diseases. 2018 May 10; 18(1): 216.
272. Dunn D. HIV Paediatric Prognostic Markers Collaborative Study Group. Short-term risk of disease progression in HIV-1-infected children receiving no antiretroviral therapy or zidovudine monotherapy: a meta-analysis. Lancet. 2003 Nov 15; 362(9396): 1605 - 11.
273. Chiappini E. et al. for the European Pregnancy and Paediatric HIV Cohort Collaboration (EPPICC) study group in EuroCoord. Use of combination neonatal prophylaxis for the prevention of mother-to-child transmission of HIV infection in European high-risk infants. AIDS 2013, vol 27 No 6: 991 - 1000.
274. John G.C. et al. Timing of breast milk HIV-1 transmission: a meta analysis//East African medical journal. - 2001. - T. 78. - N. 2. - С. 75 - 79.
275. Yah C.S., Tambo E. Why is mother to child transmission (MTCT) of HIV a continual threat to new-borns in sub-Saharan Africa (SSA)//Journal of Infection and Public Health. - 2019. - T. 12. - N. 2. - С. 213 - 223.
276. Victoria C.G. et al. Effect of breastfeeding on infant and child mortality due to infectious diseases in less developed countries: a pooled analysis//Lancet (British edition). - 2000. - T. 355. - N. 9202. - С. 451 - 455.
277. Daniels B. et al. Effect of co-trimoxazole prophylaxis on morbidity and mortality of HIV-exposed, HIV-uninfected infants in South Africa: a randomised controlled, non-inferiority trial//The Lancet Global Health. - 2019. - T. 7. - N. 12. - С. e1717 - e1727.
278. Zachariah R. et al. Scaling-up co-trimoxazole prophylaxis in HIV-exposed and HIV-infected children in high HIV-prevalence countries//The Lancet Infectious Diseases. - 2007. - T. 7. - N. 10. - С. 686 - 693.
279. Boettiger D.C. et al. Temporal Trends in Co-trimoxazole Use Among Children on Antiretroviral Therapy and the Impact of Co-trimoxazole on Mortality Rates in Children Without Severe Immunodeficiency//Journal of the Pediatric Infectious Diseases Society. - 2019 Nov 6; 8(5): 450 - 460.
280. B-Lajoie M.R., Drouin O., Bartlett G., et al. Incidence and prevalence of opportunistic and other infections and the impact of antiretroviral therapy among HIV-infected children in low- and middle-income countries: a systematic review and metaanalysis. Clin Infect Dis. 2016 Jun 15; 62(12): 1586 - 1594.
281. Consolidated guidelines on HIV prevention, testing, Treatment, service Delivery and monitoring: Recommendations for a Public health approach, WHO. July 2021.
282. Ford N., Shubber Z., Calmy A., Irvine C., Rapparini C. et al. (2015). Choice of Antiretroviral Drugs for Postexposure Prophylaxis for Adults and Adolescents: A Systematic Review. Clinical Infectious Diseases, 60(suppl 3), S170 - S17.
283. McManus H., Hoy J.F., Woolley I., Boyd M.A., Kelly M.D., Mulhall B., Roth N.J., Petoumenos K., Law M.G. and the Australian HIV observational database. Recent trends in early stage response to combination antiretroviral therapy in Australia. Antivir Ther. 2015; 20(2): 131 - 139.
284. "90-90-90" Амбициозная цель в области лечения, способствующая прекращению эпидемии СПИДа. Объединенная программа Организации Объединенных Наций по ВИЧ/СПИДу (ЮНЭЙДС): Женева, Швейцария, 2014.
285. Global Health Sector Strategy on HIV 2016 - 2021 Towards Ending AIDS. WHO, Geneva: 2016.
286. Patel A., Hirschhorn L., Fullem A., Ojikutu B., Oser R. Adult Aherence to Treatment and Retention in Care. Arlington, VA: USAID | AIDSTAR-ONE PROJECT, Task Order 1, June 2010.
287. Lamb M. R., Fayorsey R., Nuwagaba-Biribonwoha H., Viola V., Mutabazi V., Alwar T., Casalini C., Elul B. High attrition before and after ART initiation among youth (15 - 24 years of age) enrolled in HIV care. AIDS. 2014 February 20; 28(4): 559 - 568.
288. WHO. Adherence to Long-term Therapies: Evidence for Action. Geneva. 2003. 198p.
289. Shubber Z., Mills E.J., Nachega J.B., Vreeman R., Freitas M., Bock P., et al. (2016) Patient-Reported Barriers to Adherence to Antiretroviral Therapy: A Systematic Review and Meta-Analysis. PLoS Med 13(11).
290. Nachega J.B., Parienti J.J., Uthman O.A., et al. Lower pill burden and once-daily antiretroviral treatment regimens for HIV infection: A meta-analysis of randomized controlled trials. Clin Infect Dis. May 2014; 58(9): 1297 - 1307.
291. Langebeek N., Gisolf E.H., Reiss P. Vervoort S.C.,  T.B., Richter C., Sprangers M. AG., Nieuwkerket P.T. Predictors and correlates of adherence to combination antiretroviral therapy (ART) for chronic HIV infection: a meta-analysis. BMC Med. 2014 Aug 21:12:142.
T.B., Richter C., Sprangers M. AG., Nieuwkerket P.T. Predictors and correlates of adherence to combination antiretroviral therapy (ART) for chronic HIV infection: a meta-analysis. BMC Med. 2014 Aug 21:12:142.
292. Antinori A., Arendt G., Becker J.T., Brew B.J., Byrd D.A., Cherner M., Clifford D.B., Cinque P., Epstein L.G., Goodkin K., Gisslen M., Grant I., Heaton R.K., Joseph J., Marder K., Marra C.M., McArthur J.C., Nunn M., Price R.W., Pulliam L., Robertson K.R., Sacktor N., Valcour V., Wojna V.E. "Updated Research Nosology for HIV-Associated Neurocognitive Disorders," Neurology, Vol. 69, No. 18, 2007, pp. 1789 - 1799.
293. Gandhi N.D., Moxley R.T., Creighton J., Roosa H.V., Skolasky R.L., Selnes O.A., McArthur J., Sacktor N. Comparison of scales to evaluate the progression of HIVassociated neurocognitive disorder. HIV Ther. 2010 May; 4(3): 371 - 379.
294. Guidelines for the use of antiretroviral agents in HIV-1-infected adults and adolescents. Developed by the panel on clinical practices for treatment of HIV infection convened by the Department of Health and Human Services (DHHS). February 247, 2024. Guidelines for the Use of Antiretroviral Agents in Adults and Adolescents with HIV (nih.gov).
295. Федеральный закон "О внесении изменений в Федеральный закон "Об основах охраны здоровья граждан в Российской Федерации" по вопросам оказания паллиативной медицинской помощи" от 06.03.2019 N 18-ФЗ.
296. Приказ Минздрава России N 345н, Минтруда России от 31.05.2019 N 372н "Об утверждении положения об организации оказания паллиативной медицинской помощи, включая порядок взаимодействия медицинских организаций, организаций социального обслуживания и общественных объединений, иных некоммерческих организаций, осуществляющих свою деятельность в сфере охраны здоровья".
297. Приказ Минздрава России N 348н от 31 мая 2019 года "Об утверждении перечня медицинских изделий, предназначенных для поддержания органов и систем организма человека, предоставляемых для использования на дому".
298. Приказ Минздрава России N 505н от 10 июля 2019 года "Об утверждении Порядка передачи от медицинской организации пациенту (его законному представителю) медицинских изделий, предназначенных для поддержания функций органов и систем организма человека, для использования на дому при оказании паллиативной медицинской помощи".
299. Приказ МЗ РФ N 831 от 3 октября 2019 года "Об утверждении ведомственной целевой программы "Развитие системы оказания паллиативной медицинской помощи"
300. Tudor-Williams G. et al. Etravirine in treatment-experienced, HIV-1-infected children and adolescents: 48-week safety, eficacy and resistance analysis of the phase II PIANO study//HIV Medicine (2014), 15, 513 - 524.
301. MacBraynea C.E., Rutsteinb R.M., Wizniac A.A., Grahamd B., Alveroe C.G., Fairlief L. et al. The IMPAACT P1090 Protocol Team. Etravirine in treatment-experienced HIV-1-infected children 1 year to less than 6 years of age. A phase I/II, open-label trial. AIDS 2021, 35: 1413 - 1421.
302. Инструкция по медицинскому применению лекарственного препарата  ЛП-006054-190521.
ЛП-006054-190521.
303. Gaur A.H., Cotton M.F., Rodriguez C.A., McGrath E.J.,  E., Liberty A. et al. Fixed-dose combination bictegravir, emtricitabine, and tenofovir alafenamide in adolescents and children with HIV: week 48 results of a single-arm, open-label, multicentre, phase 2/3 trial. Lancet Child Adolesc Health 2021; 5: 642 - 51.
E., Liberty A. et al. Fixed-dose combination bictegravir, emtricitabine, and tenofovir alafenamide in adolescents and children with HIV: week 48 results of a single-arm, open-label, multicentre, phase 2/3 trial. Lancet Child Adolesc Health 2021; 5: 642 - 51.
304. Федеральный закон от 21 ноября 2011 г. N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации" (с изменениями и дополнениями от 02.07.2021).
305. Приказ Министерства здравоохранения Российской Федерации от 23 октября 2019 года N 878н "Об утверждении Порядка организации медицинской реабилитации детей".
306. Афонина Л.Ю., Слепцов А.И., Орлова А.А. и др. ВИЧ-ассоциированные состояния у детей: актуальные вопросы в клинической практике./Актуальные вопросы ВИЧ-инфекции. Охрана здоровья матери и ребенка: материалы международной научно-практической конференции. - СПб: Человек и здоровье, 2021. - С. 15 - 39.
307. Panel on Treatment of HIV During Pregnancy and Prevention of Perinatal Transmission. Recommendations for the Use of Antiretroviral Drugs During Pregnancy and Interventions to Reduce Perinatal HIV Transmission in the United States. Department of Health and Human Services. Available at https://clinicalinfo.hiv.gov/en/guidelines/perinatal.Accessed20.02.2024.
308. Branson B.M., Handsfield H.H., Lampe M.A., et al. Revised recommendations for HIV testing of adults, adolescents, and pregnant women in health-care settings. MMWR Recomm Rep. 2006; 55 (RR-14): 1 - 17; quiz CE11-14. Available at: http://www.ncbi.nlm.nih.gov/pubm.19.
309. Chou R., Cantor A.G., Zakher B., Bougatsos C. Screening for HIV in pregnant women: systematic review to update the 2005 U.S. Preventive services task force recommendation. Ann Intern Med. 2012; 157(10): 719 - 728.
310. Приказ Министерства здравоохранения РФ от 1 ноября 2012 г. N 572н "Об утверждении Порядка оказания медицинской помощи по профилю "акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)."
311. Lilian R.R., Kalk E., Bhowan K., et al. Early diagnosis of in utero and intrapartum HIV infection in infants prior to 6 weeks of age. J Clin Microbiol. 2012; 50(7): 2373 - 2377.
312. Sanmarti M.,  L., Huertas S., Badenes D., Dalmau D., Slevin M., Krupinski J., Popa-Wagner A., Jaen A. HIV-associated neurocognitive disorders. Review. Journal of Molecular Psychiatry 2014, 2: 2.
L., Huertas S., Badenes D., Dalmau D., Slevin M., Krupinski J., Popa-Wagner A., Jaen A. HIV-associated neurocognitive disorders. Review. Journal of Molecular Psychiatry 2014, 2: 2.
313. Phillips N., Amos T., Kuo C., Hoare J., Ipser J., Thomas K.G.F., Stein D.J. HIV-Associated Cognitive Impairment in Perinatally Infected Children: A Meta-analysis. Pediatrics. 2016; 138(5): e20160893.
314. Sturdevant C.B., Dow A., Jabara C.B., Joseph S.B., Schnell G., Takamune N. et al. (2012) Central Nervous System Compartmentalization of HIV-1 Subtype C Variants Early and Late in Infection in Young Children. PLoS Pathog 8(12): e1003094.
315. Henderson L.J., Reoma L.B., Kovacs J.A., Nath A. 2020. Advances toward curing HIV-1 infection in tissue reservoirs. J Virol 94: e00375-19.
316. Scutari R., Alteri C., Perno C.F., Svicher V., Aquaro S. The Role of HIV Infection in Neurologic Injury. Review. Brain Sci. 2017, 7, 38.
317. Thakur K.T., Boubour A., Saylor D., et al. Global HIV neurology: a comprehensive review. AIDS 2019, Vol 33 No 2: 163 - 184.
318. Connor E.M., Sperling R.S., Gelber R., Kiselev P., Scott G., O"Sullivan M.J., VanDyke R., Bey M., Shearer W., Jacobson R.L. et al. Reduction of maternal-infant transmission of human immunodeficiency virus type 1 with zidovudine treatment. Pediatric AIDS Clinical Trials Group Protocol 076 Study Group. N Engl J Med. 1994 Nov 3; 331(18): 1173 - 80.
319. Ferguson W., Goode M., Walsh A., Gavin P., Butler K. Evaluation of 4 Weeks" Neonatal Antiretroviral Prophylaxis as a Component of a Prevention of Mother-to-child Transmission Program in a Resource-rich Setting. The Pediatric Infectious Disease Journal 30(5): p 408 - 412, May 2011.
320. Mohammadi P., Desfarges S., Bartha I., Joos B., Zangger N., et al. (2013) 24 Hours in the Life of HIV-1 in a T Cell Line. PLoS Pathog 9(1): e1003161.
321. Persaud D., Chadwick E., Tierney C., et al. Virologic response to very early ART in neonates with in utero HIV: IMPAACT P115. Abstract 799. Presented at: Conference on Retroviruses and Opportunistic Infections. 2019. Seattle, Washington.
322. Persaud D., Bryson Y., Nelson B.S., Tierney C., Cotton M.F., Coletti A. et al. HIV-1 reservoir size after neonatal antiretroviral therapy and the potential to evaluate antiretroviral-therapy-free remission (IMPAACT P1115): a phase 1/2 proof-of-concept study. Lancet HIV. 2024 Jan; 11(1): e20 - e30.
323. Nielsen-Saines K., Watts H.D., Veloso V.G., Bryson Y.J., Joao E.C., Pilotto J.H. et al. for the NICHD HPTN 040/PACTG 1043 Protocol Team. Three Postpartum Antiretroviral Regimens to Prevent Intrapartum HIV Infection. N Engl J Med 2012; 366: 2368 - 79.
324. Fowler M.G., Qin M., Fiscus S.A., et al. Benefits and risks of antiretroviral therapy for perinatal HIV prevention. N Engl J Med. 2016; 375(18): 1726 - 1737.
325. Gulia J., Kumwenda N., Li Q., Taha T.E. HIV Seroreversion Time in HIV-1-Uninfected Children Born to HIV-1-Infected Mothers in Malawi. J Acquir Immune Defic Syndr 2007; 46: 332 - 337.
326. Sohn A.H., Thanh T.C., Thinh le Q. et al. Failure of human immunodeficiency virus enzyme immunoassay to rule out infection among polymerase chain reaction-negative Vietnamese infants at 12 months of age. Pediatr Infect Dis J. 2009; 28(4): 273 - 276.
327. Shiau S., Strehlau R., Technau K.-G., Patel F., Arpadi S.M., Coovadia A., Abrams E.J., Kuhn L. Early age at start of antiretroviral therapy associated with better virologic control after initial suppression in HIV-infected infants. AIDS. 2017 Jan 28; 31(3): 355 - 364
328. Massanella M., Puthanakit T., Leyre L., Jupimai T., Sawangsinth P. et al.; RV474/HIVNAT194 and RV475/HIVNAT 209 Study Groups. Continuous Prophylactic Antiretrovirals/Antiretroviral Therapy Since Birth Reduces Seeding and Persistence of the Viral Reservoir in Children Vertically Infected With Human Immunodeficiency Virus. Clin Infect Dis. 2021 Aug 2; 73(3): 427 - 438.
329. Rinaldi S., Pallikkuth S., Cameron M., et al. Impact of early antiretroviral therapy initiation on HIV-specific CD4 and CD8 T cell function in perinatally infected children. J Immunol. 2020; 204(3): 540 - 549.
330. Azzoni L., Barbour R., Papasavvas E., et al. Early ART results in greater immune reconstitution benefits in HIV-infected infants: working with data missingness in a longitudinal dataset. PLoS One. 2015; 10(12): e0145320.
331. Tarancon-Diez L., Rull A., Herrero P., et al. Early antiretroviral therapy initiation effect on metabolic profile in vertically HIV-1-infected children. J Antimicrob Chemother. 2021; 76(11): 2993 - 3001.
332. Dobe I.S., Mocumbi A.O., Majid N., Ayele B., Browne S.H., Innes S. Earlier antiretroviral initiation is independently associated with better arterial stiffness in children living with perinatally acquired HIV with sustained viral suppression in Mozambique. South Afr J HIV Med. 2021; 22(1): 1282.
333. Iyun V., Technau K.G., Eley B., et al. Earlier antiretroviral therapy initiation and decreasing mortality among HIV-infected infants initiating antiretroviral therapy within 3 months of age in South Africa, 2006 - 2017. Pediatr Infect Dis J. 2020; 39(2): 127 - 133.
334. Jantarabenjakul W., Chonchaiya W., Puthanakit T., et al. Low risk of neurodevelopmental impairment among perinatally acquired HIV-infected preschool children who received early antiretroviral treatment in Thailand. J Int AIDS Soc. 2019; 22(4): e25278.
335. Laughton B., Cornell M., Grove D., et al. Early antiretroviral therapy improves neurodevelopmental outcomes in infants. AIDS. 2012; 26(13): 1685 - 1690.
336. Laughton B., Naidoo S., Dobbels E., et al. Neurodevelopment at 11 months after starting antiretroviral therapy within 3 weeks of life. South Afr J HIV Med. 2019; 20(1): 1008
337. Payne H., Mkhize N., Otwombe K., et al. Reactivity of routine HIV antibody tests in children who initiated antiretroviral therapy in early infancy as part of the children with HIV early antiretroviral therapy (CHER) trial: a retrospective analysis. Lancet Infect Dis. 2015; 15(7): 803 - 809
338. Kuhn L., Schramm D.B., Shiau S., et al. Young age at start of antiretroviral therapy and negative HIV antibody results in HIV-infected children when suppressed. AIDS. 2015; 29(9): 1053 - 1060.
339. Dominguez-Rodriguez S., Tagarro A., Palma P., et al. Reduced time to suppression among neonates with HIV initiating antiretroviral therapy within 7 days after birth. J Acquir Immune Defic Syndr. 2019; 82(5): 483 - 490.
340. Foster C., Dominguez-Rodriguez S., Tagarro A., et al. The CARMA study: early infant antiretroviral therapy-timing impacts on total HIV-1 DNA quantitation 12 years later. J Pediatric Infect Dis Soc. 2021; 10(3): 295 - 301.
341. Mirochnick M., Stek A., Acevedo M., et al. Safety and pharmacokinetics of nelfinavir coadministered with zidovudine and lamivudine in infants during the first 6 weeks of life. J Acquir Immune Defic Syndr. 2005; 39(2): 189 - 194.
342. Tremoulet A.H., Capparelli E.V., Patel P., et al. Population pharmacokinetics of lamivudine in human immunodeficiency virus-exposed and -infected infants. Antimicrob Agents Chemother. 2007; 51(12): 4297 - 4302.
343. Tremoulet A.H., Nikanjam M., Cressey T.R., et al. Developmental pharmacokinetic changes of lamivudine in infants and children. J Clin Pharmacol. 2012; 52(12): 1824 - 1832.
344. Mirochnick M., Nielsen-Saines K., Pilotto J.H., et al. Nelfinavir and Lamivudine pharmacokinetics during the first two weeks of life. Pediatr Infect Dis J. 2011; 30(9): 769 - 772.
345. Bouazza N., Hirt D., Blanche S., et al. Developmental pharmacokinetics of lamivudine in 580 pediatric patients ranging from neonates to adolescents. Antimicrob Agents Chemother. 2011; 55(7): 3498 - 3504.
346. World Health Organization. Preferred antiretroviral medicines for treating and preventing HIV infection in younger children: Report of the WHO paediatric antiretroviral working group. 2008.
347. Cressey T.R., Bekker A., Cababasay M., et al. Abacavir safety and pharmacokinetics in normal and low birth weight infants with HIV. Abstract #843. Presented at: Conference on Retroviruses and Opportunistic Infections; 2020. Boston, MA.
348. Bekker A., Decloedt E.H., Slade G., Cotton M.F., Rabie H., Cressey T.R.. Single dose abacavir pharmacokinetics and safety in neonates exposed to human immunodeficiency virus (HIV). Clin Infect Dis. 2021; 72(11): 2032 - 2034.
349. Bekker A., Capparelli E.V., Violari A., et al. Abacavir dosing in neonates from birth: a phramcokinetic analysis. Presented at: Conference on Retroviruses and Opportunistic Infections; 2021. Virtual Conference. Available at: https://www.croiconference.org/abstract/abacavir-dosing-in-neonates-from-birth-a-pharmacokinetic-analysis/.
350. Crichton S., Collins I.J., Turkova A., et al. Abacavir dosing, effectivness, and safety in young infants living with HIV in Europe. Abstract #844. Presented at: Conference on Retroviruses and Opportunistic Infections 2020. Boston, MA Available at: https://www.croiconference.org/abstract/abacavir-dosing-effectiveness-and-safety-in-young-infants-living-with-hiv-in-europe/.
351. De Waal R., Rabie H., Technau K., et al. Abacavir safety and efficacy in young infants in South African observational cohort. Abstract #845. Presented at: Conference on retroviruses and opportunistic infections 2020. Boston, MA Available at: https://www.croiconference.org/abstract/abacavir-safety-and-efficacy-in-young-infants-in-south-african-observational-cohorts/.
352. Bekker A., Capparelli E.V., Violari A., et al. Abacavir dosing in neonates from birth to 3 months of life: a population pharmacokinetic modelling and simulation study. Lancet HIV. 2022; 9(1): e24 - e31.
353. Jesson J., Saint-Lary L., Revegue M., et al. Safety and efficacy of abacavir for treating infants, children, and adolescents living with HIV: a systematic review and meta-analysis. Lancet Child Adolesc Health. 2022; 6(10): 692 - 704.
354. Drug label Inforation Zidovudine FDA Approved. 019655Orig1s059,019910Orig1s046,019951Orig1s037lbl.pdf (fda.gov), DailyMed - RETROVIR-zidovudine capsule RETROVIR-zidovudine solution RETROVIR-zidovudine injection, solution (nih.gov).
355. Capparelli E.V., Mirochnick M., Dankner W.M., et al. Pharmacokinetics and tolerance of zidovudine in preterm infants. J Pediatr. 2003; 142(1): 47 - 52.
356. Kinai E., Kato S., Hosokawa S., et al. High plasma concentrations of zidovudine (AZT) do not parallel intracellular concentrations of AZT-triphosphates in infants during prevention of mother-to-child HIV-1 transmission. J Acquir Immune Defic Syndr. 2016; 72(3): 246 - 253.
357. Maswabi K., Ajibola G., Bennett K., et al. Safety and Efficacy of Starting Antiretroviral Therapy in the First Week of Life. Clin Infect Dis. 2021; 72(3): 388 - 393.
358. Anugulruengkitt S., Suntarattiwong P., Ounchanum P., et al. Safety of 6-week neonatal triple-combination antiretroviral postexposure prophylaxis in high-risk HIV-exposed infants. Pediatr Infect Dis J. 2019; 38(10): 1045 - 1050.
359. Kakkar F.W., Samson L., Vaudry W., et al. Safety of combination antiretroviral prophylaxis in high-risk HIV-exposed newborns: a retrospective review of the Canadian experience. J Int AIDS Soc. 2016; 19(1): 20520.
360. Raffe S.F., Savage C., Perry L.A., Patel A., Keith T., Howell R., et al. The management of HIV in pregnancy: A 10-year experience. European Journal of Obstetrics, Gynecology, & Reproductive Biology. 2017; 210: 310 - 3.
361. Illan R.M., Soto Sanchez B., Mazariegos Orellana D., et al. Safety and experience with combined antiretroviral prophylaxis in newborn at high-risk of perinatal HIV infection, in a cohort of mother living with HIV-infant pairs. Pediatr Infect Dis J. 2021; 40(12): 1096 - 1100.
362. Clarke D.F., Penazzato M., Capparelli E., et al. Prevention and treatment of HIV infection in neonates: evidence base for existing WHO dosing recommendations and implementation considerations. Expert Rev Clin Pharmacol. 2018; 11(1): 83 - 93.
363. Ruel T.D., Capparelli E.V., Tierney C., et al. Pharmacokinetics and safety of early nevirapine-based antiretroviral therapy for neonates at high risk for perinatal HIV infection: a phase 1/2 proof of concept study. Lancet HIV. 2021; 8(3): e149 - e157.
364. Lau E., Brophy J., Samson L., et al. Nevirapine pharmacokinetics and safety in neonates receiving combination antiretroviral therapy for prevention of vertical HIV transmission. J Acquir Immune Defic Syndr. 2017; 74(5): 493 - 498.
365. Cressey T.R., Punyawudho B., Le Coeur S., et al. Assessment of nevirapine prophylactic and therapeutic dosing regimens for neonates. J Acquir Immune Defic Syndr. 2017; 75(5): 554 - 560.
366. Kumwenda N.I., Hoover D.R., Mofenson L.M., et al. Extended antiretroviral prophylaxis to reduce breast-milk HIV-1 transmission. N Engl J Med. 2008; 359(2): 119 - 129.
367. Coovadia H., Brown E., Maldonado Y., et al. Efficacy of extended daily infant nevirapine (NVP) through age 6 months compared to 6 weeks for prevention of postnatal mother-to-child transmission (MTCT) of HIV through breastfeeding (BF). Presented at: 18th Conference on Retroviruses and Opportunistic Infections. 2011. Boston, MA.
368. Wade N.A., Birkhead G.S., Warren B.L., et al. Abbreviated regimens of zidovudine prophylaxis and perinatal transmission of the human immunodeficiency virus. N Engl J Med. 1998; 339(20): 1409 - 1414.
369. Van Rompay K.K.A., Otsyula M.G., Marthas M.L., Miller C.J., McChesney M.B., Pedersen N.C. Immediate zidovudine treatment protects simian immunodeficiency virus-infected newborn macaques against rapid onset of AIDS. Antimicrob Agents Chemother. 1995; 39(1): 125 - 131.
370. Beste S., Essajee S., Siberry G., Hannaford A., Dara J., Sugandhi N., et al. Optimal Anti-Retroviral Prophylaxis in Infants At High-Risk of Acquiring Human Immunodeficiency Virus: A Systematic Review. Pediatr Infect Dis J. 2018; 37(2): 169 - 75.
371. Koay W.L.A., Zhang J., Manepalli K.V., Griffith C.J., Castel A.D., Scott R.K., Ferrer K.T., Rakhmanina N.Y., Prevention of Perinatal HIV Transmission in an Area of High HIV Prevalence in the United States, The Journal of Pediatrics, vol. 228, P 101 - 109 January 2021.
372. Centers for Disease Control and Prevention, Dominguez K.L., Smith D.K., Thomas V., Crepaz N., Lang K., et al. Updated guidelines for antiretroviral postexposure prophylaxis after sexual, injection drug use, or other nonoccupational exposure to HIV - United States, 2016, update 2018.
373. Guidelines on post-exposure prophylaxis for HIV and the use of co-trimoxazole prophylaxis for HIV-related infections among adults, adolescents and children: recommendations for a public health approach. WHO, December 2014 supplement to the 2013 consolidated guidelines on the use of antiretroviral drugs for treating and preventing HIV infection.
374. Penazzato M., Dominguez K., Cotton M., Barlow-Mosha L., Ford N. Choice of antiretroviral drugs for postexposure prophylaxis for children: A systematic review. Clinical Infectious Diseases. 2015; 60 Suppl 3: S177 - 81.
375. BC Centre for Excellence in HIV/AIDS PEP Guidelines Committee. HIV post-exposure prophylaxis (PEP).
376. Rapid Response Service. The efficacy of post-exposure prophylaxis (PEP) for HIV. Toronto, ON: Ontario HIV Treatment Network; March 2019.
377. Blokhuis C., Kootstra N.A., Caan M.WA., Pajkrt D. Neurodevelopmental delay in pediatric HIV/AIDS: current perspectives. Review. Neurobehavioral HIV Medicine 2016:7, 1 - 13.
378. Smith L., Adnams C., Eley Brian. Neurological and neurocognitive function of HIV-infected children commenced on antiretroviral therapy. SAJCH October 2008 vol. 2 no. 3.
379. van Arnhem L.A., Bunders M.J., Scherpbier H.J. et al. Neurologic Abnormalities in HIV-1 Infected Children in the Era of Combination Antiretroviral Therapy. (2013) PLoS ONE 8(5): e64398.
380. Dewi M.M., Alam A., Risan N.A. Risk Factor of Human Immunodeficiency virus Encephalopathy in Children. American Journal of Clinical Medicine Research. 2019, 7(1), 18 - 25. DOI: 10.12691/ajcmr-7-1-4
381. Donald K.A., Walker K.G., Kilborn T. et al. HIV Encephalopathy: pediatric case series description and insights from the clinic coalface. AIDS Research and Therapy (2015) 12: 2.
382. van Opstal S.E.M., Wagener M.N., Miedema H.S. et al. (2021) School functioning of children with perinatal HIV-infection in high-income countries: A systematic review. PLoS ONE 16(6): e0252746.
383. Donald K.A., Hoare J., Eley B., Wilmshurst J.M. Neurologic Complications of Pediatric Human Immunodeficiency Virus: Implications for Clinical Practice and Management Challenges in the African Setting. Semin Pediatr Neurol 21: 3 - 11, 2014.
384. Wilmshurst J.M., Donald K.A., Eley B. Update on the key developments of the neurologic complications in children infected with HIV. Curr Opin HIV AIDS 2014; 9: 533 - 538
385. Cohen S., Ter Stege J.A., Geurtsen G.J., et al. Poorer cognitive performance in perinatally HIV-infected children versus healthy socioeconomically matched controls. Clin Infect Dis. 2015; 60 (7): 1111 - 1119.
386. Cohen S., Caan M.W.A., Mutsaerts H.-J. et al. Cerebral injury in perinatally HIV-infected children compared to matched healthy controls. Neurology 2016; 86: 1 - 9.
387. Crowell C.S., Malee K.M., Yogev R., Muller W.J. Neurologic disease in HIV-infected children and the impact of combination antiretroviral therapy. Rev Med Virol. 2014; 24(5): 316 - 331.
388. Crowell C.S., Huo Y., Tassiopoulos K., et al. for the PACTG 219C Study Team and the Pediatric HIV/AIDS Cohort Study (PHACS). Early viral suppression improves neurocognitive outcomes in HIV-infected children. AIDS 2015, 29: 295 - 304.
389. Smith A.B., Smirniotopoulos J.G., Rushing E.J. Central Nervous System Infections Associated with Human Immunodeficiency Virus Infection: Radiologic-Pathologic Correlation. RadioGraphics 2008; 28: 2033 - 2058.
390. Epstein L.G. Sharer L.R., Goudsmit J. Neurological and Neuropathological Features of Human Immunodeficiency Virus Infection in Children. Ann Neurol. 1988; 23 (Suppl): S19 - 23.
391. Smith Fawzi M.C., Eustache E., Oswald C. et al. Psychosocial Functioning Among HIV-Affected Youth and Their Caregivers in Haiti: Implications for Family-Focused Service Provision in High HIV Burden Settings. AIDS Patient care and STDs. Volume 24, Number 3, 2010. Mary Ann Liebert, Inc.
392. Okoromah C.A.N., Ojo O.O., Ogunkunle O.O. Cardiovascular Dysfunction in HIV-infected Children in a Sub-Saharan African Country: Comparative Cross-sectional Observational Study. Journal of Tropical Pediatrics, vol. 58, no. 1, 2012.
393. Lipshultz S.E., Williams P.L. Wilkinson J.D. et al. for the Pediatric HIV/AIDS Cohort Study (PHACS). Cardiac Status of HIV-Infected Children Treated With Long-Term Combination Antiretroviral Therapy: Results from the Adolescent Master Protocol of the NIH Multicenter Pediatric HIV/AIDS Cohort Study: Lipshultz: Cardiac status of children with HIV infection in the HAART era. JAMA Pediatr. 2013 June; 167(6): 520 - 527.
394. Badal S., Gupta R., Kumar P., Sharma M, Chhajta D.S. Cardiac manifesta-tions in HIV infected children. Are they under diagnosed? HIV/AIDS Res Treat Open J. 2015; 2(1): 21 - 26. doi: 10.17140/HARTOJ-2-103.
395. Lipshultz S.E., Wilkinson J.D., Thompson B. et al. for the CHAART 2 Investigator Group. Cardiac Effects of Highly Active Antiretroviral Therapy in Perinatally HIV-infected Children: The CHAART 2 Study. J Am Coll Cardiol. 2017 October 31; 70(18): 2240 - 2247.
396. McCrary A.W., Nyandiko W., Ellis A.M. et al. Early Cardiac Dysfunction in Children and Young Adults with Perinatally Acquired HIV. AIDS. 2020 March 15; 34(4): 539 - 548.
397. Mahtab S., Zar H.J., Ntusi N.A.B. et al. Endothelial Dysfunction in South African Youth Living With Perinatally Acquired Human Immunodeficiency Virus on Antiretroviral Therapy. Clinical Infectious Diseases, 2020; 71(10): e672-9.
398. Mahtab S., Lawrenson J., Jamieson-Luff N. et al. Echocardiographic Findings in a Cohort of Perinatally HIV-Infected Adolescents Compared with Uninfected Peers from the Cape Town Adolescent Antiretroviral Cohort. Clinical Investigation echocardiography and HIV-infections, vol. 33, issue 5, p604 - 611, May 01, 2020.
399. Tewolde Wubayehu, Workeabeba Abebe, Endale Tefera. Echocardiographic abnormalities in children and adolescents living with human immunodeficiency virus on highly active antiretroviral treatment. Cardiovasc J Afr 2020; 31: 236 - 240.
400. Majonga E.D., Chiesa S.T., McHugh G., et al. Carotid intima media thickness in older children and adolescents with HIV taking antiretroviral therapy. Medicine 2020; 99: 17 (e19554).
401. Aliyannissa A., Kuswiyanto R.B., Setiabudi D. et al. Sekarwana Correlation between CD4 count and glomerular filtration rate or urine protein:creatinine ratio in human immunodeficiency virus-infected children Correlation between CD4 count and glomerular filtration rate or urine protein:creatinine ratio in human immunodeficiency virus-infected children. Kidney Res Clin Pract Published online March 9, 2020 pISSN: 2211 - 9132; eISSN: 2211 - 9140
402. Esezobor C.I., Iroha E., Oladipo O. et al. Kidney function of HIV-infected children in Lagos, Nigeria: using Filler"s serum cystatin C-based formula. JIAS 13, 17 (2010).
403. Bk K., Tiwari S., Chhapola V. et al. Brief Report: Subclinical Kidney Dysfunction in HIV-Infected Children: A Cross-Sectional Study. J Acquir Immune Defic Syndr. 2020 Dec 1; 85(4): 470 - 474.
404. MacBraynea C.E., Rutsteinb R.M., Wizniac A.A. et al. the IMPAACT P1090 Protocol Team. Etravirine in treatment-experienced HIV-1-infected children 1 year to less than 6 years of age Etravirine in treatment-experienced HIV-1-infected children 1 year to less than 6 years of age. AIDS 2021, 35: 1413 - 1421
405. Natukunda E., Gaur A.H., Kosalaraksa P. et al. Safety, efficacy, and pharmacokinetics of single-tablet elvitegravir, cobicistat, emtricitabine, and tenofovir alafenamide in virologically suppressed, HIV-infected children: a single-arm, open-label trial. Lancet Child Adolesc Health 2017; 1: 27 - 34
406. Stevens M., Kirsh, B., Nixon S.A. (2013). Rehabilitation interventions for children living with HIV: a scoping review. Disability and Rehabilitation, 36(10), 865 - 874.
407. Devendra A., Makawa A., Kazembe P.N., Calles N.R., Kuper H. (2013) HIV and Childhood Disability: A Case-Controlled Study at a Paediatric Antiretroviral Therapy Centre in Lilongwe, Malawi. PLoS ONE 8(12): e84024
408. Siegfried N., van der Merwe L., Brocklehurst P., Sint T.T. Antiretrovirals for reducing the risk of mother-to-child transmission of HIV infection. Cochrane Database of Systematic Reviews 2011, Issue 7. Art. No.: CD003510. DOI: 10.1002/14651858.CD003510.pub3
409. Siedler K., Skopnik H. Oseltamivir for Treatment of Influenza in Infants Less Than One Year: A Retrospective Analysis. The Pediatric Infectious Disease Journal 29(6): p 495 - 498, June 2010.
410. Santos G.M.A., Locatelli I.,  M. et al. for the Neurocognitive Assessment in the Metabolic and Aging Cohort (NAMACO) Study Group. Cross-Sectional and Cumulative Longitudinal Central Nervous System Penetration Effectiveness Scores Are Not Associated With Neurocognitive Impairment in a Well Treated Aging Human Immunodeficiency Virus-Positive Population in Switzerland. Open Forum Infectious Diseases, July 2019.
M. et al. for the Neurocognitive Assessment in the Metabolic and Aging Cohort (NAMACO) Study Group. Cross-Sectional and Cumulative Longitudinal Central Nervous System Penetration Effectiveness Scores Are Not Associated With Neurocognitive Impairment in a Well Treated Aging Human Immunodeficiency Virus-Positive Population in Switzerland. Open Forum Infectious Diseases, July 2019.
411. Nwogu J.N., Ma Q., Babalola C.P. et al. Pharmacokinetic, Pharmacogenetic, and Other Factors Influencing CNS Penetration of Antiretrovirals. Review Article. AIDS Research and Treatment Volume 2016, Article ID 2587094, 13 pages.
412. Кравченко А.В., Галегов Г.А., Канестри В.Г. Фосфазид: [монография]/А.В. Кравченко, Г.А. Галегов, В.Г. Канестри. - Москва: Медпрактика-М, 2017. - 207 с.
413. Nachman S., Zheng N., Acosta E.P. et al. Pharmacokinetics, safety, and 48-week efficacy of oral raltegravir in HIV-1-infected children aged 2 through 18 years. Clin Infect Dis. 2014; 58(3): 413 - 422.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
|
ФКУ "Республиканская клиническая инфекционная больница" Минздрава России - "Научно-практический центр профилактики и лечения ВИЧ-инфекции у беременных женщин и детей" Минздрава России:
|
|
|
Воронин Евгений Евгеньевич <*>
|
руководитель рабочей группы, главный врач ФКУ РКИБ Минздрава России, профессор кафедры инфекционных болезней Северо-Западного государственного медицинского университета им. И.И. Мечникова МЗ РФ, главный детский внештатный специалист по ВИЧ-инфекции МЗ РФ, д.м.н., профессор
|
|
Афонина Лариса Юрьевна <*>
|
ведущий специалист по ВИЧ/СПИД ФКУ РКИБ" Минздрава России, доцент кафедры инфекционных болезней Северо-Западного государственного медицинского университета им. И.И. Мечникова МЗ РФ, к.м.н.
|
|
Розенберг Владимир Яковлевич <*>
|
заместитель главного врача по медицинской части ФКУ РКИБ" Минздрава России, доцент кафедры социально значимых инфекций и фтизиопульмонологии Первого Санкт-Петербургского государственного медицинского университета им. И.П. Павлова, к.м.н.
|
|
Латышева Инга Борисовна <*>
|
заместитель главного врача по организационно-методической работе ФКУ РКИБ" Минздрава России, главный внештатный детский специалист по ВИЧ-инфекции Ленинградской области. Главный внештатный детский специалист по ВИЧ-инфекции Северо-Западного Федерального округа.
|
|
Главные внештатные детские специалисты по ВИЧ-инфекции Федеральных округов РФ:
|
|
|
Бекетова Елена Владимировна <*>
|
ГБУ Ростовской области "Центр по профилактике и борьбе со СПИД", исполняющая обязанности главного врача. Главный внештатный детский специалист по ВИЧ-инфекции Ростовской области. Главный внештатный детский специалист по ВИЧ-инфекции Южного Федерального округа.
|
|
Кузнецова Анна Валерьевна <*>
|
ГКБУЗ "Центр по профилактике и борьбе со СПИДом и инфекционными заболеваниями" Хабаровского края, главный врач. Главный внештатный детский специалист по ВИЧ-инфекции Хабаровского края. Главный внештатный детский специалист по ВИЧ-инфекции Дальневосточного Федерального округа.
|
|
Плотникова Юлия Кимовна <*>
|
ГБУЗ "Иркутский областной центр по профилактике и борьбе со СПИД и инфекционными заболеваниями", главный врач. Главный внештатный детский специалист по ВИЧ-инфекции Иркутской области. Главный внештатный детский специалист по ВИЧ-инфекции Сибирского Федерального округа.
|
|
Тавасиева Валерия Эльбрусовна <*>
|
ГБУЗ "Республиканский центр по профилактике и борьбе со СПИД и инфекционными заболеваниями" Министерства здравоохранения Республики Северная Осетия - Алания, главный врач. Главный внештатный детский специалист по ВИЧ-инфекции Северо-Кавказского Федерального округа.
|
|
Главные внештатные детские специалисты по ВИЧ-инфекции субъектов РФ, руководители центров по профилактике и борьбе со СПИД и инфекционными заболеваниями
|
|
|
Каминский Григорий Дмитриевич
|
ГУЗ "Тульский областной центр по профилактике и борьбе со СПИД и инфекционными заболеваниями", главный врач. Главный внештатный детский специалист по ВИЧ-инфекции Тульской области.
|
|
Волова Людмила Юрьевна <*>
|
ГБУЗ "Ямало-Ненецкий окружной центр профилактики и борьбы со СПИД", главный врач, главный внештатный детский специалист по ВИЧ-инфекции Ямало-Ненецкого автономного округа.
|
|
Шевченко Валерий Владимирович
|
КГБУЗ "Алтайский краевой центр по профилактике и борьбе со СПИД и инфекционными заболеваниями", главный врач. Главный внештатный детский специалист по ВИЧ-инфекции Алтайского края.
|
--------------------------------
<*> является членом Национальной ассоциации специалистов по профилактике, диагностике и лечению ВИЧ-инфекции.
Конфликт интересов. Все члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов, о которых необходимо сообщить.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Клинические рекомендации разработаны с целью формирования единых организационных и методических подходов к диагностическим алгоритмам, ведению и лечению детей с ВИЧ-инфекцией на территории Российской Федерации.
Задачи Рекомендаций:
- внедрение современных научно обоснованных организационных алгоритмов диагностики ВИЧ-инфекции для раннего активного выявления и применение антиретровирусных препаратов с целью снижения смертности, улучшения качества и увеличения продолжительности детей с ВИЧ-инфекцией;
- расширение охвата диспансерным наблюдением и АРТ детей с ВИЧ-инфекцией, повышение ее эффективности и безопасности;
- предоставление данных о рекомендованных к использованию антиретровирусных препаратах и фармако-экономически обоснованных схемах АРТ, применяемых для лечения детей ВИЧ-инфекцией в Российской Федерации;
- формирование единого подхода к назначению приоритетных схем АРТ первого ряда для обеспечения максимальной терапевтической эффективности, высокого уровня приверженности пациентов при малой вероятности развития нежелательных явлений и резистентности возбудителя;
- введение единых критериев оценки эффективности проводимой АРТ;
- снижение уровня контагиозности больных, и как следствие, уменьшение риска распространения инфекции, активности эпидемического процесса ВИЧ-инфекции в Российской Федерации;
В Рекомендациях учтены требования и положения, предусмотренные Порядком оказания медицинской помощи при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции) и Стандартами оказания медицинской помощи детям при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции).
Клинические рекомендации по диагностике, наблюдению и лечению ВИЧ-инфекции у детей предназначены для руководителей и врачей центров по профилактике и борьбе со СПИДом, врачей-инфекционистов и педиатров, участвующих в системе оказания помощи ВИЧ-инфицированным пациентам, студентов, ординаторов, аспирантов и преподавателей государственных образовательных учреждений высшего и дополнительного профессионального образования.
Целевая аудитория данных клинических рекомендаций: специалисты, имеющие высшее медицинское образование по следующим специальностям:
1. Инфекционные болезни
2. Педиатрия
3. Неонатология
4. Общая врачебная практика (семейная медицина)
5. Акушерство и гинекология
6. Эпидемиология.
Клинические рекомендации могут использоваться при разработке учебно-методических комплексов для подготовки и повышения квалификации врачей.
Рекомендации обсуждены и одобрены членами Национальной ассоциации специалистов в области профилактики, лечения и диагностики ВИЧ-инфекции, рабочей группой Профильной комиссии по проблемам диагностики и лечения ВИЧ-инфекции Минздрава России.
Клинические рекомендации формулировались при консенсусе экспертов, имеющих клинический опыт в области ВИЧ-инфекции у детей. Доказательной базой для рекомендаций явились публикации, вошедшие в Кокрейновскую библиотеку, базы данных EMBASE, PUBMED и MEDLINE. Все рекомендации ранжированы в соответствии с международными критериями по уровню достоверности (доказательности) и настоятельности выполнения (убедительности) в зависимости от количества и качества исследований по данной проблеме.
Таблица 17. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|
1
|
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица 18. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД
|
Расшифровка
|
|
1
|
Систематический обзор РКИ с применением метаанализа
|
|
2
|
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа
|
|
3
|
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Таблица 19. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР
|
Расшифровка
|
|
A
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР, но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ
ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
1. Лечебные дозы АРВП у детей
(дозы АРВП для проведения курса АРТ у новорожденных с целью ППМР рассмотрены в разделе 5.1. Профилактика передачи ВИЧ-инфекции от матери ребенку)
Приведены АРВП, зарегистрированные на территории РФ, в соответствии с данными Государственного реестра лекарственных средств по состоянию на октябрь 2020 г.
Данные по дозированию АРВП представлены в соответствии с действующими инструкциями к препаратам, зарегистрированным на территории Российской Федерации, а также с учетом рекомендаций по дозированию АРВП у детей, утвержденных FDA и рекомендованных PENTA на основании результатов клинических исследований и опыта практического применения.
Перед назначением любого АРВП следует внимательно изучить приложенную к нему инструкцию.
Перерасчет доз у детей проводится при изменении массы тела на 10%.
ППТ следует высчитывать по формуле Мостеллера:
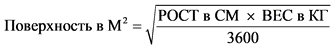
Таблица 20. Рекомендуемые лечебные дозы АРВП у детей и особенности их применения
|
Препарат, одобренный возраст применения, формы выпуска в РФ
|
Рекомендуемые дозы
|
Комментарии
|
|||
|
Нуклеозидные ингибиторы обратной транскриптазы (НИОТ)
|
|||||
|
Абакавир**
Abacavir (ABC)
Разрешен с >= 3 мес
Раствор для приема внутрь 20 мг/1 мл
Таб 150, 300, 600 мг
|
>= 3 мес < 25 кг
|
8 мг/кг
|
2
|
Тест на HLA-B*5701 перед назначением.
Хорошо переносится при округлении дозы в большую сторону.
Нет зависимости от приема пищи.
Можно крошить и смешивать в ложке еды или воды.
Детям от 3 мес до 1 г прием раствора рекомендуется 2 раза в сутки.
|
|
|
16 мг/кг
|
1
|
||||
|
>= 14 < 20 кг
|
150 мг
|
2
|
|||
|
300 мг
|
1
|
||||
|
>= 20 < 25 кг
|
150 мг (1/2 т) утр. и 300 мг (1 т) веч.
|
2
|
|||
|
450 мг (1 т + 1/2 т)
|
1
|
||||
|
>= 25 кг
|
300 мг
|
2
|
|||
|
600 мг
|
1
|
||||
|
> 8 мес
|
120 мг/м2
|
2
|
|||
|
Зидовудин**
Zidovudine (ZDV)
Разрешен с рождения
Раствор для приема внутрь 10 мг/1 мл
Таб 100, 300 мг
Капс 100, 200, 300 мг
|
#Недоношенные и доношенные <= 4 недель раствор пероральный:
|
Нет зависимости от приема пищи.
Парентерально 360 - 480 мг/м2 в сутки за 3 - 4 введения
|
|||
|
< 30 нед гестации
|
2 мг/кг с 0 до 4 нед,
3 мг/кг с 4 нед до 8 нед,
12 мг/кг с 8 нед
|
2
|
|||
|
30 - 35 нед гестации
|
2 мг/кг с 0 до 2 нед,
3 мг/кг с 2 нед до 6 нед,
12 мг/кг с 6 нед
|
2
|
|||
|
>= 35 нед гестации
|
4 мг/кг с 0 до 4 нед,
12 мг/кг с 4 нед
|
2
|
|||
|
#Доношенные > 4 недель, мг/м2:
|
|||||
|
< 30 кг
|
180 - 240 мг/м2
|
2
|
|||
|
Дозирование перорального раствора по массе тела:
|
|||||
|
>= 4 < 9 кг
|
12 мг/кг
|
2
|
|||
|
>= 9 < 30 кг
|
9 мг/кг
|
2
|
|||
|
>= 30 кг
|
300 мг
|
2
|
|||
|
Дозирование таблеток 100 и 300 мг:
|
|||||
|
>= 8 < 14 кг
|
100 мг
|
2
|
|||
|
>= 14 < 21 кг
|
100 мг утром (1 т 100 мг) и 200 мг вечером (2 т по 100 мг)
|
2
|
|||
|
>= 21 < 30 кг
|
200 мг (2 т по 100 мг)
|
2
|
|||
|
>= 30 кг
|
300 мг
|
2
|
|||
|
Ламивудин**
Lamivudine (3TC)
Разрешен с >= 3 мес
Раствор для приема внутрь 10 мг/1 мл
Таб 150, 300 мг
|
Дозирование сиропа:
|
Хорошо переносится при округлении дозы в большую сторону.
Нет зависимости от приема пищи.
Можно крошить и смешивать в ложке еды или воды.
Переход на 1-кратный прием ламивудина (сироп или таблетки) рекомендуется у детей старше 3х лет с неопределяемой ВН, стабильных клинически и иммунологически в течение более 36 недель [8].
|
|||
|
>= 3 мес < 1 г
|
5 мг/кг (0,5 мл/кг) (max 150 мг)
|
2
|
|||
|
Если невозможен прием 2 РС:
10 мг/кг (1,0 мл/кг) (max 300 мг)
|
1
|
||||
|
> 1 г < 25 кг
|
5 мг/кг (0,5 мл/кг) (max 150 мг)
|
2
|
|||
|
10 мг/кг (1,0 мл/кг) (max 300 мг)
|
1
|
||||
|
> 1 г > 25 кг
|
150 мг (15 мл)
|
2
|
|||
|
300 мг (30 мл)
|
1
|
||||
|
>= 3 лет
|
5 мг/кг (max 150 мг)
|
2
|
|||
|
10 мг/кг (max 300 мг)
|
1
|
||||
|
Дозирование у детей >= 14 кг, которые могут глотать таблетки:
|
|||||
|
>= 14 < 20 кг
|
75 мг (1/2 т)
|
2
|
|||
|
150 мг
|
1
|
||||
|
>= 20 < 25 кг
|
75 мг (1/2 т) утр. и 150 мг (1 т) веч.
|
2
|
|||
|
225 мг (1 т + 1/2 т)
|
1
|
||||
|
>= 25 кг
|
150 мг
|
2
|
|||
|
300 мг
|
1
|
||||
|
Тенофовир**
Tenofovir (TDF)
Разрешен с >= 12 лет >= 35 кг
Таб 150, 300 мг
|
>= 12 л >= 35 кг
|
300 мг
|
1
|
Принимать с пищей.
Не назначать с ATV без бустера.
|
|
|
Фосфазид** (Ф-АЗТ)
Phosphazide (pAZT)
Разрешен с >= 3 лет
Таб 200, 400 мг
|
3 - 13 лет
|
10 мг/кг за 2 - 3 приема
|
Прием перед едой.
Можно крошить для облегчения приема.
Таблетка хорошо растворяется в воде, что позволяет приготовить пероральный раствор для ребенка [11].
|
||
|
> 13 лет
|
200 мг
|
3
|
|||
|
При поражении ЦНС используется максимальная суточная доза 20 мг/кг, разделенная на 2 - 3 приема
|
|||||
|
Эмтрицитабин**
Emtricitabine (FTC)
Разрешен с >= 33 кг
Таб 200 мг
|
> 33 кг
|
200 мг
|
1
|
Капсулы и таблетки необходимо проглатывать целиком, не разжевывая.
Независимо от приемов пищи.
|
|
|
Ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ)
|
|||||
|
Невирапин**
Nevirapine (NVP)
Разрешен с рождения
Суспензия для приема внутрь 10 мг/1 мл
Таб 100, 200 мг
|
Дети < 16 лет И < 50 кг или ППТ <1,25 м2 - применять сироп:
|
При лечении NVP требуется вводная фаза сроком 14 дней в половинной суточной дозе за 1 прием. При хорошей переносимости (отсутствие сыпи и гиперферментемии) дозу увеличивают до терапевтической. В течение первых 3х месяцев лечения следует проводить тщательный контроль биохимических показателей (см. раздел VI. Диагностика ВИЧ-инфекции).
Нет зависимости от приема пищи.
|
|||
|
Расчет по ППТ (сироп):
|
|||||
|
< 16 лет
|
Вводная фаза - первые 14 дней лечения:
|
||||
|
150 мг/м2 (max 200 мг)
|
1
|
||||
|
Продолжать далее:
|
|||||
|
150 мг/м2 (max 200 мг)
|
2
|
||||
|
Расчет по массе тела (сироп):
|
|||||
|
< 8 лет
|
Вводная фаза - первые 14 дней лечения:
|
||||
|
4 мг/кг
|
1
|
||||
|
Продолжать далее:
|
|||||
|
7 мг/кг
|
2
|
||||
|
> 8 лет
|
Вводная фаза - первые 14 дней лечения:
|
||||
|
4 мг/кг
|
1
|
||||
|
Продолжать далее:
|
|||||
|
4 мг/кг
|
2
|
||||
|
>= 16 лет И >= 50 кг или >= 1,25 м2 (таблетки)
|
Вводная фаза - первые 14 дней лечения:
|
||||
|
200 мг
|
1
|
||||
|
Продолжать далее:
|
|||||
|
200 мг
|
2
|
||||
|
Рилпивирин
Rilpivirine (RPV)
Разрешен с >= 12 лет
Таб 25 мг
|
>= 12 лет
|
25 мг
|
1
|
Принимать во время еды.
Не рекомендуется назначать при ВН > 100 000 коп/мл
|
|
|
Этравирин**
Etravirine (ETR)
Разрешен с >= 2 лет >= 10 кг
Таб 25, 100, 200 мг
|
> 10 кг < 20 кг
|
100 мг
|
2
|
Прием после еды.
|
|
|
> 20 < 25 кг
|
125 мг
|
2
|
|||
|
>= 25 < 30 кг
|
150 мг
|
2
|
|||
|
>= 30 кг
|
200 мг
|
2
|
|||
|
Эфавиренз**
Efavirenz (EFV)
Разрешен с >= 3 лет >= 13 кг
Таб 100, 200, 300, 400, 600 мг
|
>= 13 < 15 кг
|
200 мг
|
1
|
Принимать перед сном, на голодный желудок. Жирная пища ускоряет абсорбцию, что может повлиять на развитие побочных эффектов.
|
|
|
>= 15 < 20 кг
|
250 мг
|
1
|
|||
|
>= 20 < 25 кг
|
300 мг
|
1
|
|||
|
>= 25 < 32,5 кг
|
350 мг
|
1
|
|||
|
>= 32,5 < 40 кг
|
400 мг
|
1
|
|||
|
>= 40 кг
|
600 мг
|
1
|
|||
|
Ингибиторы протеазы (ИП)
|
|||||
|
Атазанавир**
Atazanavir (ATV)
Разрешен с >= 6 лет >= 35 кг
Капс 150, 200, 300 мг
Таб ATV 300 мг/RTV 100 мг
|
Назначается вместе с бустером - ритонавиром (r):
|
Принимать с пищей.
Принимать за 2 часа до или через 1 час после приема ингибиторов протонного насоса или блокаторов H2-гистаминовых рецепторов.
|
|||
|
# >= 15 < 35 кг
|
# 200 мг + r 100 мг
|
1
|
|||
|
>= 35 кг
|
300 мг + r 100 мг
|
1
|
|||
|
Дарунавир**
Darunavir (DRV)
Разрешен с >= 6 лет >= 20 кг
Таб 75, 150, 300, 400, 600, 800 мг
|
Прием 2 РС у детей, получавших ранее АРТ [1]:
|
Назначается вместе с бустером - ритонавиром (r). Принимать с пищей.
Прием 1 РС возможен у детей с ВН < 100.000 коп/мл, CD4 >= 100 и отсутствием мутаций к DRV (V11I, V32I, L33F, I47V, I50V, I54M/L, T74P, L76V, I84V, L89V).
|
|||
|
>= 20 < 30 кг
|
375 мг + r 50 мг
|
2
|
|||
|
>= 30 < 40 кг
|
450 мг + r 60 мг
|
2
|
|||
|
>= 40 кг
|
600 мг + r 100 мг
|
2
|
|||
|
#Прием 1 РС у детей, не получавших АРТ, или у получавших АРТ при условиях, указанных в комментариях:
|
|||||
|
>= 15 < 30 кг
|
600 мг + r 100 мг
|
1
|
|||
|
>= 30 < 40 кг
|
675 мг + r 100 мг
|
1
|
|||
|
>= 40 кг
|
800 мг + r 100 мг
|
1
|
|||
|
Лопинавир+ритонавир ** Lopinavir/ritonavir (LPV/r)
Разрешен с >= 14 дней (42 недели гестации)
Раствор для приема внутрь 80/20 мг/1 мл
Таб 100/25, 200/50 мг
|
Расчет по LPV или r:
|
Сироп принимать во время еды.
Таблетки нельзя делить, жевать.
Расчет дозы по массе или ППТ.
|
|||
|
>= 14 дней < 6 мес
|
16/4 мг/кг
|
2
|
|||
|
300/75 мг/м2
|
2
|
||||
|
>= 6 мес < 18 лет < 40 кг
|
230/57,5 мг/м2
|
2
|
|||
|
< 15 кг
|
12/3 мг/кг
|
2
|
|||
|
>= 15 < 40 кг
|
10/2,5 мг/кг
|
2
|
|||
|
< 18 лет > 40 кг
|
400/100 мг
|
2
|
|||
|
Ритонавир**
Ritonavir (RTV, r)
Таб, капс 100 мг
|
Используется как бустер (усилитель) других ИП
|
См. рекомендации к другим ИП
|
|||
|
Фосампренавир**
Fosamprenavir (FPV)
Разрешен с >= 6 лет >= 39 кг
Таб 700 мг
|
Назначается вместе с бустером - ритонавиром (r):
|
Таблетки принимать с пищей.
|
|||
|
3 6 лет >= 39 кг
|
700 мг (1 т) + r 100 мг
|
2
|
|||
|
Ингибиторы интегразы (ИИ)
|
|||||
|
Долутегравир**
Dolutegravir (DTG)
Разрешен с >= 6 лет >= 20 кг
Таб 50 мг
|
>= 12 лет >= 20 кг
|
50 мг
|
1
|
Независимо от приема пищи
|
|
|
Ралтегравир**
Raltegravir (RAL)
Разрешен с >= 2 лет >= 7 кг
Таб 400 мг
Таб жевательные 25, 100 мг
|
Прием независимо от еды. Нельзя заменять жевательные таблетки на таблетки, покрытые пленочной оболочкой, и наоборот. Таблетки с оболочкой нельзя делить, жевать.
|
||||
|
Жевательные таблетки (< 12 лет):
|
Жевательные таблетки:
- max разовая доза 300 мг;
- фармакокинетика не изучена у детей > 12 лет
|
||||
|
>= 11 < 14 кг
|
75 мг (3 т 25 мг)
|
2
|
|||
|
>= 14 < 20 кг
|
100 мг (1 т 100 мг)
|
2
|
|||
|
>= 20 < 28 кг
|
150 мг (1 1/2 т 100 мг)
|
2
|
|||
|
>= 28 < 40 кг
|
200 мг (2 т 100 мг)
|
2
|
|||
|
>= 40 кг
|
300 мг (3 т 100 мг)
|
2
|
|||
|
Таблетки с пленочной оболочкой 400 мг:
|
Таблетки 400 мг:
- не использовать для приема 1 РС.
|
||||
|
>= 6 лет >= 25 кг
|
400 мг (1 т)
|
2
|
|||
|
АРВП с фиксированными комбинациями доз
|
|||||
|
Абакавир+Ламивудин**
Abacavir+Lamivudine (ABC+3TC)
Разрешен с >= 25 кг
Таб 600/300 мг
|
>= 25 кг
|
1 таблетка
|
1
|
Независимо от приема пищи.
Таблетки нельзя ломать, жевать.
|
|
|
Зидовудин+Ламивудин**
Zidovudine+Lamivudine (ZDV+3TC)
Разрешен с >= 14 кг
Таб 300/150 мг
|
>= 14 < 21 кг
|
1/2 т
|
2
|
Независимо от приема пищи.
Таблетки нельзя ломать, жевать.
|
|
|
>= 21 < 30 кг
|
2 РС: 1/2 т утром и 1 т вечером
|
||||
|
>= 30 кг
|
1 т
|
2
|
|||
|
Тенофовир+Эмтрицитабин
Tenofovir Disoproxil Fumarate+ Emtricitabine (TDF+FTC)
Разрешен с >= 12 лет >= 35 кг
Таб 300/200 мг
|
>= 12 лет >= 35 кг
|
1 таблетка
|
1
|
Независимо от приема пищи.
Таблетки нельзя ломать, жевать.
|
|
|
Абакавир+Зидовудин+Ламивудин**
Abacavir+Lamivudine+Zidovudine
(ABC+3TC+ZDV)
Разрешен с >= 12 лет >= 40 кг
Таб 600/300 мг
|
>= 12 лет >= 40 кг
|
1 таблетка
|
2
|
Независимо от приема пищи.
Таблетки нельзя ломать, жевать.
|
|
|
Рилпивирин+Тенофовир+Эмтрицитабин**
Rilpivirine+Tenofovir Disoproxil Fumarate+Emtricitabine (RPV+TDF+FTC)
Разрешен с >= 12 лет >= 35 кг
Таб 25/300/200 мг
|
>= 12 лет >= 35 кг
|
1 т
|
1
|
Режим в одной таблетке.
Не следует назначать при ВН > 100 000 коп/мл плазмы.
Не назначать при наличии мутаций к ННИОТ.
Принимать во время еды.
Таблетки нельзя ломать, жевать.
|
|
|
Кобицистат+Тенофовираалафенамид+Элвитегравир+
Эмтрицитабин**
Elvitegravir+Cobicistat+Tenofoviralafenamide+Emtricitabine (EVG+COBI+TAF+FTC)
Разрешен с >= 6 лет >= 25 кг
Таб 150/150/10/200 мг
|
>= 6 лет >= 25 кг
|
1 т
|
1
|
Режим в одной таблетке.
Не следует назначать при тяжелом поражении почек.
Таблетки нельзя ломать, жевать.
|
|
|
Биктегравир+Тенофовира алафенамид+Эмтрицитабин**
Bictegravir+Tenofoviralafenamide+Emtricitabine
(BIC+TAF+FTC)
Разрешен с >= 6 лет >= 25 кг
Таб 50/25/200 мг
|
>= 6 лет >= 25 кг
|
1 т
|
1
|
Независимо от приема пищи. Таблетки не рекомендуется разжевывать, измельчать или разламывать.
|
|
2. Оценка степени проникновения АРВП в ЦНС
Таблица 21. Шкала уровней проникновения АРВП в ЦНС [410, 411] <1>
|
Класс АРВП
|
Уровень проникновения в ЦНС <2>
|
|||
|
4
|
3
|
2
|
1
|
|
|
НИОТ
|
Зидовудин**
|
Абакавир**
Эмтрицитабин**
|
Ламивудин**
Диданозин**
|
Тенофовир**
|
|
ННИОТ
|
Невирапин**
|
Эфавиренз**
|
Рилпивирин** <3>
Этравирин**
|
|
|
ИП
|
Дарунавир**+Ритонавир**
Фосампренавир**+Ритонавир**
Лопинавир+Ритонавир**
|
Атазанавир**
Атазанавир**+Ритонавир**
Фосампренавир**
|
Ритонавир**
|
|
|
ИИ
|
Долутегравир**
|
Ралтегравир**
|
Элвитегравир** <4>
|
|
--------------------------------
Примечания: <1> приведены АРВП, указанные в данных клинических рекомендациях; <2> уровень 4 соответствует наиболее высокой степени проникновения, уровень 1 - наиболее низкой; <3> в составе комбинированного противовирусного препарата рилпивирин+тенофовир+эмтрицитабин**; <4> в составе комбинированного противовирусного препарата кобицистат+тенофовира алафенамид+элвитегравир+эмтрицитабин**
3. Диагностика ВИЧ-инфекции
Таблица 22. Рекомендуемые методы диагностики ВИЧ-инфекции у детей различных категорий
|
Категория
|
Возраст
|
Вид вскармливания
|
Выявление антител/антигена ВИЧ <1>
|
Выявление НК ВИЧ <2>
|
|
Дети матерей, ВИЧ-серопозитивных во время беременности и/или родов (или серо-статус матери неизвестен)
|
< 18 месяцев
|
Искусственное
с рождения
|
Не применяется для диагностики.
Используется для подтверждения элиминации материнских антител и снятия с диспансерного учета
|
Рекомендуется минимум 2 раза в декретированные сроки
|
|
Грудное
|
Не применяется для диагностики.
Используется для подтверждения элиминации материнских антител и снятия с диспансерного учета
|
Рекомендуется в течение всего периода грудного вскармливания и после его окончания в декретированные сроки
|
||
|
>= 18 месяцев
|
Искусственное
с рождения
|
Рекомендуется стандартный метод диагностики
|
Может быть использовано для ранней диагностики
|
|
|
Грудное
|
Рекомендуется стандартный метод диагностики в течение всего периода грудного вскармливания и после его окончания в декретированные сроки
|
|||
|
Дети матерей, ВИЧ-серонегативных на момент родов (ВИЧ-инфекция выявлена у матери или/и у отца после рождения ребенка)
|
Независимо
|
Искусственное
с рождения
|
Рекомендуется стандартный метод диагностики
|
Может быть использовано для ранней диагностики
|
|
Грудное
|
Рекомендуется стандартный метод диагностики в течение всего периода грудного вскармливания и после его окончания в декретированные сроки
|
|||
|
Дети с контактом по ВИЧ-инфекции, исключая перинатальный
|
Независимо
|
Независимо
|
Рекомендуется стандартный метод диагностики
|
Может быть использовано для ранней диагностики
|
--------------------------------
Примечания:
<1> - Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови; Определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови; Исследование уровня антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1/2 и антигена p24 (Human immunodeficiency virus HIV 1/2 + Agp24) в крови; Определение антигена p24 вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в крови
<2> - Молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1); Определение ДНК вируса иммунодефицита человека методом ПЦР, качественное исследование; Количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР
4. Наблюдение ребенка с ВИЧ-инфекцией
Таблица 23. График и объем обследования ВИЧ-инфицированного ребенка в процессе наблюдения, при назначении и проведении АРТ <1>
|
Процедура
|
Взятие на ДУ
|
Наблюдение (интервал, месяцев)
|
Начало АРТ <2>
|
На фоне АРТ (недели и месяцы от начала лечения)
|
||
|
4 - 8 н.
|
12 н.
|
В дальнейшем (интервал, месяцев) <3>
|
||||
|
Сбор анамнеза
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Физикальное обследование <4>
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Определение стадии заболевания
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Регистрация вторичных и сопутствующих заболеваний
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Рентгенография легких <5>
|
+
|
<**> или <5>
|
+
|
<**>
|
<**>
|
<**> или <5>
|
|
Диагностика туберкулеза
|
+
|
6 м.
|
+
|
<**>
|
<**>
|
6 м. и <**>
|
|
Ультразвуковое исследование органов брюшной полости (комплексное)
|
+
|
12 м.
|
<**>
|
<**>
|
<**>
|
<**>
|
|
Исследование CD4+лимфоцитов
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Вирусная нагрузка ВИЧ
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Общий (клинический) анализ крови развернутый
|
+
|
3 м.
|
+
|
+
|
+
|
3 м. и <**>
|
|
Анализ крови биохимический общетерапевтический <6>
|
+
|
3 м.
|
+
|
+
|
+
|
3 м.
|
|
Анализ крови по оценке нарушений липидного обмена биохимический
|
+
|
12 м.
|
+
|
-
|
-
|
12 м. и <**>
|
|
Исследование уровня креатинина в крови
Исследование уровня глюкозы в крови
Исследование уровня неорганического фосфора в крови
Исследование уровня общего кальция в крови
|
+
|
12 м.
|
+
|
-
|
-
|
12 м. и <**>
|
|
Общий (клинический) анализ мочи
|
+
|
6 м.
|
+
|
+
|
+
|
6 м. и <**>
|
|
Определение антител к вирусу гепатита C (Hepatitis C virus) в крови; определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови
|
+
|
12 м.
|
+
|
<**>
|
<**>
|
12 м. и <**>
|
|
Выявление аллели 5701 локуса B главного комплекса гистосовместимости человека (HLA B*5701)
|
+
|
-
|
-
|
-
|
-
|
-
|
|
Оценка НЯ
|
+
|
+
|
+
|
+
|
+
|
При каждом осмотре и обращении
|
|
Оценка сопутствующего лечения
|
+
|
+
|
+
|
+
|
+
|
При каждом осмотре и обращении
|
--------------------------------
Примечания:
<1> Осмотр детей до 1 года проводится ежемесячно (детей 1-го месяца жизни 1 раз в 10 дней). Обследование осуществляется участковым врачом-педиатром и специалистами детской поликлиники, а также в рамках специализированной медицинской помощи.
<2> Могут использоваться результаты исследований, полученных в декретированные сроки при диспансерном наблюдении до начала лечения
<3> Диспансерное наблюдение детей без иммунодефицита, в ремиссии на фоне АРТ и стабильной супрессией ВН ВИЧ более 2-х лет может осуществляться 1 раз в 6 месяцев
<4> Физикальное обследование с оценкой физического развития (масса тела, рост, индексы)
<5> Рентгенография проводится подросткам с ВИЧ-инфекцией с 15 лет 2 раза в год
<6> Исследование включает: анализ крови биохимический общетерапевтический, комплексы исследований для оценки степени печеночно-клеточной недостаточности, для оценки повреждения клеток печени (степень цитолиза), для оценки холестатического синдрома
<**> Исследование проводится при наличии показаний
5. Оценка эффективности и безопасности АРТ у детей
Таблица 24. Перечень минимальных требований клинико-лабораторной оценки эффективности и безопасности АРТ у детей
|
Сроки обследования
|
Мониторинг безопасности <1>
|
Мониторинг эффективности и приверженности
|
|
Перед началом АРТ
|
Анамнез и физикальное обследование, общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический <2>
|
Исследование CD4+ - лимфоцитов (% содержание и абсолютное количество), количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР, консультирование по вопросам приверженности АРТ
|
|
Через 2 недели от начала АРТ
|
Анамнез и физикальное обследование
|
Консультирование по вопросам приверженности АРТ
|
|
Через 4 - 8 недель от начала АРТ
|
Анамнез и физикальное обследование, общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический
|
Консультирование по вопросам приверженности АРТ, количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР
|
|
В дальнейшем - каждые 3 месяца до достижения неопределяемого уровня ВН и его поддержания в течение не менее 24 месяцев
|
Анамнез и физикальное обследование, общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический
|
Консультирование по вопросам приверженности АРТ, Исследование CD4+ - лимфоцитов (% содержание и абсолютное количество), количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР
|
|
В дальнейшем - каждые 6 месяцев <3>
|
Анамнез и физикальное обследование, общий (клинический) анализ крови развернутый, анализ крови биохимический общетерапевтический (в том числе оценка нарушений липидного обмена) <2>
|
Консультирование по вопросам приверженности АРТ, Исследование CD4+ - лимфоцитов (% содержание и абсолютное количество), количественное определение РНК вируса иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1) в плазме крови методом ПЦР
|
--------------------------------
Примечания
<1> у детей, получающих невирапин**, уровень сывороточных трансаминаз исследуется каждые 2 недели в первый месяц лечения, затем 1 раз в месяц в течение следующих 3-х месяцев, затем каждые 3 месяца
<2> оценку нарушений липидного обмена рекомендуется проводить каждые 12 месяцев от начала АРТ
<3> при наличии клинико-иммунологической эффективности АРТ (ВН < 50 копий/мл в течение не менее 96 недель, уровень CD4-лимфоцитов соответствует 1ой иммунной категории), высокой приверженности лечению и наблюдению
ОБРАЗЕЦ
6. Информированное согласие на проведение антиретровирусной терапии у ребенка с ВИЧ-инфекцией в возрасте до 15 лет
(подписывает законный представитель, осуществляющий уход за ребенком)
|
Я,
|
|
|
(Фамилия, Имя, Отчество полностью разборчиво, домашний адрес, телефон)
|
|
|
настоящим подтверждаю свое добровольное согласие на лечение моего ребенка
|
|
|
(Фамилия, Имя, Отчество полностью разборчиво)
|
|
|
(Дата рождения)
|
|
лекарственными препаратами, направленными на предотвращение прогрессирования заболевания, вызванного вирусом иммунодефицита человека.
Я подтверждаю, что мне разъяснено:
- почему проведение данного лечения необходимо моему ребенку;
- действие назначаемых моему ребенку препаратов;
- как необходимо давать моему ребенку назначенные препараты;
- возможное побочное действие препаратов, назначенных моему ребенку;
- что мой ребенок должен проходить регулярные обследования, в том числе сдавать кровь, для контроля течения ВИЧ-инфекции и назначенного лечения и выявления возможного побочного действия лекарств;
- в какие сроки я должна приводить ребенка на обследование;
- что эффект лечения может быть достигнут при неукоснительном соблюдении всех рекомендаций, данных мне лечащим врачом моего ребенка.
Я осознаю, что:
- по состоянию здоровья моего ребенка ему необходимо лечение по поводу ВИЧ-инфекции;
- назначенные моему ребенку препараты должны подавлять размножение вируса в его организме и замедлять прогрессирование ВИЧ-инфекции;
- чем лучше я буду соблюдать режим приема препаратов моим ребенком, тем выше вероятность того, что увеличится продолжительность и качество его жизни;
- даже при абсолютном соблюдении мною всех правил приема препаратов моим ребенком излечение от ВИЧ-инфекции не произойдет;
- назначенное моему ребенку лечение может в любой момент быть прекращено по моему желанию;
- если вследствие проведения лечения возникнет угроза здоровью моего ребенка, я буду проинформирован(а) об этом для принятия решения о целесообразности дальнейшего его проведения;
- если вследствие проведения лечения возникнет угроза жизни моего ребенка, это лечение может быть прекращено по решению лечащего врача. В этом случае мне должны быть разъяснены причины этого решения;
- все лекарственные препараты, назначаемые моему ребенку, разрешены к применению в России;
- как и любое лекарственное средство, назначенные моему ребенку препараты могут вызывать некоторые побочные реакции, информация о которых предоставлена мне моим лечащим врачом;
Я обязуюсь:
- по установленному графику приводить своего ребенка на медицинское обследование для контроля воздействия назначенных ему препаратов, заполнять предусмотренные для этого анкеты, давать разрешение на взятие крови на анализы;
- давать назначенные моему ребенку лекарственные препараты строго в соответствии с предписанием лечащего врача;
- выполнять рекомендации лечащего врача по уходу за моим ребенком, его кормлению;
- сообщать лечащему врачу обо всех нарушениях в приеме назначенных моему ребенку препаратов или прекращении лечения по каким-либо причинам;
- сообщать лечащему врачу обо всех изменениях в состоянии здоровья моего ребенка и делать это незамедлительно (в течение суток), если я считаю, что эти изменения связаны с приемом препаратов, назначенных моему ребенку;
- не посоветовавшись с лечащим врачом, не давать моему ребенку какие-либо лекарственные препараты и не делать прививки (даже если лекарства и прививки назначаются другим врачом). Если же прием этих лекарств неизбежен (например, в экстренных случаях), незамедлительно сообщать об этом лечащему врачу;
- сообщить врачу, назначившему моему ребенку лекарственные препараты в экстренных случаях, что ребенок получает препараты для лечения ВИЧ-инфекции.
|
Подпись лица, осуществляющего уход за ребенком:
|
Дата:
|
|||||
|
Врач:
|
Дата:
|
|||||
|
(Фамилия И.О., разборчиво)
|
(подпись)
|
|||||
ОБРАЗЕЦ
7. Информированный отказ от видов медицинских вмешательств, включенных в перечень определенных видов медицинских вмешательств, на которые граждане дают информированное добровольное согласие при выборе врача и медицинской организации для получения первичной медико-санитарной помощи и/или антиретровирусной терапии
(подписывает законный представитель, осуществляющий уход за ребенком)
|
Я,
|
|
|
(Ф.И.О.)
|
|
|
Дата рождения:
|
|
|
Зарегистрированный(ая) по адресу:
|
|
|
при оказании первичной медико-санитарной помощи моему ребенку
|
|
|
(Фамилия, Имя, Отчество полностью разборчиво)
|
|
|
(Дата рождения)
|
|
|
в
|
|
|
(название медицинской организации)
|
|
отказываюсь от следующих видов медицинских вмешательств, включенных в Перечень определенных видов медицинских вмешательств, на которые граждане дают информированное добровольное согласие при выборе врача и медицинской организации для получения первичной медико-санитарной помощи, утвержденный приказом Министерства здравоохранения и социального развития Российской Федерации от 23 апреля 2012 г. N 390н (зарегистрирован Министерством юстиции Российской Федерации 5 мая 2012 г. N 24082) (далее - виды медицинских вмешательств):
1. Опрос, в том числе выявление жалоб, сбор анамнеза
2. Осмотр, в том числе пальпация, перкуссия, аускультация, вагинальное исследование (для женщин), ректальное исследование.
3. Антропометрические исследования.
4. Термометрия.
5. Тонометрия.
6. Неинвазивные исследования органов зрения и зрительных функций.
7. Неинвазивные исследования органов слуха и слуховых функций.
8. Исследование функций нервной системы (чувствительной и двигательной сферы).
9. Лабораторные методы обследования, в том числе клинические, биохимические, бактериологические, вирусологические, иммунологические.
10. Функциональные методы обследования, в том числе электрокардиография.
11. Рентгенологические методы обследования, в том числе флюорография (для лиц старше 15 лет) и рентгенография, ультразвуковые исследования.
12. Введение лекарственных препаратов по назначению врача, в том числе внутримышечно, внутривенно, подкожно, внутрикожно.
13. Антиретровирусная терапия
|
14. Другое:
|
||
|
(наименование другого вида медицинского вмешательства)
|
||
|
Медицинским работником
|
||
|
(должность, Ф.И.О. медицинского работника)
|
||
в доступной для меня форме мне разъяснено состояние здоровья моего ребенка, диагноз, изложены цели, характер, необходимость проведения диагностических и лечебных мероприятий. Разъяснено, что предложенная моему ребенку антиретровирусная терапия направлена на подавление размножения вируса иммунодефицита человека в его организме, замедление прогрессирования ВИЧ-инфекции, что позволит увеличить продолжительность и улучшить качество его жизни. Разъяснено, что предоставление антиретровирусных препаратов осуществляется на бесплатной основе. Мне разъяснены и понятны возможные последствия отказа от медицинского вмешательства/антиретровирусной терапии (нужное подчеркнуть), в том числе вероятность развития осложнений заболевания (состояния), что отказ от антиретровирусной терапии может привести к прогрессированию ВИЧ-инфекции у моего ребенка с развитием угрожающих жизни проявлений, таких как генерализованный туберкулез, пневмоцистная пневмония, поражения центральной нервной системы различными инфекциями, развитие онкологических заболеваний и др. вплоть до гибели. Разъяснено, что при возникновении необходимости в осуществлении медицинского вмешательства, в отношении которого оформлен настоящий отказ, я имею право оформить информированное добровольное согласие на такой вид медицинского вмешательства. Настоящим я подтверждаю свой добровольный отказ от проведения своему ребенку антиретровирусной терапии, последствия отказа мне разъяснены, ответственность за состояние здоровья моего ребенка беру на себя.
|
Причина отказа:
|
||
|
(Ф.И.О. лица, осуществляющего уход за ребенком)
|
(подпись)
|
(дата)
|
|
(Ф.И.О. медицинского работника)
|
(подпись)
|
(дата)
|
ОБРАЗЕЦ
8. Информированное согласие на проведение антиретровирусной терапии у ребенка с ВИЧ-инфекцией в возрасте 15 лет и старше
|
Я,
|
|
(Фамилия, Имя, Отчество полностью разборчиво, домашний адрес, телефон)
|
|
настоящим подтверждаю свое добровольное согласие на мое лечение лекарственными препаратами, направленными на предотвращение прогрессирования ВИЧ-инфекции:
|
Я подтверждаю, что мне разъяснено:
- что предложенная мне антиретровирусная терапия назначена по клиническим и лабораторным показаниям, и направлена на подавление размножения вируса иммунодефицита человека в моем организме, замедление прогрессирования ВИЧ-инфекции, что позволит увеличить продолжительность и улучшить качество моей жизни.
- что на сегодняшний день не существует лечения, позволяющего излечиться от ВИЧ-инфекции.
- что все антиретровирусные препараты, назначенные мне, разрешены к применению в Российской Федерации и предоставляются на бесплатной основе.
- что антиретровирусные препараты, как и другие лекарственные препараты, могут вызывать нежелательные явления, информация о которых предоставлена мне лечащим врачом.
- что назначенная мне антиретровирусная терапия может быть прекращена по моему собственному желанию или решению лечащего врача из-за несоблюдения мною режима приема препаратов и/или графика обследования.
Я обязуюсь:
- согласно графику, установленному лечащим врачом, проходить лабораторные обследования и консультаций, в целях своевременного мониторинга назначенного мне лечения;
- принимать назначенные мне лекарственные препараты в соответствии с режимом приема и указаниями лечащего врача;
- в кратчайшие сроки сообщать лечащему врачу обо всех изменениях схемы лечения, а также об изменениях в моем состоянии, если я считаю, что это связано с назначенным мне лечением.
Я информирован(а), что в соответствии с требованиями Федерального Закона Российской Федерации N 323-ФЗ в случае нарушения сроков лабораторного обследования и/или посещения лечащего врача, меня будут приглашать в медицинскую организацию по телефону/посещением на дому специалистами поликлиники.
|
Пациент
|
Дата
|
|||||
|
(Ф.И.О.)
|
(подпись)
|
|||||
|
Врач
|
Дата
|
|||||
|
(Ф.И.О.)
|
(подпись)
|
ОБРАЗЕЦ
9. Информированный отказ от видов медицинских вмешательств, включенных в перечень определенных видов медицинских вмешательств, на которые граждане дают информированное добровольное согласие при выборе врача и медицинской организации для получения первичной медико-санитарной помощи и/или антиретровирусной терапии ребенка с ВИЧ-инфекцией в возрасте 15 лет и старше
|
Я,
|
|
(Ф.И.О.)
|
|
Дата рождения:
|
|
Зарегистрированный(ая) по адресу:
|
|
при оказании мне первичной медико-санитарной помощи в
|
|
(название медицинской организации)
|
отказываюсь от следующих видов медицинских вмешательств, включенных в Перечень определенных видов медицинских вмешательств, на которые граждане дают информированное добровольное согласие при выборе врача и медицинской организации для получения первичной медико-санитарной помощи, утвержденный приказом Министерства здравоохранения и социального развития Российской Федерации от 23 апреля 2012 г. N 390н (зарегистрирован Министерством юстиции Российской Федерации 5 мая 2012 г. N 24082) (далее - виды медицинских вмешательств):
1. Опрос, в том числе выявление жалоб, сбор анамнеза
2. Осмотр, в том числе пальпация, перкуссия, аускультация, вагинальное исследование (для женщин), ректальное исследование.
3. Антропометрические исследования.
4. Термометрия.
5. Тонометрия.
6. Неинвазивные исследования органов зрения и зрительных функций.
7. Неинвазивные исследования органов слуха и слуховых функций.
8. Исследование функций нервной системы (чувствительной и двигательной сферы).
9. Лабораторные методы обследования, в том числе клинические, биохимические, бактериологические, вирусологические, иммунологические.
10. Функциональные методы обследования, в том числе электрокардиография.
11. Рентгенологические методы обследования, в том числе флюорография (для лиц старше 15 лет) и рентгенография, ультразвуковые исследования.
12. Введение лекарственных препаратов по назначению врача, в том числе внутримышечно, внутривенно, подкожно, внутрикожно.
15. Антиретровирусная терапия
|
16. Другое:
|
||
|
(наименование другого вида медицинского вмешательства)
|
||
|
Медицинским работником
|
||
|
(должность, Ф.И.О. медицинского работника)
|
||
в доступной для меня форме мне разъяснено состояние моего здоровья, диагноз, изложены цели, характер, необходимость проведения диагностических и лечебных мероприятий. Разъяснено, что предложенная мне антиретровирусная терапия направлена на подавление размножения вируса иммунодефицита человека в моем организме, замедление прогрессирования ВИЧ-инфекции, что позволит увеличить продолжительность и улучшить качество моей жизни. Разъяснено, что предоставление антиретровирусных препаратов осуществляется на бесплатной основе. Мне разъяснены и понятны возможные последствия отказа от медицинского вмешательства/антиретровирусной терапии (нужное подчеркнуть), в том числе вероятность развития осложнений заболевания (состояния), что отказ от антиретровирусной терапии у меня может привести к прогрессированию ВИЧ-инфекции с развитием угрожающих жизни проявлений, таких как генерализованный туберкулез, пневмоцистная пневмония, поражения центральной нервной системы различными инфекциями, развитие онкологических заболеваний и др. вплоть до гибели. Разъяснено, что при возникновении необходимости в осуществлении медицинского вмешательства, в отношении которого оформлен настоящий отказ, я имею право оформить информированное добровольное согласие на такой вид медицинского вмешательства. Настоящим я подтверждаю свой добровольный отказ от проведения мне антиретровирусной терапии, последствия отказа мне разъяснены, ответственность за состояние моего здоровья беру на себя.
|
Причина отказа:
|
||
|
(Ф.И.О. гражданина)
|
(подпись)
|
(дата)
|
|
(Ф.И.О. медицинского работника)
|
(подпись)
|
(дата)
|
10. Индекс массы тела у детей
У детей в возрасте двух лет и старше:
Формула ИМТ:

Расчет ИМТ: [вес (кг) / рост (см) / рост (см)] x 10 000
Полученный ИМТ оценивается в процентилях по графикам.
|
Процентиль
|
Интерпретация
|
|
>= 95
|
Избыточный вес
|
|
>= 85 < 95
|
Риск избыточного веса
|
|
>= 5 < 85
|
Нормальный вес
|
|
< 5
|
Сниженный вес
|
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Алгоритм диагностики ВИЧ-инфекции у детей ВИЧ-серопозитивных матерей при отсутствии грудного вскармливания
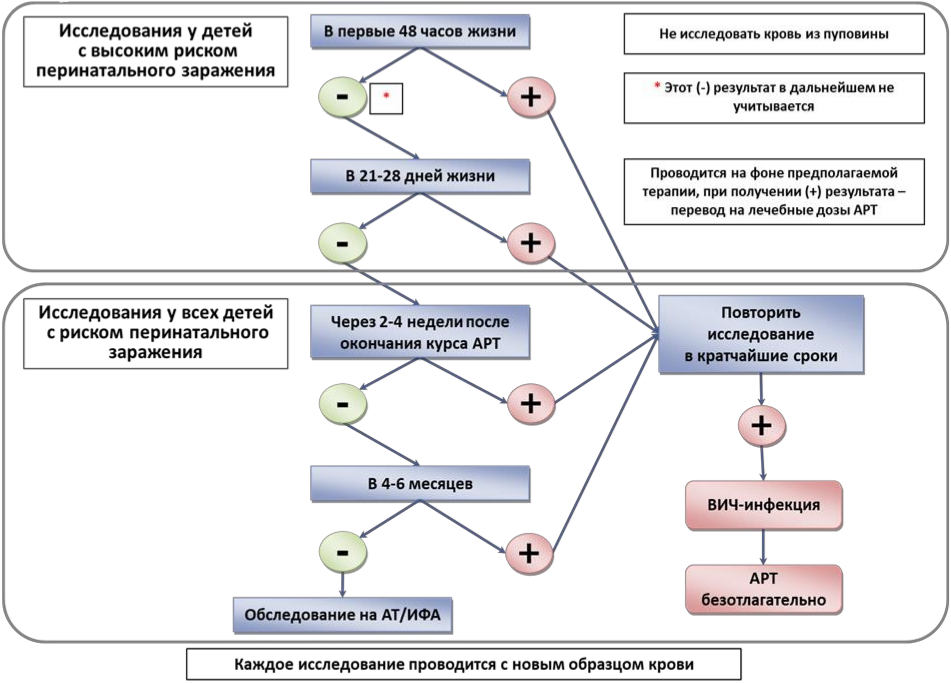
См. разделы: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики, 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики.
Алгоритм назначения АРТ ВИЧ-инфицированным детям
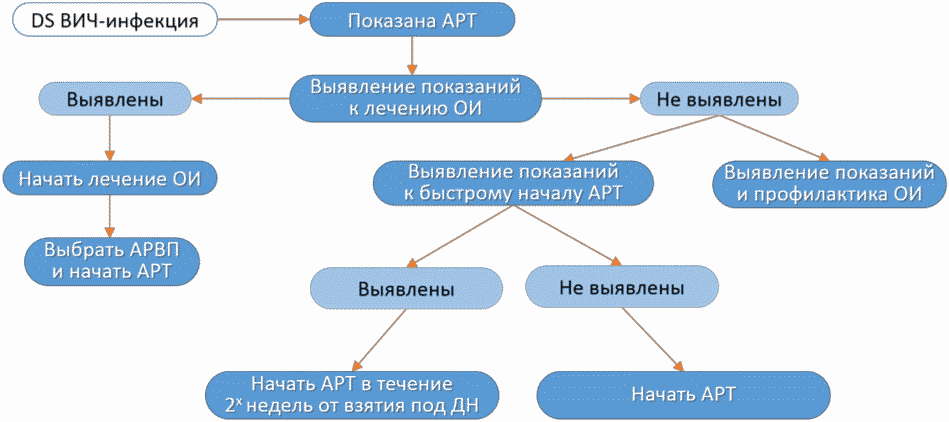
ОИ - оппортунистические инфекции
См. разделы: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики, 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения, 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики, 7. Дополнительная информация.
Алгоритм оценки вирусологической эффективности АРТ у детей

Примечания к алгоритму:
- У детей с ВН > 100.000 и особенно > 500.000 коп/мл перед началом АРТ возможно ее более медленное снижение (в первую очередь у детей первого года жизни и у детей с поздно выявленной ВИЧ-инфекцией).
См. разделы: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики, 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения, 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики, 7. Дополнительная информация.
Алгоритм оценки и коррекции приверженности лекарственной терапии в структуре медицинского и социо-психологического сопровождения ВИЧ-инфицированного ребенка
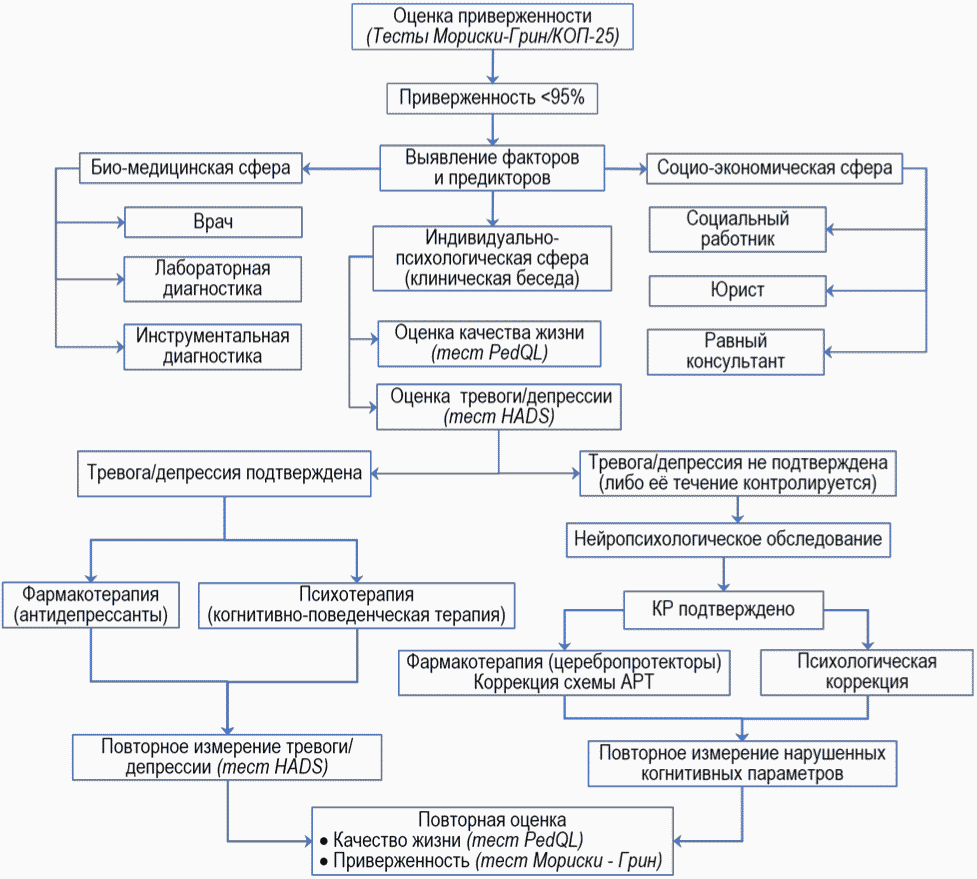
См. разделы: 2. Диагностика ВИЧ-инфекции, медицинские показания и противопоказания к применению методов диагностики, 3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения, 7. Дополнительная информация, Приложения Г1 - Г4.
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
После постановки диагноза ВИЧ-инфекции проводится беседа с лицом, ухаживающим за ребенком, о заболевании, его прогнозе и предполагаемой схеме лечения. По мере взросления ребенка и установления с ним контакта проводится беседа с самим пациентом в доступной для него форме, при необходимости с привлечением медицинского психолога. Объем предоставляемой информации должен быть согласован с опекуном заранее во избежание нежелательного преждевременного раскрытия ВИЧ-статуса ребенку. Учитывая пожизненный прием препаратов и необходимость выработки максимальной приверженности, при каждом визите оценивается понимание цели терапии пациентом и его индивидуальная удовлетворенность лечением. Оценка включает активный поиск нежелательных реакций и явлений при проведении длительной АРТ и психологических препятствий к соблюдению режима лечения, невнимание к которым приведет к пропускам доз у пациента, особенно подросткового возраста.
Приложение Г1 - ГN
ШКАЛЫ
ОЦЕНКИ, ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ СОСТОЯНИЯ
ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Приложение Г1
ШКАЛА КОЛИЧЕСТВЕННОЙ ОЦЕНКИ ПРИВЕРЖЕННОСТИ АРТ МОРИСКИ-ГРИН
Название на русском языке: Шкала комплаентности Мориски-Грин.
Оригинальное название: Medication Adherence Scale.
Источник: Morisky D.E., Green L.W., Levine D.M. Concurrent and Predictive Validity of a Self-Reported Measure of Medication Adherence. Medical Care, Vol. 24, No. 1 (Jan., 1986), pp. 67 - 74.
Тип: шкала оценки.
Назначение: клинико-психологическая тестовая методика, предназначенная для предварительной оценки комплаентности и скринигового выявления недостаточно комплаентных больных в рутинной врачебной практике. Используется для включения в программу стандартного медицинского обследования людей с хроническими заболеваниями. Может быть применена для выделения контингента, нуждающегося в дополнительном внимании как недостаточно приверженного лечению. Используется в научных исследованиях как основной инструмент и как эталон сравнения при разработке новых, более подробных и специализированных шкал.
Содержание: Шкала Мориски-Грин состоит из 8 пунктов, касающихся отношения пациента к приему препаратов. Шкала предназначена для заполнения самим пациентом; при необходимости врач может зачитывать вопросы и помечать ответы на них. В оригинальной шкале каждый пункт оценивается по принципу "Да-Нет". Каждый пункт оценивается по принципу "Да-Нет". В вопросах под номерами 1 - 4 и 6 - 8 ответ "Нет" оценивается в 1 балл; в вопросе под номером 5 в 1 балл оценивается ответ "Да". Анкетирование для количественной оценки приверженности к лечению можно выполнить как в автоматизированном, так и в ручном режиме.
Ключ: Высоко приверженными считаются пациенты, набравшие 8 из 8 баллов, средне приверженными - получившие 6 - 7 баллов, и плохо приверженными - те, кто набрал менее 6 баллов.
Пояснения: Приверженность лечению - степень, с которой пациент следует рекомендациям врача, таким как изменение поведения или прием препаратов. При этом комплаентность - следствие контакта между врачом и пациентом, так как роль врача не ограничивается односторонним высказыванием рекомендаций, а роль пациента - их односторонним восприятием. В узком смысле под комплаентностью понимают процент препаратов, предписанных для длительного (в том числе пожизненного) приема, приятых в нужное время и в нужной дозировке. Именно на таком понимании комплаентости построена шкала Мориски-Грин. Многочисленными исследованиями подтверждено, что высокая приверженность по шкале Мориски-Грин значимо коррелирует с достижением долгосрочных целей лечения.
|
Интерпретация полученных данных
|
|||
|
Количество баллов
|
%
|
Заключение
|
Дальнейшие меры
|
|
8
|
100%
|
Высокая приверженность
|
|
|
6 - 7
|
от 75 до 87,5%
|
Недостаточная приверженность. Группа риска по развитию неприверженности
|
Диагностика причин и факторов и работа по повышению приверженности
|
|
менее 6
|
менее 75%
|
Неприверженность
|
|
Вопросы для оценки приверженности АРТ по шкале Мориски-Грин
Для ребенка:
|
ФИО:
|
ДАТА:
|
||
|
N
|
ВОПРОС
|
ДА
|
НЕТ
|
|
1.
|
Забываешь ли ты иногда принимать лекарства?
|
||
|
2.
|
За прошедшие 2 недели, был ли день когда ты забывал(а) принять лекарства?
|
||
|
3.
|
Ты когда-нибудь прекращал(а) принимать лекарства или уменьшал(а) дозу без уведомления врача потому, что ты почувствовал(а) себя хуже, чем было до этого?
|
||
|
4.
|
Бывает ли, что ты забываешь принимать лекарства, находясь в пути или вне дома?
|
||
|
5.
|
Принимал(а) ли ты твои лекарства вчера?
|
||
|
6.
|
Прекращаешь ли ты прием лекарств, когда чувствуешь, что твое самочувствие под контролем?
|
||
|
7.
|
Не огорчала ли тебя когда-нибудь необходимость постоянно принимать лекарства?
|
||
|
8.
|
Ты испытываешь трудности, в запоминании времени приема лекарств?
|
||
|
Итог
|
|||
|
Приверженность
|
|||
Для законного представителя ребенка:
|
ФИО:
|
ДАТА:
|
||
|
N
|
ВОПРОС
|
ДА
|
НЕТ
|
|
1.
|
Забываете ли вы иногда давать ребенку лекарства?
|
||
|
2.
|
За прошедшие 2 недели, был ли день когда вы забывали дать ребенку лекарства?
|
||
|
3.
|
Вы когда-нибудь прекращали давать лекарства или уменьшали дозу без уведомления врача потому, что ребенок почувствовал себя хуже, чем было до этого?
|
||
|
4.
|
Бывает ли, что вы забываете давать ребенку лекарства, находясь в пути или вне дома?
|
||
|
5.
|
Принимал ли ребенок лекарства вчера?
|
||
|
6.
|
Прекращаете ли вы давать лекарства ребенку, когда чувствуете, что его самочувствие под контролем?
|
||
|
7.
|
Не огорчала ли вас когда-нибудь необходимость строго придерживаться схемы лечения для вашего ребенка?
|
||
|
8.
|
Как часто вы испытываете трудности, в запоминании времени приема лекарства вашим ребенком?
|
||
|
Итог
|
|||
|
Приверженность
|
|||
Приложение Г2
ГОСПИТАЛЬНАЯ ШКАЛА ТРЕВОГИ И ДЕПРЕССИИ HADS
Название на русском языке: Госпитальная шкала тревоги и депрессии HADS.
Оригинальное название: The Hospital Anxiety and Depression Scale.
Источники: Андрющенко А.В., Дробижев М.Ю., Добровольский А.В. Сравнительная оценка шкал CES-D, BDI и HADS(D) в диагностике депрессий в общемедицинской практике. Журнал неврологии и психиатрии им. С.С. Корсакова, 2003, No. 5, 11 - 17. Zigmond A.S., Snaith R.P. The Hospital Anxiety and Depression Scale. Acta Psychiatr Scand. 1983; 67: 361-70.
Тип: шкала оценки.
Назначение: Госпитальная шкала тревоги и депрессии представляет собой экспресс-скрининг для оценки уровня тревоги и депрессии в условиях общемедицинской практики. Обладает высокой дискриминантной валидностью в отношении двух расстройств: тревоги и депрессии.
Госпитальная шкала тревоги и депрессии (HADS) - ключевые преимущества:
1. Надежная шкала самооценки, которая измеряет степень тревоги и депрессии.
2. Скорость. Всего 14 вопросов. Заполнение занимает от 2 до 5 минут.
3. Простота. Легко заполнить, легко подсчитать, легко интерпретировать результаты.
4. Распространенность. Шкала доступна на 115 языках и, поэтому подходит для исследований на международном уровне.
Содержание: Госпитальная шкала тревоги и депрессии содержит 14 пунктов, каждому из которых соответствует 4 варианта ответов, отражающих степень нарастания симптоматики.
Бланк шкалы выдается для самостоятельного заполнения испытуемому и сопровождается инструкцией. Шкала составлена из 14 утверждений, обслуживающих 2 подшкалы - "тревога" (7 утверждений) и "депрессия" (7 утверждений). Каждому утверждению соответствуют 4 варианта ответа, отражающие градации выраженности признака и кодирующиеся по нарастанию тяжести симптома от 0 (отсутствие) до 3 (максимальная выраженность).
Ключ: Уровень депрессии и тревоги оценивается независимо друг от друга. Для этого ведется отдельный подсчет баллов по вопросам, оценивающим уровень депрессии и по вопросам оценки степени тревоги.
|
Количество баллов
|
Интерпретация
|
|
0 - 7
|
"норма" (отсутствие достоверно выраженных симптомов тревоги и депрессии)
|
|
8 - 10
|
"субклинически выраженная тревога/депрессия"
|
|
11 и более
|
"клинически выраженная тревога/депрессия"
|
Пояснения: Изначально госпитальная шкала тревоги и депрессии HADS (The hospital Anxiety and Depression Scale Zigmond A.S., Snaith R.P.) была разработана для выявления состояний депрессии, тревоги и эмоционального расстройства среди пациентов, которые проходили лечение по разным клиническим заболеваниям. По замыслу разработчиков шкалы (Zigmond & Snaith, 1983) это позволило бы выявить вклад расстройств настроения (особенно - тревоги и депрессии) в развитие и лечение основного заболевания. В настоящее время данная шкала является наиболее используемой в мире для первичного выявления депрессии и тревоги в условиях общемедицинской практики. Шкала HADS валидизирована в России (русская версия А.В. Андрюшенко, М.Ю. Дробижев, А.В. Добровольский, 2003).
Шкала HADS для определения уровня тревоги и депрессии не вызывает затруднений у пациента и не требует продолжительного времени на заполнение и интерпретацию результатов. Шкала предназначена для того, чтобы помочь врачу лучше понять эмоциональное состояние и самочувствие пациента. Для углубленной диагностики эмоционального состояния пациента рекомендуется использовать: шкалу Гамильтона для оценки тревоги - HARS и шкалу Гамильтона для оценки депрессии - HDRS.
Практические рекомендации пациенту: Шкалу необходимо заполнить за 10 - 15 минут самостоятельно, без обсуждения с кем-либо. По всем пунктам должны быть выбраны ответы. Каждому утверждению шкалы HADS соответствуют четыре варианта ответа. Выберите и отметьте тот из ответов, который соответствует Вашему состоянию в течение последних 7 дней. Не раздумывайте долго над ответом на вопрос. Ваша первая реакция будет наиболее верной.
Госпитальная Шкала Тревоги и Депрессии (HADS)
Ученые уверены в том, что эмоции играют важную роль в возникновении большинства заболеваний. Если Ваш доктор больше узнает о Ваших переживаниях, он сможет лучше помочь Вам. Этот опросник разработан для того, чтобы помочь Вашему доктору понять, как Вы себя чувствуете. Не обращайте внимания на цифры. Прочитайте внимательно каждое утверждение и отметьте ответ, который в наибольшей степени соответствует тому, как Вы себя чувствовали на прошлой неделе. Не раздумывайте слишком долго над каждым утверждением, Ваша первая реакция всегда будет более верной.
Часть I (оценка уровня ТРЕВОГИ)
1. Я испытываю напряжение, мне не по себе
3 - все время
2 - часто
1 - время от времени, иногда
0 - совсем не испытываю
2. Я испытываю страх, кажется, что что-то ужасное может вот-вот случиться
3 - определенно это так, и страх очень велик
2 - да, это так, но страх не очень велик
1 - иногда, но это меня не беспокоит
0 - совсем не испытываю
3. Беспокойные мысли крутятся у меня в голове
3 - постоянно
2 - большую часть времени
1 - время от времени и не так часто
0 - только иногда
4. Я легко могу присесть и расслабиться
0 - определенно, это так
1 - наверно, это так
2 - лишь изредка, это так
3 - совсем не могу
5. Я испытываю внутреннее напряжение или дрожь
0 - совсем не испытываю
1 - иногда
2 - часто
3 - очень часто
6. Я испытываю неусидчивость, мне постоянно нужно двигаться
3 - определенно, это так
2 - наверно, это так
1 - лишь в некоторой степени, это так
0 - совсем не испытываю
7. У меня бывает внезапное чувство паники
3 - очень часто
2 - довольно часто
1 - не так уж часто
0 - совсем не бывает
Количество баллов ________
Часть II (оценка уровня ДЕПРЕССИИ)
1. То, что приносило мне большое удовольствие, и сейчас вызывает у меня такое же чувство
0 - определенно, это так
1 - наверное, это так
2 - лишь в очень малой степени, это так
3 - это совсем не так
2. Я способен рассмеяться и увидеть в том или ином событии смешное
0 - определенно, это так
1 - наверное, это так
2 - лишь в очень малой степени, это так
3 - совсем не способен
3. Я испытываю бодрость
3 - совсем не испытываю
2 - очень редко
1 - иногда
0 - практически все время
4. Мне кажется, что я стал все делать очень медленно
3 - практически все время
2 - часто
1 - иногда
0 - совсем нет
5. Я не слежу за своей внешностью
3 - определенно, это так
2 - я не уделяю этому столько времени, сколько нужно
1 - может быть, я стал меньше уделять этому времени
0 - я слежу за собой так же, как и раньше
6. Я считаю, что мои дела (занятия, увлечения) могут принести мне чувство удовлетворения
0 - точно так же, как и обычно
1 - да, но не в той степени, как раньше
2 - значительно меньше, чем обычно
3 - совсем так не считаю
7. Я могу получить удовольствие от хорошей книги, радио- или телепрограммы
0 - часто
1 - иногда
2 - редко
3 - очень редко
Количество баллов ________