МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
БОЛЕЗНЬ КРОНА
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: K50
Год утверждения (частота пересмотра): 2024
Возрастная категория: Взрослые
Пересмотр не позднее: 2026
ID: 176
Разработчик клинической рекомендации
- Общероссийская общественная организация "Ассоциация колопроктологов России"
- Российская Гастроэнтерологическая Ассоциация
Одобрено Научно-практическим Советом Минздрава РФ
Список сокращений
АЛТ - аланинаминотрансфераза
АСТ - аспартатаминотрансфераза
5-АСК - аминосалициловая кислота**
АЗА - азатиоприн
БК - болезнь Крона
БОС - биологическая обратная связь
ВЗК - воспалительные заболевания кишечника
ВТЭО - венозные тромбоэмболические осложнения
гамма-ГТ - гамма-глютамилтранспептидаза
ГИБП - генно-инженерный биологический препарат
ГКС - глюкокортикостероиды
ДИ - доверительный интервал
ЖКТ - желудочно-кишечный тракт
ИАБК - индекс активности болезни Крона
ИАРА - илеоанальный резервуарный анастомоз
ИМТ - индекс массы тела
КТ - компьютерная томография
ЛДГ - лактатдегидрогеназа
МП - меркаптопурин
МТ - метотрексат
МРТ - магнитно-резонансная томография
НПВС - нестероидные противовоспалительные средства
НМГ - низкомолекулярный гепарин
НФГ - нефракционированный гепарин
ПЦР - полимеразная цепная реакция
РКИ - рандомизированное контролируемое испытание
СОЭ - скорость оседания эритроцитов
CРБ - C-реактивный белок
ТИС - таргетные иммуносупрессоры (L04AA Селективные иммунодепрессанты)
ЦМВ - цитомегаловирус
ФК - фекальный кальпротектин
ФНО-альфа - фактор некроза опухоли-альфа
УЗИ - ультразвуковое исследование
ЭУЗИ - эндоректальное ультразвуковое исследование
ЭндоУЗИ - эндосонография
ЯК - язвенный колит
SES-CD (Simple Endoscopic Score for crohn"s disease) - простая эндоскопическая шкала болезни Крона
Термины и определения
Болезнь Крона (БК) - хроническое, рецидивирующее заболевание желудочно-кишечного тракта (ЖКТ) неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений [1].
Рецидив БК - возобновление типичных проявлений заболевания у пациента с установленным диагнозом БК, в стадии клинической ремиссии, спонтанной или медикаментозно поддерживаемой или после оперативного лечения, подтвержденное объективными инструментальными и лабораторными тестами [2].
Ранний рецидив БК - возобновление типичных симптомов заболевания менее, чем через 3 месяца после достижения клинической ремиссии на предшествующей терапии.
Клинический ответ БК - снижение индекса Харви-Брэдшоу 4 и менее балла, или активности БК (ИАБК) более, чем на 100 баллов.
Клиническая ремиссия БК - отсутствие симптомов БК (соответствует значению индекса Харви-Брэдшоу <= 4 или индекса активности БК (ИАБК) < 150)
Эндоскопический ответ БК - снижение эндоскопической активности заболевания по шкале SES-CD более, чем на 50% от исходного.
Эндоскопическое заживление слизистой оболочки (mucosal healing) - подразумевает не полную эндоскопическую ремиссию, а отсутствие язв слизистой оболочки по SES-CD в зоне поражения при возможном сохранении афт, гиперемии и других признаков воспаления.
Эндоскопическая ремиссия БК - состояние, при котором воспалительная активность при эндоскопическом исследовании по шкале SES-CD составляет менее 4 баллов.
Трансмуральное заживление БК - нормализация (<= 3 мм) толщины кишечной стенки (при лучевых методах исследования) [3].
Генно-инженерные биологические препараты (ГИБП) - группа лекарственных средств биологического происхождения, в том числе моноклональные антитела (химерные, гуманизированные, полностью человеческие) и рекомбинантные белки (обычно включают Fc фрагмент IgG человека), полученные с помощью методов генной инженерии, специфически подавляющие иммуновоспалительный процесс и замедляющие прогрессирование заболевания [4].
Таргетные иммуносупрессоры (ТИС) - группа синтетических противовоспалительных лекарственных средств химического происхождения, по механизму действия специфически блокирующих функционирование внутриклеточных сигнальных путей "провоспалительных" и иммунорегуляторных цитокинов [4].
Бионаивный пациент - пациент, не получавший ранее генно-инженерных биологических препаратов (ГИБП) или таргетных иммуносупрессоров (ТИС).
Биосимиляры - это биологические лекарственные средства, содержащие версию активного вещества, уже разрешенного оригинального биологического лекарственного средства (эталонного препарата).
Стероидорезистентность
- В случае тяжелого обострения БК - отсутствие положительной динамики со стороны клинических и лабораторных показателей, несмотря на применение системных ГКС в дозе, эквивалентной 2 мг/кг массы тела преднизолона** в сутки, в течение более чем 7 дней
- В случае среднетяжелого обострения БК - сохранение активности заболевания при пероральном приеме ГКС в дозе, эквивалентной 1 мг/кг массы тела преднизолона** в сутки, в течение 2 недель
Стероидозависимость
- Увеличение активности болезни, возникшее при уменьшении дозы ГКС после достижения исходного улучшения в течение 3 месяцев от начала лечения
- Возникновение рецидива болезни в течение 3 месяцев после окончания лечения ГКС [2]
1. Краткая информация по заболеванию или состоянию (группы заболеваний или состояний)
1.1 Определение заболевания или состояния (группы заболеваний или состояний)
Болезнь Крона (БК) - хроническое, рецидивирующее заболевание желудочно-кишечного тракта (ЖКТ) неясной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений [1].
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Этиология воспалительных заболеваний кишечника (ВЗК), в том числе БК, не установлена. Заболевание развивается в результате сочетания нескольких факторов, включающих генетическую предрасположенность, дефекты врожденного и приобретенного иммунитета, нарушения кишечной микрофлоры и влияние факторов окружающей среды. Описано около 100 генетических полиморфизмов, ассоциированных с БК. Генетическая детерминированность приводит к изменениям врожденного иммунного ответа, аутофагии, нарушению механизмов распознавания микроорганизмов, нарушению эпителиального барьера и, как результат, извращению адаптивного иммунитета. Ключевым дефектом, предрасполагающим к развитию ВЗК является нарушение механизмов распознавания бактериальных молекулярных маркеров дендритными клетками, что приводит к гиперактивации сигнальных провоспалительных путей. Также при ВЗК отмечается уменьшение разнообразия кишечной микрофлоры за счет снижения доли анаэробных бактерий, преимущественно Bacteroidetes и Firmicutes [5, 6]. При наличии указанных микробиологических, иммунологических и генетических изменений ВЗК развиваются под действием пусковых факторов, к которым относят курение, нервный стресс, дефицит витамина D, питание с пониженным содержанием пищевых волокон и повышенным содержанием животного белка, кишечные инфекции, особенно инфекция Clostridioides difficile и цитомегаловирусная инфекция.
Результатом взаимного влияния генетических и предрасполагающих факторов является активация различных субпопуляций Т-лимфоцитов: Т-хелперов 1, 2, 17 типов и регуляторных Т-лимфоцитов на разных этапах воспаления, что ведет к гиперэкспрессии провоспалительных цитокинов, таких как фактор некроза опухоли-альфа 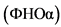 , интерлекинов 1, 12, 23, 17 (ИЛ1, ИЛ12, ИЛ23, ИЛ17) и других и молекул клеточной адгезии.
, интерлекинов 1, 12, 23, 17 (ИЛ1, ИЛ12, ИЛ23, ИЛ17) и других и молекул клеточной адгезии.
Каскад гуморальных и клеточных реакций при БК приводит к трансмуральному воспалению кишечной стенки с образованием характерных для БК саркоидных гранулем, состоящих из эпителиоидных гистиоцитов без очагов некроза и гигантских клеток.
При БК могут поражаться любые отделы ЖКТ - от полости рта до ануса. Тем не менее, в подавляющем большинстве случаев БК поражает илеоцекальный отдел. БК, в отличие от ЯК, не может быть излечена ни терапевтическими, ни хирургическими методами [2]
1.3 Эпидемиология заболевания или состояния (группы заболеваний или состояний)
Максимальная распространенность БК в мире в настоящее время составляет 322/100000 населения (в Европе), а заболеваемость в разных регионах колеблется в интервале от 0,3 до 20,2 на 100000 населения [7, 8, 9, 10]. Данные о распространенности и заболеваемости БК в Российской Федерации крайне ограничены, представлены частичными данными из региональных Регистров и в значительной степени отличаются друг от друга [11, 12, 13, 14]. Распространенность БК выше в северных широтах и на Западе, постоянно увеличивается и в настоящее время достигает до 1 на 200 человек [9]. Заболеваемость и распространенность БК в Азии ниже, однако постоянно увеличивается. Европеоиды страдают заболеванием чаще, чем представители негроидной и монголоидной рас. Пик заболеваемости отмечается между 20 и 30 годами жизни, а второй пик заболеваемости в некоторых странах описан в возрасте 60 - 70 лет. Заболеваемость приблизительно одинакова у мужчин и женщин.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
K 50.0 - Болезнь Крона тонкой кишки
K 50.1 - Болезнь Крона толстой кишки
K 50.8 - Другие разновидности болезни Крона
K 50.9 - Болезнь Крона неуточненная
1.5 Классификация заболевания или состояния (группы заболеваний или состояний)
Для классификации БК применяется Монреальская классификация, по которой БК определяется по нескольким ключевым категориям: локализации воспалительного процесса, характеру течения (фенотипу заболевания) и возрасту начала заболевания (табл. 1). Необходимость выделения БК по возрасту обусловлена разницей клинических проявлений и разным прогнозом заболевания в различных возрастных группах [15].
Таблица 1. Монреальская классификация БК [15].
|
Классификационная категория
|
Обозначение по Монреальской классификации
|
Характеристика
|
|
Локализация воспаления
|
L1
|
Очаг воспаления ограничен терминальным отделом подвздошной кишки или илеоцекальной областью (с вовлечением или без вовлечения в процесс слепой кишки)
|
|
L2
|
Любая локализация воспалительного очага в толстой кишке между слепой кишкой и анальным сфинктером, без вовлечения тонкой кишки или верхнего отдела ЖКТ
|
|
|
L3
|
Терминальный илеит (с вовлечением или без вовлечения слепой кишки) в сочетании с одним или несколькими очагами воспаления между слепой кишкой и анальным сфинктером
|
|
|
L4
|
Изолированное поражение верхних отделов ЖКТ (проксимальнее терминального отдела подвздошной кишки (исключая полость рта).
L4 может сочетаться с локализациями L1 - L3
|
|
|
Фенотип заболевания (характер течения)
|
B1
|
Не стриктурирующая, не пенетрирующая
(синонимы рус. - просветная, воспалительная, неосложненная, анг. - luminal) - воспалительный характер течения заболевания, которое никогда не было осложненным (в любое время в ходе болезни)
|
|
B2
|
Стриктурирующая (стенозирующая) - сужение просвета кишки на любом уровне (по данным лучевых и/или эндоскопических методов или по результатам хирургического вмешательства)
|
|
|
B3
|
Пенетрирующая (синонимы рус. - свищевая, англ. - fistulising) - формирование интраабдоминальных свищей, и/или воспалительного инфильтрата с абсцессом в любое время в течении болезни, исключая послеоперационные интраабдоминальные осложнения
|
|
|
p
|
Перианальная: наличие перианальных поражений (свищи, анальные трещины, перианальные абсцессы), которые могут сочетаться с любым из указанных фенотипов или быть самостоятельным проявлением перианальной БК
|
|
|
Возраст установления диагноза
|
A1
|
Менее 16 лет
|
|
A2
|
От 17 до 40 лет
|
|
|
A3
|
Более 40 лет
|
По распространенности поражения выделяют [10]:
1. Локализованная БК:
- Поражение протяженностью менее 30 см. Чаще встречается при изолированном поражении илеоцекальной зоны;
- Возможно изолированное поражение небольшого участка толстой кишки.
2. Распространенная БК:
- Поражение протяженностью более 100 см (сумма всех пораженных участков).
По характеру течения выделяют [16]:
1. Острое течение (менее 6 месяцев от дебюта заболевания);
2. Хроническое течение (более 6 месяцев от дебюта заболевания).
Оценка тяжести БК
Для правильного формулирования диагноза и определения тактики лечения следует оценивать тяжесть текущего обострения (рецидива) активной БК с выделением легкого, среднетяжелого и тяжелого обострения. Для этого используются различные индексы, включая индекс Харви-Брэдшоу (табл. 2), индекс активности БК (ИАБК, синоним - индекс Беста или англ. CDAI) (табл. 3) [17]. Следует сразу оговориться, что ИАБК как правило, применяется в клинических испытаниях и неудобен для практического применения из-за сложности расчета, а для клинической практики проще и удобнее применять индекс Харви-Брэдшоу [18]. Можно также использовать простые критерии, разработанные Всероссийским обществом по изучению ВЗК и Ассоциацией колопроктологов России (Табл. 4) [19]. Использование той или иной системы оценки тяжести определяется рутинной практикой конкретного лечебного учреждения.
Таблица 2. Индекс Харви-Брэдшоу [18]
|
Критерий оценки
|
Выраженность симптома
|
Оценка в баллах
|
|
Общее самочувствие накануне
|
Очень хорошее
|
0
|
|
Немного хуже обычного
|
1
|
|
|
Плохое
|
||
|
Очень плохое
|
3
|
|
|
Ужасное
|
4
|
|
|
Боль в животе накануне
|
Нет
|
0
|
|
Слабая
|
1
|
|
|
Умеренная
|
2
|
|
|
Сильная
|
2
|
|
|
Частота жидкого/мягкого стула/день (например накануне)
|
1 балл за каждую дефекацию
|
|
|
Пальпируемое образование в брюшной полости
|
Нет
|
0
|
|
Сомнительно
|
1
|
|
|
Четко определяется
|
2
|
|
|
Четко определяется, болезненно при пальпации
|
3
|
|
|
Осложнения (указать все, что применимо.
|
артралгия, увеит, узловатая эритема, афтозный стоматит, гангренозная пиодермия, анальная трещина, свищ, абсцесс, другое
|
1 балл за каждое осложнение
|
|
Сумма баллов <= 4 ремиссия, 5 - 7 баллов - легкое обострение, 8 - 16 баллов - обострение средней тяжести, >= 16 баллов - тяжелое обострение
|
||
https://www.thecalculator.co/health/Harvey-Bradshaw-Index-For-Crohn%E2%80%99s-Disease-Calculator-1036.html (ссылка на калькулятор для подсчета индекса Харви-Брэдшоу)
Таблица 3. Индекс активности БК (ИАБК) [17]
|
Критерии. Оценка в баллах
|
Коэффициент
|
|
1. Количество дефекаций жидким или мягким калом на протяжении недели (сумма за 7 дней)
|
X 2
|
|
2. Интенсивность болей в животе (от 0 до 3 баллов) на протяжении недели (сумма за 7 дней)
|
X 5
|
|
3. Самочувствие в течение недели (от 0 до 4 баллов, сумма за 7 дней)
|
X 7
|
|
4. Число осложнений из перечисленных: артралгии или артриты; увеит; узловатая эритема или гангренозная пиодермия или афтозный стоматит; анальная трещина, свищи или абсцессы; межкишечные свищи; лихорадка в течение последней недели
|
X 20
|
|
5. Прием опиатов (0 баллов - нет, 1 балл - да)
|
X 30
|
|
6. Инфильтрат брюшной полости (0 баллов - отсутствует, 2 балла - сомнительный, 5 баллов определяется)
|
X 6
|
|
7. Гематокрит менее 47% для мужчин или менее 42% для женщин (разность между нормальной и фактической величиной)
|
X 6
|
|
8. (1 - фактическая масса тела) x 100 индекс массы тела
|
X 1
|
|
Сумма
|
|
|
Количество баллов ниже 150 указывает на ремиссию болезни, 150 - 300 - на легкую форму, 300 - 450 - на среднетяжелую форму, свыше 450 - на тяжелую форму.
|
|
Таблица 4. Критерии оценки тяжести (клинической активности) обострения БК Всероссийское общество по изучению ВЗК и Ассоциация колопроктологов России [19]
|
Критерий
|
Легкая БК
|
Средней тяжести
|
Тяжелая БК
|
|
Средняя частота стула/сутки за последние 3 дня
|
менее 4
|
4 - 6
|
7 и более
|
|
Боль в животе
|
отсутствует или незначительная
|
умеренная
|
сильная
|
|
Лихорадка
|
отсутствует
|
< 38° C
|
> 38° C
|
|
Тахикардия
|
отсутствует
|
< 90 в 1"
|
> 90 в 1"
|
|
Снижение массы тела
|
отсутствует
|
до 5%
|
5% и более
|
|
Гемоглобин
|
> 100 г/л
|
90 - 100 г/л
|
< 90 г/л
|
|
СОЭ
|
норма
|
< 30 мм/час
|
> 30 мм/час
|
|
CРБ
|
норма
|
до 2-х норм
|
> 2-х норм
|
|
Гипопротеинемия (гипоальбуминемия)
|
отсутствует
|
не значительная
|
выраженная
|
|
Внекишечные проявления (любые)
|
нет
|
есть
|
есть
|
|
Кишечные осложнения (любые)
|
нет
|
есть
|
есть
|
Однако следует оценивать не только тяжесть обострения, но также учитывать тяжесть заболевания в целом, что необходимо для оценки прогноза заболевания и определения социального статуса пациента, включая получение инвалидности, льготного лекарственного обеспечения, бесплатного санаторно-курортного лечения и других социальных льгот. Тяжесть болезни в целом определяется не только тяжестью текущего обострения, но и локализацией и протяженностью воспаления, наличием внекишечных проявлений и осложнений (абсцессов, стриктур, свищей и др), рефрактерностью к лечению, в частности, развитием стероидной зависимости и резистентности.
Классификация БК в зависимости от ответа на гормональную терапию соответствует таковой при ЯК. Выделяют (см. раздел "Термины и определения"):
1. Стероидная резистентность:
2. Стероидная зависимость:
При формулировании диагноза следует отразить:
а) локализацию поражения с перечислением пораженных сегментов ЖКТ;
б) фенотипический вариант;
в) тяжесть текущего обострения или наличие ремиссии заболевания;
г) характер течения заболевания;
е) наличие стероидной зависимости или резистентности;
ж) наличие внекишечных и/или кишечных и перианальных осложнений.
При наличии у пациента свищей и стриктур одновременно или в разные периоды заболевания диагноз БК, согласно Монреальской классификации, формулируется как "пенетрирующая", так как это более тяжелое осложнение, но в диагнозе также обязательно должна фигурировать стриктура как осложнение.
1.6 Клиническая картина заболевания или состояния (группы заболеваний или состояний)
Клиническая картина БК включает четыре клинических синдрома:
Кишечный синдром. Типичные кишечные симптомы включают диарею (более 6 недель), в большинстве случаев без примеси крови, боль в животе.
Эндотоксемия - признаки системного воспаления, обусловленные высокой активностью воспалительного процесса в кишке. Эндотоксемия в разной степени сопутствует среднетяжелым и тяжелым формам БК. Основные симптомы - общая интоксикация, лихорадка, тахикардия, анемия, увеличение СОЭ, лейкоцитоз, тромбоцитоз, повышение уровня острофазных белков: CРБ, фибриногена.
Метаболические расстройства являются следствием токсемии, избыточной потери белка с калом вследствие экссудации и нарушением всасывания воды и электролитов. Клинические симптомы типичны: потеря массы тела (иногда до степени истощения), гипопротеинемия, гипоальбуминемия с развитием отечного синдрома, гипокалиемия и другие электролитные нарушения, гиповитаминоз.
Внекишечные системные проявления (ВКП) (табл. 5).
Таблица 5. Основные внекишечные (системные) проявления БК [14, 20, 21, 22, 23].
|
Аутоиммунные, связанные с активностью заболевания
|
Аутоиммунные, не связанные с активностью заболевания
|
Обусловленные длительным воспалением и метаболическими нарушениями
|
|
Артропатии (артралгии, артриты)
Поражение кожи (узловатая эритема, гангренозная пиодермия)
Поражение слизистых (афтозный стоматит)
Поражение глаз (увеит, ирит, иридоциклит, эписклерит)
Поражение печени (аутоиммунный гепатит)
|
Первичный склерозирующий холангит
Анкилозирующий спондилит (сакроилеит)
Остеопороз, остеомаляция
Псориаз, псориатический артрит
|
Холелитиаз
Стеатоз печени, стеатогепатит
Тромбоз периферических вен, тромбоэмболия легочной артерии
Амилоидоз
|
Аутоиммунные проявления, связанные с активностью воспалительного процесса, появляются вместе с основными кишечными симптомами обострения и исчезают вместе с ними на фоне лечения. Аутоиммунные проявления, не связанные с активностью процесса (в англоязычной литературе их часто называют "сопутствующими аутоиммунными заболеваниями"), имеют тенденцию к прогрессированию независимо от фазы основного заболевания (обострение или ремиссия) и часто определяют негативный прогноз болезни.
Клиническая картина БК на ранних стадиях не всегда имеет четко выраженные симптомы, что затрудняет своевременную диагностику. В связи с этим у значительной части больных в момент установления диагноза, заболевание уже имеет осложненное течение. В ряде случаев БК манифестирует осложнениями, например, нарушением кишечной проходимости, возникшей, как будто бы, на фоне полного здоровья. В этой связи при постановке диагноза у значительной части пациентов обнаруживаются симптомы, связанные с осложнениями БК.
Осложнения БК:
1. Свищи различной локализации
- наружные (кишечно-кожные)
- внутренние (межкишечные, кишечно-пузырные, ректо-вагинальные)
2. Инфильтрат брюшной полости
3. Межкишечные или интраабдоминальные абсцессы
4. Стриктуры ЖКТ (с нарушением кишечной проходимости и без нее)
5. Анальные трещины, парапроктит (при аноректальном поражении)
6. Кишечное кровотечение (редко).
2. Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Однозначных диагностических критериев БК не существует, диагноз устанавливается на основании сочетания данных анамнеза, клинической картины и типичных эндоскопических и гистологических изменений [2, 24, 25].
Общепринятыми являются критерии достоверного диагноза БК по Lennard-Jones, включающие определение семи ключевых признаков заболевания [26]:
1. Локализация в любом месте ЖКТ от полости рта до анального канала; хроническое гранулематозное поражение слизистой оболочки губ или щек; пилородуоденальное поражение, поражение тонкой кишки, хроническое перианальное поражение.
2. Прерывистый характер поражения.
3. Трансмуральный характер поражения: язвы-трещины, абсцессы, свищи.
4. Фиброз: стриктуры.
5. Лимфоидная инфильтрация (гистология): афтоидные язвы или трансмуральные очаговые лимфоидные скопления.
6. Слизь (гистология): нормальное содержание слизи (сохранение секреции) в зоне активного воспаления слизистой оболочки толстой кишки.
7. Наличие эпителиоидной гранулемы.
Диагноз БК считается достоверным при наличии 3 любых признаков или при обнаружении гранулемы в сочетании с любым другим признаком.
Диагноз должен быть подтвержден:
- эндоскопическим и морфологическим методом и/или эндоскопическим и лучевым методом диагностики.
Эндоскопические критерии БК:
- Регионарное (прерывистое) поражение слизистой оболочки;
- Симптом "булыжной мостовой" (сочетание глубоких продольно и поперечно ориентированных язв с выбухающей гиперплазированной слизистой между ними);
- Линейные язвы (язвы-трещины);
- Афты;
- В ряде случаев стриктуры и устья свищей.
Для объективизации и количественной оценки эндоскопической картины применяются эндоскопические индексы. Наиболее удобным и простым для использования является простая эндоскопическая шкала оценки БК (Simple Endoscopic Score CD - SES-CD) (Табл. 6) [27]. В соответствии с этой шкалой эндоскопическая картина в обязательном порядке оценивается в 5 кишечных сегментах: подвздошная кишка, восходящая ободочная кишка, поперечная ободочная кишка, нисходящая ободочная кишка, включая сигмовидную, прямая кишка. В каждом сегменте определяют: наличие и размер язв, наличие афт, площадь поверхности изъязвлений, площадь поверхности поражений, наличие и выраженность стенозов. Каждый критерий оценивается в баллах.
Таблица 6. Простая эндоскопическая шкала оценки БК (SES-CD) [27]
|
SES-CD (оценивается в баллах по каждому из 5 подвздошно-толстокишечных сегментов
|
||||
|
0
|
1
|
2
|
3
|
|
|
Наличие и размер язв
|
Нет
|
Афты
(d 0.1 - 0.5 см)
|
Крупные язвы
(d 0.5 - 2 см)
|
Очень крупные язвы
(d > 2 см)
|
|
Изъязвленная поверхность
|
Нет
|
< 10%
|
10 - 30%
|
> 30%
|
|
Пораженная поверхность
|
Неповрежденный сегмент
|
< 50%
|
50 - 75%
|
> 75%
|
|
Наличие стенозов <*>
|
Нет
|
Единичный, проходимый
|
Множественные, проходимые
|
Непроходимые
|
|
- Сумма баллов всех критериев SES-CD по 5 кишечным сегментам варьирует от 0 до 56
--------------------------------
- <*> Сумма баллов за наличие сужения (стеноза) варьирует от 0 до 11, т.к. 3 - означает стеноз, не проходимый для колоноскопа, т.е. может наблюдаться только один раз
|
||||
SES-CD позволяет не только интерпретировать новые цели, сформулированные в концепции STRIDE 2 [76], но также мониторировать динамику активности воспаления и, соответственно, эффективность лечения. Новые цели (см. раздел термины) включают такие понятия как:
- Эндоскопический ответ - снижение эндоскопической активности заболевания по шкале SES-CD более, чем на 50% от исходного
- Заживление слизистой оболочки (mucosal healing) - подразумевает не полную эндоскопическую ремиссию, а отсутствие язв слизистой оболочки в зоне поражения
- Эндоскопическая ремиссия - трактуется как воспалительная активность <= 4 баллов
Для оценки активности послеоперационного рецидива БК применима шкала Rutgeerts (Табл. 7) [49].
Таблица 7. Шкала эндоскопической оценки активности послеоперационного рецидива БК (Rutgeerts) [49].
|
Эндоскопическая оценка
|
Определения
|
|
i 0
|
нет признаков воспаления
|
|
i 1
|
<= 5 афтозных язв
|
|
i 2
|
> 5 афтозных язв с нормальной слизистой оболочкой между ними или протяженные участки здоровой слизистой оболочки между более выраженными изъязвлениями или поражения, ограниченные подвздошно-толстокишечным анастомозом
|
|
i 3
|
диффузный афтозный илеит с диффузно воспаленной слизистой оболочкой
|
|
i 4
|
диффузное воспаление с крупными язвами, "булыжной мостовой" и/или сужением просвета
|
Рентгенологические проявления БК:
- Регионарное поражение;
- Прерывистое поражение;
- Стриктуры;
- "Булыжная мостовая";
- Межкишечные свищи или внутрибрюшные абсцессы.
Морфологические признаки БК:
- Глубокие щелевидные язвы, проникающие в подслизистую основу или мышечный слой;
- Эпителиоидные гранулемы (скопления эпителиоидных гистиоцитов без очагов некроза и гигантских клеток), которые обычно обнаруживаются в стенке резецированного участка и только в 15 - 36% случаев - при биопсии слизистой оболочки);
- Фокальная (дискретная) лимфоплазмоцитарная инфильтрация собственной пластинки слизистой оболочки;
- Трансмуральная воспалительная инфильтрация с лимфоидной гиперплазией во всех слоях кишечной стенки;
- Поражение подвздошной кишки со структурными изменениями ворсин, мукоидной или псевдопилорической метаплазией крипт и хроническим активным воспалением [28];
- Прерывистое поражение - чередование пораженных и здоровых участков кишки (при исследовании резецированного участка кишки).
В отличие от ЯК, крипт-абсцессы при БК формируются редко, а секреция слизи остается нормальной.
2.1 Жалобы и анамнез
С целью первичной диагностики всем пациентам рекомендуется прием (осмотр, консультация) врача-колопроктолога и/или врача-гастроэнтеролога с обязательным трансректальным пальцевым исследованием (при наличии свищей и/или перианальных проявлениях болезни Крона, наружных кишечных свищей, свищей с полыми органами, межкишечных свищей, стриктуры кишечника), а также при наружных кишечных свищах, свищах с полыми органами, межкишечных свищах, стриктурах кишечника, проявлениях, кровотечениях рекомендован осмотр/консультация врача-колопроктолога или врача-хирурга) [29, 246 - 251].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
При опросе пациента стоит обратить внимание на частоту и характер стула, длительность данных симптомов, наличие примеси крови, характер болей в животе, наличие эпизодов повышения температуры тела, появление анемии неясного генеза, симптомов нарушения кишечной проходимости, перианальных осложнений (хронические анальные трещины, рецидивирующие после хирургического лечения, парапроктит, свищи прямой кишки), внекишечные проявления заболевания [14, 20, 21, 22, 23].
При сборе анамнеза стоит уточнить наличие аутоиммунных проявлений, связанных и не связанных с активностью воспалительного процесса, а также на симптомы, связанные с осложнениями БК. Кроме того, следует уточнить характер начала заболевания, информацию о поездках в южные страны, непереносимости пищевых продуктов, приеме лекарственных препаратов (включая антибиотики и нестероидные противовоспалительные средства (НПВС), курении и семейном анамнезе.
2.2 Физикальное обследование
- Рекомендуется при физикальном обследовании всех пациентов с подозрением на БК кроме общих методов (осмотр, аускультация, перкуссия и пальпация живота) выполнять с целью первичной диагностики:
- осмотр перианальной области
- пальцевое исследование прямой кишки с целью выявления перианальных проявлений БК [29].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Комментарий: при физикальном обследовании могут быть обнаружены различные проявления БК, включая лихорадку, дефицит питания, наличие инфильтрата брюшной полости, наружных кишечных свищей, перианальных проявлений (трещин, свищей), а также внекишечные проявления.
2.3 Лабораторные диагностические исследования
- Рекомендуется всем пациентам с целью определения степени анемии, признаков системного воспаления и метаболических нарушений выполнять определение уровня общего гемоглобина, железа, трансферрина и ферритина, гематокрита, количества эритроцитов, лейкоцитов, тромбоцитов крови и скорости оседания эритроцитов (СОЭ) [24, 29, 30].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется определение уровня C-реактивного белка, общего белка, альбуминов, глюкозы, АЛТ, АСТ, холестерина, K+, Na+, Cl-, щелочной фосфатазы, фибриногена крови [24, 31].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Комментарий: лабораторные проявления БК носят неспецифический характер. При клиническом анализе крови могут быть диагностированы анемия (железодефицитная, анемии хронического заболевания, B-12- или фолат-дефицитная), лейкоцитоз (на фоне хронического воспаления, при наличии абсцесса или на фоне стероидной терапии). Биохимическое исследование позволяет выявить электролитные нарушения, гипопротеинемию (в частности, гипоальбуминемию).
Пациентам с БК при необходимости дифференциальной диагностики анемии рекомендуется исследовать уровень фолиевой кислоты, витамина B-12, сывороточного железа, общую железосвязывающую способность сыворотки, ферритина [236].
Уровень убедительности рекомендации - B (уровень достоверности доказательств - 3)
- Рекомендуется пациентам с БК, при необходимости оценки или мониторинга активности воспаления в кишечнике, выполнять анализ кала на фекальный кальпротектин (ФК) [32, 33, 34, 35].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 2)
- Рекомендуется пациентам с БК, при недавно проведенном курсе антибиотикотерапии или пребывании в стационаре, выполнять копрологическое исследование для исключения острой кишечной инфекции, выполнить исследование кала на токсины A и B Cl. difficile для исключения клостридиальной инфекции [36, 37, 38, 39].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 4)
- Рекомендуется выполнение лабораторного исследования кала для идентификации токсигенной Cl. difficile методами: иммуноферментного анализа с определением токсинов A и B и/или иммунохемилюминесцентного анализа с определением токсинов A и B и/или полимеразной цепной реакции (ПЦР) [237 - 239].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
Комментарий: для выявления инфекции в 90% случаев требуется минимум 4 образца кала [38, 39, 40]. Важным при тяжелой атаке БК является морфологическое исследование биоптатов и/или проведение ПЦР в материале биоптатов слизистой оболочки толстой кишки (из очагов поражения) на наличие цитомегаловирусной инфекции (ЦМВ) [41].
- Пациентам с подозрением на БК, при первичной диагностике рекомендуется выполнять микроскопическое исследование кала на гельминты с применением методов обогащения для исключения паразитарной инфекции [29, 42].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется пациентам с БК, перед назначением лекарственной терапии, выполнить исследование уровня свободного и связанного билирубина, креатинина, мочевины, глюкозы, K+, Na+, общего кальция в крови, определение активности аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, амилазы в крови и общего (клинического) анализа мочи для оценки функции печени, поджелудочной железы и почек [29].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется пациентам со среднетяжелой и тяжелой формой БК, с наличием метаболических нарушений, для оценки динамики состояния выполнять общий (клинический) и биохимический анализ крови 1 раз в 3 - 5 дней [29].
Уровень убедительности рекомендации C (уровень достоверности доказательств - 5)
2.4 Инструментальные диагностические исследования
- Пациентам с подозрением на БК с целью первичной диагностики рекомендуется выполнение ректороманоскопии [29].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Рекомендуется пациентам с симптомами кишечной непроходимости выполнить обзорную рентгенографию брюшной полости [43, 44].
Уровень убедительности рекомендации C (уровень достоверности доказательств - 5)
- Пациентам с БК для определения локализации, протяженности, степени активности воспалительного процесса рекомендовано проведение колоноскопии с исследованием терминального отдела подвздошной кишки и биопсией из зоны патологического процесса [45, 46, 48].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Для оценки эндоскопической активности БК рекомендована к использованию простая эндоскопическая шкала оценки БК (SES-CD) (см. Раздел 2 "Эндоскопические критерии БК") (табл. 6). Для оценки активности послеоперационного рецидива БК применима шкала Rutgeerts (Табл. 7) [49].
- Пациентам при первичной диагностике БК, подозрении на прогрессирование заболевания, при признаках рецидива, а также при ежегодном контроле рекомендовано проведение эзофагогастродуоденоскопии для исключения/подтверждения поражения верхних отделов ЖКТ [50, 51, 52].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Пациентам с БК при необходимости определения локализации, протяженности, степени активности воспалительного процесса, также для выявления абдоминальных инфильтратов, межкишечных и межорганных свищей, перфораций, стриктур рекомендовано проведение магнитно-резонансной томографии (МРТ) и/или компьютерной томографии (КТ) с контрастированием кишечника [53, 54].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
- Пациентам с перианальными проявлениями БК в виде свищей прямой кишки или при подозрении на них, рекомендовано проведение МРТ малого таза с внутривенным контрастированием для подтверждения диагноза, определения локализации, протяженности свищевого хода и наличия/отсутствия осложнений [53, 55, 56].
Уровень убедительности рекомендации A (уровень достоверности доказательств - 1)
Комментарий: целью обследования при перианальных проявлениях БК является, в первую очередь, исключение острого гнойного процесса в параректальной области, требующего срочного хирургического лечения. МРТ является основным методом диагностики конфигурации свищевых ходов и затеков в полости малого таза.
- Пациентам с перианальными проявлениями БК или при подозрении на них, при отсутствии рубцово-воспалительных стриктур анального канала и нижнеампулярного отдела прямой кишки рекомендовано выполнение эндоректального УЗИ (ЭУЗИ) как в B-режиме, так и с трехмерной реконструкцией изображения [57].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
Комментарий: ЭУЗИ (с частотой 5 - 16 МГц) позволяет детально визуализировать свищевой ход и его расположение относительно мышечных структур в 86 - 95% наблюдений, идентифицировать внутренние свищевые отверстия в 62 - 94% случаев. При наличии наружных свищевых отверстий, введение в них перекиси водорода значительно улучшает визуализацию свищевого хода. При наличии острого гнойно-воспалительного процесса и при выраженных болевых ощущениях целесообразно выполнение исследования под обезболиванием. В качестве дополнительного метода при невозможности введения датчика в просвет кишки, возможно применение трансперинеального УЗИ, однако его точность в диагностике глубоко расположенных абсцессов довольно низкая (47,1%) в связи с ограниченным полем зрения [58, 59].
- Пациентам при невозможности проведения КТ или МРТ, после исключения нарушения кишечной проходимости рекомендовано проведение рентгенографии тонкой кишки с контрастированием (с бариевой взвесью) для подтверждения локализации и протяженности воспалительного процесса, межкишечных, межорганных свищей, стриктур [43].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Пациентам с острой атакой БК или при первом обращении рекомендовано проведение биопсии слизистой оболочки кишки в зоне поражения и патолого-анатомическое исследование биопсийного материала для уточнения диагноза [45, 60, 61].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Всем пациентам с БК рекомендовано проведение трансабдоминального УЗИ органов брюшной полости, забрюшинного пространства, малого таза для исключения осложнений основного заболевания и сопутствующей патологии, а также для оценки толщины кишечной стенки, наличия дефектов в зоне поражения, определения степени васкуляризации и других признаков воспаления. При проведении УЗИ целесообразно проводить эластометрию стенки кишки, особенно в зоне сужений для определения ее характера по цветовому картированию (фиброз или воспалительный отек) [62, 63, 64, 65, 66].
Уровень убедительности рекомендации - B (уровень достоверности доказательств - 2)
- Пациентам с подозрением на поражение тощей кишки (при отсутствии участков сужения просвета ЖКТ) и отсутствии достаточной информации о наличии очага воспаления при МРТ, КТ и УЗИ или невозможности их проведения, рекомендовано проведение видеокапсульной эндоскопии для подтверждения диагноза, определения локализации, степени активности воспалительного процесса [67].
Уровень убедительности рекомендации - B (уровень достоверности доказательств - 1)
Комментарий: необходимо помнить, что задержка капсулы в кишечнике наблюдается у 13% пациентов [67].
- Пациентам с БК проведение видеокапсульной эндоскопии рекомендовано при отсутствии сужений по данным МРТ или КТ с контрастированием кишечника [68, 69].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Пациентам с БК, при подозрении на поражение тонкой кишки и невозможности достоверного подтверждения диагноза по данным колоноскопии (с исследованием терминального отдела тонкой кишки), КТ и МРТ с контрастированием кишечника, невозможности проведения видеокапсульного исследования, рекомендована двухбаллонная интестиноскопия, для подтверждения диагноза, определения локализации и степени активности воспалительного процесса и забора биопсии [70].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
2.5 Иные диагностические исследования
Дополнительные инструментальные и лабораторные исследования выполняются, преимущественно, с целью проведения дифференциальной диагностики с рядом заболеваний [71, 72, 73].
Дифференциальный диагноз БК проводится с:
- язвенным колитом
- острыми бактериальными инфекционными колитами (дизентерия, сальмонеллез, кампилобактериоз, иерсиниоз, амебиаз)
- вирусными колитами (прежде всего цитомегаловирусным)
- паразитозами
- гельминтозами
- поражениями кишечника, ассоциированными с Cl.difficile, в том числе вызванными антибиотиками
- туберкулезом кишечника
- системными васкулитами
- ишемической болезнью кишечника (ишемическим колитом, энтеритом)
- раком толстой кишки
- дивертикулитом
- микроскопическими колитами (коллагеновым и лимфоцитарным)
- лучевым колитом (обычно проктитом)
- первичными иммунодефицитными состояниями, имитирующими БК (общий вариабельный иммунодефицит, первичный дефицит IgA)
- лекарственными поражениями кишечника (НПВС).
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1 Консервативное лечение
Лечебные мероприятия при БК включают в себя назначение лекарственных препаратов, хирургическое лечение, психосоциальную поддержку и диетические рекомендации [74].
Глобально цели лечения БК в настоящее время определены стратегией "Treat-to-target (T2T)", что означает "Лечение до достижения цели". Эта концепция направлена на достижение долгосрочного эффекта лечения, профилактики осложнений, уменьшение частоты госпитализаций, снижение риска операций, улучшение качества жизни и снижение частоты инвалидизации у пациентов с хроническими заболеваниями [75, 76].
С точки зрения ежедневной клинической практики целями терапии БК являются достижение и поддержание долговременной бесстероидной клинико-эндоскопической ремиссии [2, 24, 77].
При прогрессировании процесса и/или развитии опасных для жизни осложнений конкретной целью является своевременное проведение хирургического лечения.
В рамках стратегии "T2T" предусмотрен непрерывный мониторинг эффективности лечения путем регулярного исследования биологических маркеров (СРБ, ФК) и проведения эндоскопического и лучевых методов исследования [76, 78].
Варианты лечения пациентов с БК определяются на основании тяжести атаки, протяженности и локализации воспаления в ЖКТ, наличию внекишечных проявлений и кишечных осложнений (стриктура, абсцесс, инфильтрат), длительности анамнеза, эффективности и безопасности ранее проводившейся терапии, а также риска развития осложнений и наличием факторов риска негативного прогноза течения БК.
Факторы негативного прогноза течения БК и риска развития осложнений [79, 80]:
- Возраст пациента < 40 лет при установлении диагноза (раннее начало заболевания, дебют в детском возрасте)
- Распространенное (> 100 см по сумме пораженных сегментов) поражение кишечника
- Потребность в назначении системных ГКС в дебюте
- Наличие перианальных поражений
- Глубокие язвы слизистой оболочки по эндоскопи
- Осложненный фенотип болезни. Стриктурирующая или пенетрирующая БК
- Вовлечение верхних отделов ЖКТ
- Курение (более агрессивное течение)
- Наличие сопутствующих аутоиммунных заболеваний или ВКП
- Наличие гранулем.
Поскольку хирургическое лечение не приводит к полному излечению пациентов с БК даже при радикальном удалении всех пораженных сегментов кишечника, необходимо проведение противорецидивной терапии, которую следует начать не позднее 2 недель после перенесенного оперативного вмешательства [81].
Лекарственные препараты, назначаемые пациентам с БК, условно подразделяются на:
- Средства для индукции ремиссии: системные (преднизолон** и метилпреднизолон**) и топические (будесонид**) ГКС, в комбинации с тиопуринами (АЗА**, #МП**, #МТ** (МТ), ГИБП: ингибиторы фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаб**, адалимумаб** и цертолизумаба пэгол**), ингибиторы интерлейкина 12/23 (устекинумаб**) и селективные кишечные ингибиторы интегрина 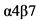 (ведолизумаб**), ТИС (упадацитиниб**), а также антибиотики.
(ведолизумаб**), ТИС (упадацитиниб**), а также антибиотики.
- Средства для поддержания ремиссии (противорецидивные средства): тиопурины (АЗА**, #МП**), #МТ**, ГИБП (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб** и ведолизумаб**) и ТИС (упадацитиниб**).
- Вспомогательные симптоматические средства: препараты для коррекции анемии, препараты для коррекции белковых и электролитных нарушений, средства для профилактики остеопороза (препараты кальция и витамин Д) и др.
Ниже представлены рекомендации по выбору препаратов для индукции и поддержания ремиссии в зависимости от протяженности поражения и тяжести атаки.
3.1.1 Легкая БК илеоцекальной локализации
- Данной группе пациентов в качестве терапии первой линии рекомендуется назначать будесонид** (капсулы кишечнорастворимые с пролонгированным высвобождением, гранулы кишечнорастворимые в саше) [74, 82, 83].
Уровень убедительности рекомендации - B (уровень достоверности доказательств - 1)
Комментарий: при приеме капсул будесонида** суточная доза составляет 9 мг/сут однократно или по 3 мг 3 раза в день в течение 8 недель с последующим снижением по 3 мг в неделю до полной отмены. При приеме гранул суточная доза составляет 9 мг/в сутки однократно в течение 8 недель с последующим снижением по 9 мг через день в течение двух недель. Терапевтический эффект будесонида** следует оценивать через 2 - 4 недели. При отсутствии терапевтического ответа на будесонид** лечение проводится как при среднетяжелой атаке БК. Будесонид** не предусмотрен для проведения поддерживающей терапии, но в случае необходимости максимальная длительность приема препарата может составлять 16 недель [24].
Пероральный прием месалазина** не показал эффективности по сравнению с плацебо для индукции ремиссии и не рекомендуется для использования при БК [24, 61, 84, 85].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 2)
- Данной группе пациентов в качестве противорецидивной терапии рекомендуется раннее (одновременно с будесонидом**) назначение тиопуринов (АЗА** 2 - 2,5 мг/кг в день или #МП** 1,5 мг/кг в день), а при их непереносимости или неэффективности - #МТ** (25 мг/нед. п/к или в/м). Длительность противорецидивной терапии тиопуринами (АЗА**/#МП**) не менее 2 - 4 лет в терапевтических дозах [24, 61, 86, 87, 88].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
Комментарий: поскольку АЗА** начинает действовать через 12 недель, раннее назначение необходимо для того, чтобы начало его действия реализовалось к моменту отмены ГКС.
3.1.2 БК илеоцекальной локализации средней тяжести
- Данной группе пациентов для индукции ремиссии рекомендованы топические ГКС для перорального приема (будесонид** капсулы кишечнорастворимые с пролонгированным высвобождением, гранулы кишечнорастворимые в саше), режим дозирования, сроки оценки эффективности см. в разделе 3.1.1 "Легкая БК илеоцекальной локализации" [74, 82, 83].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 1)
- Данной группе пациентов для индукции ремиссии БК, при отсутствии эффекта от будесонида, при наличии инфильтрата, воспалительного сужения и признаков системного воспаления, рекомендуются ГКС для системного применения (преднизолон** или эквивалентные дозы других ГКС) [89] (Таблица 8).
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
Комментарий: доза преднизолона** при данной локализации и тяжести составляет 1 мг/кг массы тела в сутки до достижения клинического ответа с последующим снижением по 5 мг в 5 - 7 дней до полной отмены, в течение не более 12 недель. Эффективность ГКС оценивается через 2 - 4 недели.
Таблица 8. Длительность действия и эквивалентные дозы ГКС [240, 241].
|
Препарат
|
Длительность действия (t1/2)
|
Эквивалентная доза (мг)
|
|
Гидрокортизон**
|
8 - 12 ч
|
20
|
|
Преднизолон**
|
12 - 36 ч
|
5
|
|
Метилпреднизолон**
|
12 - 36 ч
|
4
|
- Данной группе пациентов при наличии признаков системного воспаления и/или инфильтрата брюшной полости рекомендуются комбинировать системные ГКС в сочетании с антибиотиками [24, 90].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 1)
- Данной группе пациентов в качестве противорецидивной терапии рекомендуется раннее (одновременно с ГКС) назначение тиопуринов (АЗА** 2 - 2,5 мг/кг или #МП** 1,5 мг/кг), а при их непереносимости или неэффективности - #МТ** (25 мг/нед. п/к или в/м). Длительность противорецидивной терапии тиопуринами (АЗА**/#МП**) не менее 2 - 4 лет в терапевтических дозах [24, 61, 86, 87].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
- Группе пациентов с активной БК со стероидорезистентностью, стероидозависимостью, непереносимостью ГКС или при неэффективности/ непереносимости иммуносупрессоров рекомендуется терапия ГИБП (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб**, ведолизумаб**) или ТИС (упадацитиниб**) в виде индукционного (инициирующего) курса с последующим длительным поддерживающим лечением [93, 94, 95, 96].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
Комментарий: Схемы и дозы препаратов для ГИБП и ТИС в рамках индукционного (инициирующего) курса и поддерживающей терапии:
- для инфликсимаба** индукционный (инициирующий) курс предусматривает трехкратное введение на 0, 2 и 6 неделе внутривенно в дозе 5 мг/кг массы тела, затем такая же доза для поддерживающей терапии 1 раз в 8 недель;
- для адалимумаба** индукционный (инициирующий) курс состоит из первого подкожного введения в дозе 160 мг, затем второго подкожного введения через 2 недели в дозе 80 мг, затем - поддерживающая терапия в дозе 40 мг каждые 2 недели;
- для цертолизумаба пэгол** индукционный (инициирующий) курс состоит из первого подкожного введения 400 мг, второго подкожного введения на 2 неделе в дозе 400 мг, третьего подкожного введения препарата в той же дозировке на 4 неделе лечения, далее поддерживающая терапия проводится в той же дозировке, подкожно каждые 4 недели;
- для ведолизумаба** индукционный (инициирующий) курс предусматривает трехкратное введение на 0, 2 и 6 неделе внутривенно в дозе 300 мг, затем поддерживающее лечение по 300 мг внутривенно каждые 8 недель;
- для устекинумаба** индукционная (инициирующая) доза вводится внутривенно в первый день с расчетом дозы по массе тела пациента на момент введения, далее через 8 недель - первое поддерживающее подкожное введение в дозе 90 мг и далее - терапия в дозе 90 мг подкожно каждые 8 или 12 недель (в зависимости от характера течения заболевания);
- для упадацитиниба** 12-недельный индукционный (инициирующий) курс в дозе 45 мг в таблетках 1 раз в сутки и затем 30 мг или 15 мг (в зависимости от характера течения заболевания) в таблетках 1 раз в сутки в качестве поддерживающей терапии.
Все ГИБП и ТИС примерно одинаковы по эффективности, поэтому у бионаивных пациентов любой из указанных препаратов может быть использован в качестве первой линии терапии. Однако оптимальная последовательность назначения ГИБП и ТИС пока не установлена. В значительной степени выбор первого препарата зависит от индивидуальных особенностей пациента и наличия факторов риска негативного прогноза заболевания. Тем не менее, следует иметь в виду, что все ГИБП более эффективны в первой линии у бионаивных пациентов. Каждый дополнительный ГИБП статистически значимо снижает вероятность достижения клинической, эндоскопической и бесстероидной ремиссии [97]. Некоторые из ГИБП и ТИС сохраняют эффективность во 2 и последующих линиях терапии (устекинумаб**, упадацитиниб**) [98, 99, 100].
Кроме того, при выборе разных классов препаратов следует учитывать, что устекинумаб** и адалимумаб** продемонстрировали сопоставимую эффективность в 1-ой линии терапии, но в группе адалимумаба** частота прекращения лечения из-за нежелательных явлений была почти вдвое больше, чем в группе устекинумаба** [101].
Отсутствие первичного ответа на терапию определяется после индукционного курса (в зависимости от препарата). При наличии отрицательной динамики эффективность препарата оценивается раньше.
- Пациентам, достигшим ремиссии при лечении любым из ГИБП или ТИС рекомендуется проводить поддерживающую терапию тем же препаратом (с иммуносупрессорами или без них) [24, 61, 85, 102].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
- Пациентам с активной БК рекомендуется комбинировать назначение инфликсимаба** с тиопуринами для повышения эффективности лечения [85, 88, 103].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
Комментарий: для других ГИБП целесообразность такой комбинации не доказана. Назначение комбинированной терапии остается на усмотрение лечащего врача.
- Пациентам с активной БК с непереносимостью/отсутствием эффекта от тиопуринов рекомендовано использование инфликсимаба** в комбинации с #метотрексатом** (#МТ** 25 мг/нед. п/к или в/м) [61, 85, 104].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
- Пациентам при первичной неэффективности любого из анти-ФНО препаратов рекомендуется смена терапии на ведолизумаб**, устекинумаб**, упадацитиниб** для индукции ремиссии [253, 254, 255, 256].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
Комментарий: любой из указанных препаратов может быть назначен в качестве 2-ой и последующих линий терапии на фоне ГКС или без них. При выборе ведолизумаба после анти-ФНО следует иметь в виду, что его эффективность в качестве препарата 2-ой линии ниже, чем в 1-й линии [105, 106].
- Пациентам при потере ответа на анти-ФНО препараты в 1-ой линии терапии (рецидив БК на фоне ранее достигнутой ремиссии) рекомендуется оптимизация терапии в виде увеличения дозы препарата (10 мг/кг инфликсимаба** каждые 8 недель, 80 мг адалимумаба каждые 2 недели) или сокращение интервалов между введениями (инфликсимаб** до 4 - 6 недель, адалимумаб** 40 мг каждую неделю) или назначение препаратов другого механизма действия: ведолизумаба**, устекинумаба** упадацитиниба** для достижения терапевтического эффекта [107, 108, 109].
Уровень убедительности рекомендации A (уровень достоверности доказательств - 2)
Комментарий: смена на другой анти-ФНО препарат допустима, но ее эффективность ниже, чем при переходе на препараты других классов (ведолизумаб**, устекинумаб**, упадацитиниб**) [107, 111]. Для повышения эффективности лечения при переключении на другой анти-ФНО возможна комбинация с иммуносупрессорами [108, 109]. При выборе ведолизумаба** следует иметь в виду, что его эффективность в качестве препарата первой линии выше, чем во второй и последующих линиях [110].
- Пациентам при потере ответа на ведолизумаб** в стандартной дозе 300 мг каждые 8 недель рекомендуется оптимизация терапии в виде сокращения интервалов между введениями до 4 - 6 недель или смена на препарат другого класса (анти-ФНО, устекинумаб**, упадацитиниб**) [105, 110].
Уровень убедительности рекомендации C (уровень достоверности доказательств - 4)
Комментарий: эффективность анти-ФНО во 2-й линии терапии после потери ответа на ведолизумаб** не снижается по сравнению с их эффективностью в 1-ой линии, т.е. применение ведолизумаба** не влияет на последующую эффективность анти-ФНО [110].
- Пациентам при потере ответа на устекинумаб** в стандартном режиме введения каждые 12 недель рекомендуется оптимизация терапии в виде сокращения интервалов между введениями до 8 недель или смена на препарат другого класса (анти-ФНО, ведолизумаб**, упадацитиниб**) [85].
Уровень убедительности рекомендации C (уровень достоверности доказательств - 5)
- При первичной неэффективности или потере ответа на упадацитиниб** рекомендуется оптимизация лечения с увеличением поддерживающей дозы с 15 мг до 30 мг или смена на другой класс препарата [233].
Уровень убедительности рекомендации C (уровень достоверности доказательств - 4)
- Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [61].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
3.1.3 БК толстой кишки легкой и средней тяжести
Данной группе пациентов рекомендуется терапия системными ГКС (преднизолон** или эквивалентные дозы других ГКС) [89, 91].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
Комментарий: доза преднизолона** при данной локализации и тяжести составляет 0,75 - 1 мг/кг массы тела в сутки до достижения клинического ответа с последующим снижением по 5 мг в 5 - 7 дней до полной отмены, в течение 12 недель. Эффективность ГКС оценивается через 2 - 4 недели.
- Данной группе пациентов одновременно с системными ГКС рекомендуется назначить тиопурины (АЗА** 2 - 2,5 мг/кг или #МП** 1,5 мг/кг), а при их непереносимости или неэффективности - #МТ** (25 мг/нед п/к или в/м 1 раз в неделю) [86, 87, 102].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
- Данной группе пациентов в случае наличия признаков активного системного воспаления и/или наличии инфильтрата рекомендуется добавить антибиотики в схему лечения [61, 85, 90].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
Терапия иммуносупрессорами, ГИБП и ТИС см. раздел 3.1.2 "БК илеоцекальной локализации".
- Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [61].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
3.1.4 БК тонкой кишки (кроме терминального илеита)
- Пероральный прием месалазина** не показал эффективности по сравнению с плацебо для индукции ремиссии и не рекомендуется для использования при БК [24, 61, 79, 84, 85].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 2)
- Данной группе пациентов рекомендуются системные ГКС (преднизолон** или эквивалентные дозы других ГКС) [24, 85, 89, 91].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
Комментарий: доза преднизолона** при данной локализации и тяжести составляет 1 мг/кг массы тела в сутки до достижения клинического ответа с последующим снижением по 5 мг в 5 - 7 дней до полной отмены, в течение не более 12 недель. Эффективность ГКС оценивается через 2 - 4 недели.
- Данной группе пациентов рекомендуется одновременно с системными ГКС назначение тиопуринов (АЗА** 2 - 2,5 мг/кг или #МП** 1,5 мг/кг), а при их непереносимости или неэффективности - #МТ** (25 мг/нед п/к или в/м 1 раз в неделю). Длительность противорецидивной терапии тиопуринами (АЗА**/#МП**) не менее 2 - 4 лет в терапевтических дозах [24, 61, 86, 87].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
- Данной группе пациентов, при наличии признаков системного воспаления и/или наличии инфильтрата рекомендуется антибактериальная терапия: #метронидазол 1 г/день + фторхинолоны 1 г/день парентерально 10 - 14 дней [24, 61, 90].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
Терапия иммуносупрессорами, ГИБП и ТИС см. раздел 3.1.2 "БК илеоцекальной локализации"
- Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [61].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
3.1.5 Тяжелое течение активной БК любой локализации
Тяжелое течение БК оценивается по индексу Харви-Брэдшоу как > 16 баллов (табл. 3) (см. раздел 1.5 "Классификация заболевания или состояния (группы заболеваний или состояний)").
Пациентам с тяжелым течением БК рекомендуются начинать лечение с системных ГКС (преднизолон** или эквивалентные дозы других ГКС) внутривенно или перорально. Эквивалентность доз и длительность действия ГКС приведена в таблице 7 (см. раздел 3.1.2 "БК илеоцекальной локализации средней тяжести") [89, 91].
Уровень убедительности рекомендации - A (уровень достоверности доказательств - 1)
Комментарий: доза преднизолона** при данной тяжести составляет 1,5 - 2 мг/кг массы тела в сутки до достижения клинического ответа с последующим снижением по 5 мг в 5 - 7 дней до полной отмены, в течение не более 12 недель. Эффективность ГКС оценивается через 2 - 4 недели.
- Данной группе пациентов рекомендуется одновременно с системными ГКС назначение тиопуринов (АЗА** 2 - 2,5 мг/кг или #МП** 1,5 мг/кг), а при их непереносимости или неэффективности - #МТ** (25 мг/нед п/к или в/м 1 раз в неделю). Длительность противорецидивной терапии тиопуринами (АЗА**/#МП**) не менее 2 - 4 лет в терапевтических дозах [24, 61, 86, 87].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
- Данной группе пациентов, при наличии признаков системного воспаления и/или наличии инфильтрата рекомендуется антибактериальная терапия: #метронидазол 1 г/день + фторхинолоны 1 г/день парентерально 10 - 14 дней [24, 61, 90, 112].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 1)
- Данной группе пациентов при раннем рецидиве заболевания менее 3 месяцев после достижения клинической ремиссии рекомендуется сразу начинать с ГИБП или ТИС без повторного назначения системных ГКС [24, 74].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: Повторные курсы ГКС крайне нежелательны. ГКС допустимо применять только при невозможности применения ГИБП или ТИС.
Терапия иммуносупрессорами, ГИБП и ТИС см. раздел 3.1.2 "БК илеоцекальной локализации"
- Пациентам с активной БК при неэффективности консервативной терапии рекомендовано хирургическое лечение [61].
Уровень убедительности рекомендации - C (уровень достоверности доказательств
3.1.6 БК с перианальными поражениями
Перианальные поражения при БК часто требуют хирургического лечения, которое рассматривается в Разделе 3.2.6 "Хирургическое лечение перианальной БК".
- У всех пациентов с перианальным поражением БК в случае отсутствия показаний к хирургическому лечению или после него рекомендовано назначение иммуносупрессоров (АЗА**, #МП**, #МТ**) и/или ГИБП (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб**, ведолизумаб**) или ТИС (упадацитиниб**) в виде индукционного (инициирующего) курса с последующим длительным поддерживающим лечением [58, 113, 114, 115].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- Пациентам с перианальными поражениями БК с целью лечения гнойно-воспалительного процесса рекомендовано назначение #метронидазола** 0,75 г/сут и/или #ципрофлоксацина** 1 г/сут [24, 116].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 2)
Комментарий: антибиотики назначаются длительно (до 6 месяцев или до появления побочных эффектов). Проведение комбинированной терапии анти-ФНО (инфликсимаб**, адалимумаб**) с антибактериальными препаратами повышает их эффективность [116, 117, 118, 119, 120].
- У пациентов с перианальными проявлениями БК рекомендовано подключение к терапии #метронидазола** в виде свечей и мазей [116, 117].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- У пациентов с перианальными проявлениями БК, при наличии трещин анального канала хирургическое вмешательство не рекомендуется, а отдается предпочтение вышеописанному местному консервативному лечению [24, 58, 116].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
3.1.7 Мониторинг эффективности и побочных эффектов лекарственной терапии
В период терапии ГКС пациенты нуждаются в мониторинге уровня глюкозы крови.
В период терапии иммуносупрессорами необходимы контрольные общие анализы крови и биохимические анализы крови с учетом уровня лейкоцитов и печеночных ферментов (в начале лечения раз в две недели, далее раз в месяц в течение первых 6 месяцев терапии, далее раз в три месяца).
Кроме того, перед проведением ГИБТ и ТИС и далее каждые 6 месяцев согласно приказу Минздрава России (N 124н от 21.03.2017 "Об утверждении порядков и сроков проведения профилактических медицинских осмотров граждан в целях выявления туберкулеза) обязательными являются консультация врача-фтизиатра и скрининг на туберкулез (квантифероновый тест, а при невозможности проведения - внутрикожная проба с туберкулезным аллергеном: проба Манту, диаскин-тест).
- Пациентам до назначения лечения иммуносупрессорами, ГИБП и ТИС на фоне лечения рекомендуется проводить определение антигена (HBsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител вируса гепатита C (Hepatitis C virus) в крови; определение антител к бледной трепонеме (Treponema pallidum) иммуноферментным методом (ИФА) в крови или определение антител к бледной трепонеме (Treponema pallidum) в нетрепонемных тестах (RPR, РМП) (качественное и полуколичественное исследование) в сыворотке крови; определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1) в крови; определение антител классов M, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2 (Human immunodeficiency virus HIV 2) в крови [121, 242, 243].
Уровень убедительности рекомендаций - C (уровень достоверности доказательств - 5)
- Рекомендуется строгое соблюдение доз и графика введения ГИБП и ТИС. Нерегулярное введение ГИБП и ТИС повышает риск аллергических реакций и неэффективности лечения [24, 61, 122].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 2)
- Рекомендуется пациентам при уровне гемоглобина ниже 80 г/л коррекция анемии в виде гемотрансфузии (эритроциты), при уровне гемоглобина от 80 до 100 г/л - терапия препаратами железа парентерально (железа (III) гидрооксид сахарозный комплекс**, железа (III) гидроксид декстрана, железа (III) гидроксид олигоизомальтозат, железа карбоксимальтозат**) [30].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
3.1.8 Биосимиляры (Биоаналоги)
Биосимиляры - это биологические лекарственные средства, содержащие версию активного вещества, уже разрешенного оригинального биологического лекарственного средства (эталонного препарата) [123]. В настоящее время рынок биосимиляров постоянно расширяется. Применительно к ВЗК это пока касается биоаналогов на основе моноклональных антител к ФНО-альфа. Только в Европе в последнюю декаду были зарегистрированы 21 биосимиляр, из них 14 на основе адалимумаба и 4 на основе инфликсимаба [124]. В РФ также зарегистрированы биосимиляры инфликсимаба и адалимумаба. Применение биосимиляров снижает экономическую нагрузку на систему здравоохранения и, тем самым, значительно расширяет возможности использования и доступность ГИБП. Сейчас существует достаточная доказательная база по эффективности и безопасности биосимиляров, однако среди клиницистов остается предубеждение против них, как препаратов с более низкой эффективностью [125]. Европейская организация по изучению ВЗК (ЕССО) в 2017 г декларировала позицию по использованию биоаналогов при ВЗК, в которой подчеркивается, что после регистрации биоаналог считается таким же эффективным препаратом, как и оригинальный продукт, а для оценки его долговременной эффективности и безопасности требуются большие наблюдательные исследования [126]. Именно с этих позиций систематический обзор 90 исследований при разных иммуно-воспалительных заболеваниях 2018 года показал, что в подавляющем большинстве исследований не наблюдалось различий в безопасности, эффективности или иммуногенности между биоаналогами и соответствующими оригинальными препаратами, что свидетельствует о сохранении хорошего профиля польза-риск при переходе с оригинального препарата на биоаналог [127]. Реальная клиническая практика европейских стран и США демонстрирует сходную эффективность, безопасность и иммуногенность при переключении пациентов ВЗК с оригинального инфликсимаба на его биоаналоги [128, 129, 130, 131, 132]. Лишь в одном исследовании в 9,9% случаев фиксировали необходимость обратного переключения с биосимиляра на эталонный препарат вследствие нежелательных проявлений со стороны кожи, желудочно-кишечного тракта или из-за потери ответа на препарат. У подавляющего большинства больных ответ на лечение после обратного переключения восстановился [130]. Сравнение адалимумаба и двух его аналогов у больных ВЗК в Италии не показало значимой разницы в эффективности, безопасности и иммуногенности между препаратами после индукционного курса и после 6 мес поддерживающего лечения [133]. Результаты долгосрочного постмаркетингового наблюдения за эффективностью и безопасностью биосимиляров на основе моноклональных антител в течение 7 лет не выявили каких-либо побочных эффектов, специфичных для биосимиляров [134]. ЕССО консенсус подчеркивает, что принятие решения о переходе с оригинального препарата на биоаналог по не медицинским показаниям должно проводиться в соответствии с национальными клиническими рекомендациями и вся информация должна быть доведена до сведения пациента и объяснена ему [126].
Несмотря на достаточно четко сформулированные утверждения относительно биосимиляров, существуют и определенные противоречия в этом вопросе, согласно которым принятые положения основаны на исследованиях с разными методологическими подходами и недостаточным числом наблюдений, что ограничивает их достоверность [234].
Российские публикации свидетельствуют, что частота вторичной потери ответа и нежелательных явлений у пациентов с ВЗК при переводе с оригинального инфликсимаба на его биосимиляр составляет около 30%, что достоверно выше, чем у тех, кто постоянно получает оригинальный препарат. Кроме того, частота нежелательных явлений достоверно выше у больных, получающих препарат по МНН, что ведет к неоправданному и нерегулируемому чередованию оригинального препарата и биоаналогов по сравнению с больными, получающими препараты по торговому наименованию [235].
В Российские клинические рекомендации по БК положение о биосимилярах вносится впервые. Поскольку российские биосимиляры не представлены на зарубежном рынке, то международные данные об успешном опыте переключения будут иметь для России ограниченную применимость. Поэтому следует с осторожностью экстраполировать эти данные на отечественную клиническую практику.
- Рекомендуется при наличии показаний к назначению ГИБП класса ингибиторов фактора некроза опухоли альфа (ФНО-альфа) (инфликсимаба** и адалимумаба**) использовать как оригинальный препарат, так и его биоаналоги, как равноценные лекарственные средства [125, 126].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Комментарий: это положение касается в равной мере как первичного назначения анти-ФНО препаратов у бионаивных пациентов, так и при переключении с оригинального препарата на биоаналог и обратно по немедицинским показаниям. Однако, следует иметь в виду, что неконтролируемое переключение с оригинала на биосимиляр или разные биосимиляры и обратно по МНН может привести к ухудшению течения заболевания, быстрой потере ответа и нежелательным явлениям. Переход с одного анти-ФНО препарата на другой в рамках одного класса при потере ответа на первый препарат не рекомендуется ни для оригинальных препаратов, ни для биосимиляров. Достаточной доказательной базы для использования биоаналогов лекарственных препаратов других классов для лечения БК пока нет.
3.2 Хирургическое лечение БК
Большинство пациентов с БК в течение жизни переносят хотя бы одно оперативное вмешательство на ЖКТ. Невозможность радикального излечения пациентов с БК нередко приводит к повторным резекциям, увеличивая риск синдрома короткой кишки. Современная тактика хирургического лечения БК направлена на выполнение ограниченных резекций, а при возможности - проведение органосохраняющих вмешательств (стриктуропластика, дилатация стриктур) [135].
Предоперационный прием глюкокортикостероидов в дозе более 20 мг в сутки ассоциирован с увеличением послеоперационных септических осложнений [136].
У пациентов с БК, перенесших хирургическое лечение, применение биологической терапии (препараты анти-ФНО, ведолизумаба** или устекинумаба**) в анамнезе не ассоциировано с увеличением послеоперационных септических осложнений. [137, 138, 139, 140, 141, 142].
Прекращение приема указанных препаратов перед операцией не является обязательным.
Прием иммуномодуляторов перед хирургическим вмешательством не ассоциирован с увеличением послеоперационных септических осложнений [143, 144].
3.2.1 Показания к хирургическому лечению БК
Показаниями к оперативному вмешательству при БК служат острые и хронические осложнения, а также неэффективность консервативной терапии и задержка физического развития [135].
Острые осложнения БК.
К острым осложнениям БК относят кишечное кровотечение, перфорацию кишки и токсическую дилатацию ободочной кишки.
- При кишечном кровотечении экстренное хирургическое вмешательство рекомендуется при невозможности стабилизировать гемодинамику пациента, несмотря на переливание эритроцитарной массы и проведение интенсивной гемостатической терапии [145, 146].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
Комментарий: кишечное кровотечение констатируют при потере более 100 мл крови/сутки по данным объективных лабораторных методов (сцинтиграфия, исследование кала на скрытую кровь, экспресс-исследование кала на скрытую кровь иммунохроматографическим методом) или при объеме каловых масс с визуально определяемой примесью крови более 800 мл/сутки. В подобных случаях выполняется резекция пораженного участка кишечника (с наложением анастомоза или без такового, а также с возможным формированием стом) с обязательной интраоперационной энтеро- или колоноскопией [147].
- У пациентов с осложненной формой БК, в случае перфорации тонкой/ободочной кишки в свободную брюшную полость, с развитием острого перитонита, рекомендовано экстренное хирургическое вмешательство с резекцией пораженного отдела кишечника, предпочтительно, с формированием кишечной стомы [148, 149].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
Комментарий: формирование кишечной стомы, как альтернатива первичному анастомозу, при осложненной БК и контаминации брюшной полости, вследствие перфорации в свободную брюшную полость, позволяет снизить риски септических осложнений и рецидива БК. У пациентов с локализацией БК в тонкой кишке ее перфорация в свободную брюшную полость является достаточно редким осложнением и обычно возникает либо дистальнее, либо проксимальнее участка кишки с наличием стриктуры. В случае экстренной операции рекомендовано избегать формирования первичного анастомоза без протекции при помощи двуствольной илеостомы [150].
- У пациентов с локализацией БК в толстой кишке, при развитии токсической дилатации, операцией выбора рекомендуется субтотальная колэктомия с одноствольной илеостомией [150].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
Комментарий: токсическая дилатация ободочной кишки является редким осложнением при БК и представляет собой не связанное с обструкцией расширение ободочной кишки до 6,0 см и более с явлениями интоксикации. К факторам риска токсической дилатации относятся гипокалиемия, гипомагниемия, подготовка кишки к колоноскопии при помощи осмотических слабительных и прием антидиарейных препаратов. О развитии токсической дилатации свидетельствует внезапное сокращение частоты стула на фоне имевшейся диареи, вздутие живота, а также внезапное уменьшение или исчезновение болевого синдрома и нарастание симптомов интоксикации (нарастание тахикардии, снижение АД). При развитии перфорации толстой кишки у пациентов с осложненным течением БК, в тяжелом состоянии и с метаболическими нарушениями, допустима экстериоризация пораженного участка.
Хронические осложнения БК.
Хронические осложнения включают стриктуры, инфильтрат брюшной полости, внутренние или наружные кишечные свищи и наличие неоплазии [151].
Также к хроническим осложнениям следует отнести задержку физического развития, вследствие неадекватной лекарственной терапии, чаще всего возникающая при поражении верхних отделов ЖКТ.
3.2.2 Хирургическое лечение БК в форме терминального илеита или илеоколита
- Пациенту с клинической картиной острого аппендицита, при ревизии брюшной полости и выявлении макроскопически неизмененного червеобразного отростка и терминального илеита, рекомендовано воздержаться от выполнения аппендэктомии, а также резекции кишки или илеоцекальной резекции кишечника [149, 152].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: иногда дебют болезни Крона в виде терминального илеита может протекать под маской острого аппендицита, что приводит к госпитализации пациента в стационар общехирургического профиля и нередко к аппендэктомии и неоправданной резекции пораженного отдела подвздошной кишки [153, 154]. В клинических рекомендациях Российского общества хирургов 2020 года такая ситуация описывается как "вторичный аппендицит". В таком случае настоятельно рекомендуется воздержаться от выполнения аппендэктомии при отсутствии в червеобразном отростке макроскопических признаков вторичного воспаления. Проспективные исследования на эту тему отсутствуют. В 2021 году опубликован систематический обзор Quaresma A.B., основанный на данных 6 ретроспективных исследований, большинство из которых являются описанием клинических случаев. В результате проведенного обзора авторы не рекомендуют выполнение аппендэктомии и первичной резекции подвздошной кишки при неосложненной БК [155]. Важно отметить, что данная рекомендация согласуется с положением консенсуса панели экспертов Европейской организации по изучению ЯК и БК (ЕССО) и Европейской ассоциации колопроктологов (ESCP) [152, 156].
- У пациентов с пенетрирующей формой БК с формированием абсцесса брюшной полости рекомендуется его дренирование под контролем УЗИ или КТ с последующей консервативной терапией (антибактериальная, гормональная терапия и ГИБТ) в качестве альтернативы хирургическому лечению резекционным методом [149, 152, 157].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: дренирование абсцесса брюшной полости и последующая консервативная терапия служат неким мостом к резекционным методам лечения, позволяющим сократить объем оперативного вмешательства ввиду уменьшения размеров воспалительных изменений. Также важно отметить, что тактика консервативного лечения после проведенного дренирования, снижает вероятность несостоятельности межкишечного анастомоза, образования наружных кишечных свищей и необходимость формирования кишечной стомы после плановой резекции кишки [158, 159, 160]. В том числе, в метаанализе He X., et al. выявлено значимое снижение вероятности послеоперационных осложнений (ОШ = 0,44; 95% CI 0,23 - 0,83; p = 0,03) [161]
В случае выполнения первичной резекции кишки в условиях инфильтрата и абсцесса брюшной полости при БК, возрастает объем оперативного вмешательства, что в последующем может привести к синдрому короткой кишки [162]. Важно подчеркнуть, что по данным систематического обзора Clancy C., et al., дренирование абсцесса в сочетании с консервативной терапией позволило избежать хирургического лечения резекционным методом более чем у 30% пациентов [157].
- У пациентов данной группы при формировании стриктуры подвздошной кишки или илеоцекального клапана в качестве операции выбора рекомендуется резекция илеоцекального угла с формированием илео-асцендоанастомоза или стом [163, 164].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
Комментарий: приблизительно 1/3 всех пациентов с БК имеет подобную локализацию, которая часто осложняется формированием стриктуры подвздошной кишки или илеоцекального клапана. При этом решающим фактором для отказа от выполнения первичного анастомоза является наличие нарушения кишечной проходимости.
- У пациентов данной группы, при выявлении стриктуры после первого курса консервативного лечения (т.е. применения кортикостероидов) в качестве первого этапа лечения рекомендуется резекция пораженного участка кишки, а не повторный курс консервативной (гормональной) терапии [165].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- У пациентов с активной БК с формированием абсцесса брюшной полости рекомендуется назначение антибиотиков, а также дренирование абсцесса или резекция пораженного участка [157, 161].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: дренирование может осуществляться хирургическим путем или, в специализированных центрах и при наличии достаточной квалификации - путем чрескожного дренирования. Последний вариант может применяться только при отсутствии стриктуры пораженного участка кишечника, что определяет необходимость резекции пораженного отдела.
- У пациентов с осложненной формой БК, при наличии непротяженных стриктур тощей или подвздошной кишки, включая стриктуры анастомоза после предшествовавшей резекции, альтернативой резекции рекомендовано выполнение рассечения рубцовых стриктур тонкой кишки (стриктуропластики), позволяющей избежать обширных резекций тонкой кишки [166].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: выполнение данного вмешательства возможно при длине стриктуры не более 10 см. Противопоказаниями к стриктуропластике служат наличие инфильтрата, абсцесса, злокачественных образований в стенке кишки или активное кровотечение и выраженное воспаление пораженного участка.
- При наличии непротяженной стриктуры (менее 4 см) тощей или подвздошной кишки, включая стриктуры анастомоза после предшествовавшей резекции без инфильтрата, гнойных полостей, межкишечных свищей без признаков острой кишечной непроходимости, альтернативой резекции и стриктуропластики может быть баллонная дилатация зоны сужения при расположении в отделе, достижимом эндоскопу [167].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 2)
Комментарий: выполнение эндоскопической баллонной дилатации позволяет избежать хирургического вмешательства резекционным методом. Балонная дилатация более эффективна и безопасна при диагностике не более 4 стриктур, расположенных в непосредственной близости друг от друга, чем в случаях множественных стриктур. Не рекомендуется выполнение баллонной дилатации при наличии протяженной стриктуры (более 4 см), межкишечных свищей, гнойных полостей, глубоких изъязвлений в области стриктур, а также престенотического расширения.
- У пациентов данной группы, при отсутствии инфильтрата и абсцесса рекомендовано выполнение хирургического вмешательства на тонкой кишке и илеоцекальной зоне лапароскопическим способом [168, 169, 170, 171].
Уровень убедительности рекомендации - A (уровень достоверности рекомендации - 2)
Комментарий: одномоментное формирование более одного анастомоза не приводит к увеличению частоты послеоперационных осложнений и частоты рецидива заболевания [172]. Предпочтительной методикой формирования анастомоза на тонкой кишке является наложение аппаратного анастомоза по типу "бок-в-бок", что уменьшает вероятность его несостоятельности [173] и последующего развития стриктуры.
3.2.3 Хирургическое лечение БК толстой кишки
- У пациентов данной группы, при ограниченном поражении толстой кишки рекомендуется резекция пораженного сегмента с формированием кишечного анастомоза в пределах здоровых тканей [174, 175].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: пациентам с ограниченным поражением толстой кишки (менее трети толстой кишки), при развитии осложнений БК, не требуется колэктомии. При наличии поражения в восходящем отделе ободочной кишки, в силу анатомических особенностей показана правосторонняя гемиколэктомия (с сохранением терминального отдела подвздошной кишки). При поражении левого изгиба и/или нисходящей ободочной кишки выполняется левосторонняя гемиколэктомия с формированием трансверзосигмоидного анастомоза или стомы. При локализации БК в сигмовидной кишке выполняется резекция пораженного участка.
- У пациентов с распространенной БК толстой кишки с тяжелыми клиническим проявлениями, в качестве операции выбора рекомендуется субтотальная колэктомия с наложением одноствольной илеостомы [74, 176].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: дистальную часть толстой кишки возможно не резецировать при условии отсутствия в ней выраженного воспаления и вывести на переднюю брюшную стенку в виде одноствольной сигмостомы, или ушить культю прямой кишки наглухо.
- У пациентов с поражением всей толстой кишки, а также наличием выраженного воспаления в прямой кишке и тяжелыми перианальными поражениями в качестве альтернативной операции рекомендуется колэктомия с брюшно-анальной резекцией прямой кишки и формированием концевой одноствольной илеостомы [74].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: данное вмешательство выполняется только у пациентов с выраженной активностью воспалительного процесса в прямой кишке или тяжелыми перианальными проявлениями, поскольку делает невозможным дальнейшее восстановление анальной дефекации.
- У пациентов с тяжелыми перианальными поражениями не рекомендована брюшно-промежностная экстирпация [149].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: экстирпация прямой кишки нецелесообразна в связи с крайне низкими репарационными возможностями и риском формирования обширных промежностных ран, которые в дальнейшем длительно заживают вторичным натяжением, что инвалидизирует пациентов и ограничивает их социальную активность.
- При хирургическом лечении БК толстой кишки с гнойно-септическим процессом в параректальной области и промежности резекцию прямой кишки рекомендовано выполнять в объеме тотальной мезоректумэктомии [149, 177].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: в последнее время накопились данные о том, что при БК брыжейка кишки играет ключевую роль в патогенезе воспалительного процесса в кишечной стенке. Так, по данным de Groof et al., мезоректальная клетчатка содержит повышенное количество активированных CD14+макрофагов, продуцирующих 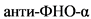 , а также сниженную концентрацию маркера заживления ран CD206 по сравнению с аналогичной тканью при ЯК. Эти фундаментальные данные также имеют практическое значение, поскольку выполнение тотальной мезоректумэктомии, в сравнении с резекцией прямой кишки вдоль стенки с оставлением клетчатки в полости малого таза, сопровождается меньшей частотой послеоперационных осложнений в области промежности, включая рецидив БК: 17,6% и 59,5%, p = 0,007 [177]. Важно заметить, что речь идет о БК с выраженными перианальными проявлениями, гнойно-септическим процессом в области промежности. Решение о необходимости выполнения мезоректумэктомии в других ситуациях остается на усмотрение оперирующего хирурга.
, а также сниженную концентрацию маркера заживления ран CD206 по сравнению с аналогичной тканью при ЯК. Эти фундаментальные данные также имеют практическое значение, поскольку выполнение тотальной мезоректумэктомии, в сравнении с резекцией прямой кишки вдоль стенки с оставлением клетчатки в полости малого таза, сопровождается меньшей частотой послеоперационных осложнений в области промежности, включая рецидив БК: 17,6% и 59,5%, p = 0,007 [177]. Важно заметить, что речь идет о БК с выраженными перианальными проявлениями, гнойно-септическим процессом в области промежности. Решение о необходимости выполнения мезоректумэктомии в других ситуациях остается на усмотрение оперирующего хирурга.
- У пациентов с тотальным поражением толстой кишки, при отсутствии тяжелых клинических проявлений и минимальной активностью воспалительных изменений в прямой кишке, адекватной функции держания кишечного содержимого и отсутствии перианальных поражений, в качестве операции выбора рекомендована колэктомия с формированием илео-ректального анастомоза [91].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: возможность формирования тонкокишечного резервуара (илео-анального резервуарного анастомоза (ИАРА)) при БК толстой кишки является спорной в связи с высокой частотой осложнений и частым возникновением показаний к удалению резервуара. В то же время средняя продолжительность жизни пациентов после формирования ИАРА без постоянной илеостомы достигает 10 лет, что имеет значение для молодых работоспособных пациентов [178]. Основные проблемы, угрожающие пациенту с ИАРА на фоне БК, это развитие перианальных поражений и развитие БК в тонкокишечном резервуаре.
- У пациентов с локализацией БК в толстой кишке формирование илеостомы (отключающей двуствольной стомы) с целью прекращения транзита кишечного содержимого по толстой кишке рекомендовано только у крайне истощенных пациентов и у беременных женщин [168].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: данный вид хирургического лечения является временным. Учитывая, что при БК отключение пассажа по толстой кишке не всегда является эффективным, в последующем необходимо вновь обсуждать вопрос об объеме оперативного вмешательства после проведения точной дифференциальной диагностики между БК толстой кишки и ЯК.
Все перечисленные хирургические вмешательства возможно безопасно выполнить с использованием лапароскопических технологий [174, 180].
- У пациентов с локализацией БК в толстой кишке при выявлении непротяженной стриктуры рекомендовано выполнение балонной дилатации стенозов толстой кишки (эндоскопическим способом) [167, 181, 182, 183].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: данная манипуляция связана с более высоким риском рецидива заболевания по сравнению с резекцией пораженного участка кишечника.
- У пациентов с локализацией БК в толстой кишке выполнение рассечения рубцовых стриктур (стриктуропластики) не рекомендуется [165, 184, 185].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 2)
3.2.4 Хирургическое лечение БК с поражением верхних отделов ЖКТ
- У пациентов данной группы, при наличии единичных или множественных непротяженных стриктур, в качестве операций выбора рекомендуются различные варианты рассечения рубцовых стриктур тонкой кишки (стриктуропластики) [64, 149, 184, 185, 186].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 2)
Комментарий: вовлечение в воспалительный процесс участка кишечника проксимальнее терминального отдела подвздошной кишки часто приводит к формированию множественных стриктур и межкишечных свищей, что обусловливает неблагоприятный прогноз БК и требует хирургического лечения. У пациентов данной группы прибегать к формированию обходного анастомоза рекомендовано лишь в исключительных случаях, поскольку высок риск развития синдрома избыточного бактериального роста в отключенной части тонкой кишки, а также возможно развитие рака. Вместе с тем обширные резекции обуславливают развитие синдрома короткой кишки [149].
- У пациентов данной группы, при выявлении стриктуры гастродуоденальной зоны (как правило, 12-перстной кишки) рекомендована эндоскопическая баллонная дилатация или рассечение рубцовой стриктуры (стриктуропластика) [186].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
3.2.5 Лечение БК с перианальными проявлениями (перианальная БК)
Подход к хирургическому вмешательству на перианальной области должен быть индивидуален для каждого пациента [187, 188].
- У пациентов с перианальными проявлениями БК, при наличии простых наружных перианальных свищей рекомендована ликвидация свища путем его иссечения (при помощи фистулотомии) [189] или его адекватное дренирование при наличии абсцессов при помощи установки латексных дренажей-сетонов в сочетании с медикаментозной терапией [190, 191].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
Комментарий: простые свищи, не сопровождающиеся какими-либо симптомами, не требуют хирургического вмешательства. Рекомендовано динамическое наблюдение на фоне вышеописанной консервативной терапии. Показанием к установке сетонов в большинстве случаев являются транс- и экстрасфинктерные свищи. При отсутствии воспалительного процесса в слизистой оболочке прямой кишки возможно выполнение низведения слизисто-мышечного лоскута прямой кишки с пластикой внутреннего свищевого отверстия [190].
- У пациентов с перианальными проявлениями БК, при лечении сложных свищей рекомендовано их дренирование (установка латексных дренажей-сетонов) в комбинации с биологической терапией [58, 191, 192].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 4)
Комментарий: дренирующую латексную лигатуру используют в качестве дополнения к медикаментозной терапии БК в качестве средства обеспечения адекватного дренирования свищевого хода для предотвращения повторного образования абсцессов и ликвидации местной воспалительной реакции в окружающих тканях. Зачастую установка дренирующей лигатуры является подготовительным этапом к выполнению радикальной операции по ликвидации свища. Преимуществами этого метода являются: низкая стоимость, возможность предотвращения формирования новых свищевых ходов и гнойных полостей, снижение потребности во временной или постоянной кишечной стоме, а также низкая частота повторных вмешательств (от 10% до 20%). Учитывая высокую эффективность биологической терапии при надлежащем дренировании сложных свищей прямой кишки оправдано ее раннее назначение (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб**, ведолизумаб**, упадацитиниб**). Тем не менее, сложные свищи, с затеками и выраженным гнойным воспалением часто являются показанием к отключению пассажа путем формирования кишечной стомы.
- У пациентов с перианальными проявлениями БК, при ректовагинальном свище рекомендовано его иссечение с ушиванием дефекта влагалища и низведением полнослойного лоскута прямой кишки [58].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: ректовагинальные свищи в большинстве случаев требуют хирургического вмешательства. При этом, оперативное лечение показано под прикрытием илеостомы. Лишь в отдельных ситуациях при наличии низкого свища между прямой кишкой и преддверием влагалища рекомендовано проведение только консервативного лечения. При наличии активного поражения прямой кишки адекватная противовоспалительная терапия до операции увеличивает эффективность вмешательства [58].
- Пациентам с перианальными проявлениями БК, сопровождающимися эвакуаторными нарушениями и анальным недержанием, приводящих к значительному снижению качества жизни, рекомендовано выполнение брюшно-анальной резекции прямой кишки [58, 149].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
Комментарий: наиболее неблагоприятным фактором, повышающим вероятность постоянной илеостомы или колостомы, является наличие стриктуры нижне-ампулярного отдела прямой кишки или стеноза анального канала. В отдельных ситуациях, при отсутствии активного воспаления в вышележащих отделах кишечника, возможно бужирование стриктуры [58].
- Пациентам со сложными свищами рекомендовано этапное хирургическое лечение. В качестве первого этапа рекомендуется вскрытие и дренирование абсцессов, гнойных полостей [251].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: адекватное вскрытие гнойной полости позволяет проводить иммуносупрессивную терапию по поводу БК без риска развития абсцесса в перианальной области или генерализации инфекции. Дренирование затеков возможно и с использованием дренирующей латексной лигатуры при условии четкой локализации внутреннего свищевого отверстия.
- Пациентам со сложными свищами в качестве второго этапа хирургического лечения рекомендуется иссечение свища с пластикой внутреннего свищевого отверстия слизисто-мышечным лоскутом из стенки прямой кишки при условии ликвидации гнойных затеков, явлений проктита и отсутствия выраженных рубцовых изменений стенок анального канала и прямой кишки [193].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: низведенный лоскут может быть как слизисто-подслизистый, так и слизисто-мышечный. Преимуществами методики являются отсутствие воздействия на структуры запирательного аппарата прямой кишки и минимизация обширности раневых дефектов. При этом частота заживления составляет около 60%, при частоте развития инконтиненции до 10%. В качестве второго этапа лечения также возможности выполнение таких методик, как видеоасстированный метод лечения свищей прямой кишки (VAAFT), а также перевязка свищевого хода в межсфинктерном пространстве (LIFT) у строго отобранной группы больных при отсутствии затеков, явлений проктита и отсутствии признаков инконтиненции [194, 195].
3.2.6 Противорецидивная терапия после хирургического лечения БК
Даже при полном удалении всех макроскопически измененных отделов кишечника, хирургическое вмешательство не приводит к полному выздоровлению: в течение 5 лет клинически значимый рецидив отмечается у 28 - 45% пациентов, а в течение 10 лет - у 36 - 61%, что диктует необходимость назначения или продолжения противорецидивной терапии после операций по поводу БК [196, 197].
К факторам, достоверно повышающим риск послеоперационного рецидива, относятся: курение, две и более резекции кишки в анамнезе, протяженные резекции тонкой кишки в анамнезе (> 50 см), перианальные поражения, пенетрирующий фенотип [198].
В зависимости от сочетания факторов риска, а также от эффективности, ранее проводившейся противорецидивной терапии, пациенты после операции должны быть стратифицированы на группы с различным риском послеоперационного рецидива.
К высокому риску послеоперационного рецидива относится наличие 2 и более факторов риска:
- курение;
- перианальные поражения;
- пенетрирующая БК;
- протяженная резекция (более 50 см) кишечника;
- предыдущее хирургическое вмешательство;
- раннее начало заболевания.
- Пациентам из группы низкого риска с целью профилактики рецидива рекомендовано проведение терапии тиопуринами (АЗА** 2,0 - 2,5 мг/кг/сут или #МП** 1,5 мг/кг/сут) [199, 245, 252].
Уровень убедительности рекомендации - B (уровень достоверности доказательств - 1)
- Пациентам с высоким риском обострения БК еще до проведения контрольного эндоскопического исследования с целью профилактики рецидива рекомендована терапия ГИБП (инфликсимаб**, адалимумаб**, цертолизумаба пэгол**, устекинумаб**, ведолизумаб**) или ТИС (упадацитиниб**) [61, 85, 200, 201, 202].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 3)
Комментарий: данных по применению устекинумаба**, ведолизумаба** и упадацитиниба** в настоящее время еще недостаточно, чтобы достоверно судить об их эффективности в качестве послеоперационной противорецидивной терапии.
- Пациентам с БК противорецидивную терапию рекомендовано начинать в течение 4 недель после оперативного вмешательства при отсутствии послеоперационных осложнений [204].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Спустя 6 - 12 месяцев после операции пациентам с БК рекомендовано проведение контрольного эндоскопического обследования, а при необходимости МРТ и/или КТ с контрастированием кишечника [200, 205, 206, 207].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 3)
- Оперированным пациентам с БК, при невозможности визуализировать зону анастомоза рекомендовано констатировать наличие или отсутствие рецидива, основываясь на сочетании данных рентгенологического обследования (КТ и/или МРТ с контрастированием кишечника) и неинвазивных маркеров воспаления - СРБ, ФК и др. [200, 206, 207, 208].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 3)
Комментарий: при резекции терминального отдела подвздошной кишки или илеоцекальной резекции целесообразно применять шкалу эндоскопической активности послеоперационного рецидива БК по Rutgeerts (см. раздел 2.4 "Инструментальные диагностичесикие исследования", табл. 7) [49, 209].
- У пациентов с БК при отсутствии признаков воспаления или обнаружении минимальных (i1 по шкале Rutgeerts) воспалительных изменений проводимую терапию рекомендовано продолжить [209].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- При наличии более выраженных воспалительных изменений (i2 - i4) рекомендовано усиление терапии: подключение иммуносупрессоров у пациентов, ранее их не получавших или проведение ГИБП или ТИС, находящихся на поддерживающей терапии тиопуринами (АЗА**/#МП**) или при невозможности их назначения [210, 211].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
Комментарий: наличие более выраженных воспалительных изменений (i2 - i4) указывает на неэффективность проводимой терапии.
- В дальнейшем у пациентов с БК, вне зависимости от характера течения заболевания и клинической манифестации БК, рекомендовано не реже одного раза в 1 - 3 года выполнять контрольное эндоскопическое исследование [212].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 4)
3.2.7 Дисфункция илеостомы после хирургического лечения БК
Под дисфункцией илеостомы понимается увеличение объема кишечного отделяемого по илеостоме более 1000 мл в сутки. Ведение пациентов с данным состоянием описана в клинических рекомендациях "Язвенный колит" [213].
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Меры медицинской реабилитации направлены на профилактику осложнений консервативной терапии и нежелательных последствий хирургического лечения.
Легкая и умеренная степень нарушения функционирования требует лечения в амбулаторных условиях. Тяжелая степень нарушения функции, либо абсолютная ее невозможность требуют госпитализации в круглосуточный стационар.
У пациентов, которым потребовалось хирургическое лечение осложнений БК возможна реабилитация в три этапа.
1-й этап - ранняя реабилитация, осуществляется непосредственно после хирургического лечения со 2-х по 14-е сутки. Основной задачей 1 этапа реабилитации является восстановление нормального функционирования ЖКТ после хирургического вмешательства. Именно на этом этапе чаще всего выявляются и должны быть корригированы нарушения мочеиспускания. Важная роль отводится также контролю гомеостаза, мероприятиям, направленным на заживление послеоперационных ран, купированию послеоперационного болевого синдрома, активизации пациента. В данный период проводится контроль общего анализа крови, биохимического анализа крови, коагулограммы крови, общего анализа мочи.
2-й этап реабилитации начинается после 15 суток и продолжается по мере необходимости в последующем. Направлен на окончательное заживление послеоперационных ран с контролем за деятельностью ЖКТ и других систем организма. Данный этап возможно осуществлять как амбулаторно, так и в условиях стационара дневного или круглосуточного пребывания.
3-й этап реабилитации осуществляется в поздний реабилитационный период у пациентов как с постоянной илеостомой, так и перед реконструктивно-восстановительной операцией. Основной задачей на данном этапе является компенсация функции ЖКТ, мероприятия, направленные на выявление и коррекцию нарушений функции запирательного аппарата прямой кишки.
Недостаточность анального сфинктера (НАС) - реабилитация возможна на 2 и 3 этапах. У пациентов после оперативного вмешательства по поводу БК с формированием стомы отмечается снижение функции держания.
- Пациентам с недостаточностью анального сфинктера перед реконструктивно-восстановительным лечением рекомендуется исследование функции сфинктерного (запирательного) аппарата прямой кишки с последующей консультаций врача-физиотерапевта [214].
Уровень убедительности рекомендации - C (уровень достоверности доказательств - 5)
- Пациентам при выявлении недостаточности анального сфинктера 2 - 3 степени рекомендуется провести реабилитационное лечение, включающее 10-дневный цикл БОС-терапии и тибиальной нейромодуляции в условиях дневного или круглосуточного стационара [214]
Уровень убедительности рекомендации C (уровень достоверности доказательств - 5)
Комментарий: в реабилитации пациентов с недостаточностью анального сфинктера по данным литературы широкое применение имеет метод лечения биологической обратной связью (БОС-терапия), направленный на улучшение сократительной способности мышц наружного сфинктера и тазового дна за счет увеличения как силы, так и длительности произвольного сжатия [215, 216]. Данный неинвазивный метод вовлекает в процесс реабилитации собственные ресурсы организма с выработкой правильных навыков на уровне создания новых условно-рефлекторных связей. Также эффективным является метод тибиальной нейромодуляции. Нейромодуляция - это процесс, при котором электрический ток по одним нервным путям модулирует существовавшую ранее активность в других нервных путях или центрах. Чрескожная электростимуляция заднего большеберцового нерва (n.tibialis) - применяется при функциональных заболеваниях органов малого таза, так как в составе заднего большеберцового нерва проходят волокна из II и III крестцовых сегментов спинного мозга, играющие значительную роль в иннервации прямой кишки, мочевого пузыря и их сфинктеров. Доказано, что мышечные структуры отключенного запирательного аппарата могут реагировать на БОС-терапию и проведение тибиальной неийромодуляции, увеличивая как тонус, так и силу волевых сокращений [214, 216]. Стимуляцию тибиального нерва проводят с помощью накожного стимулирующего электрода, что позволяет пациенту после курса предварительного обучения продолжить курс лечения самостоятельно в домашних условиях. В таком случае курс лечения с ежедневными сеансами стимуляции может продлеваться до 1 - 3 месяцев. Контроль эффективности БОС-терапии производится перед началом и по окончании каждого курса процедур путем комплексного физиологического исследования функции запирательного аппарата прямой кишки. При улучшении показателей тонуса и сократительной способности анальных сфинктеров, можно ставить вопрос о выполнении реконструктивно-восстановительной операции, направленной на возобновление естественного пассажа по ЖКТ.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
БК характеризуется прогрессирующим поражением кишечника. На момент установления диагноза осложнения (стриктуры, свищи) обнаруживаются у 10 - 20% пациентов, в то время как в течение 10 лет подобные осложнения развиваются более чем 90% наблюдений. В течение 10 лет хирургические вмешательства в связи с осложнениями и/или неэффективностью консервативной терапии выполняются у половины пациентов с БК, а у 35 - 60% в течение 10 лет после оперативного вмешательства развивается рецидив заболевания. Гормональная зависимость при БК в течение 10 лет хотя бы раз констатируется в 30% случаев [217].
В связи с прогрессирующим характером заболевания пациенты, страдающие БК, должны получать постоянную (пожизненную терапию) и проходить регулярный (пожизненный) мониторинг активности заболевания. Контроль активности заболевания важно проводить используя не только инструментальные методы исследования, но и посредством изучения маркеров воспаления, в первую очередь, уровня ФК, концентрация которого в стуле коррелирует со степенью язвенного поражения ЖКТ.
Периодичность и объем диспансерного наблюдения определяется индивидуально, но у большинства пациентов целесообразно придерживаться следующего:
- В среднем, каждые 6 месяцев - консультация врача-гастроэнтеролога, каждые 12 месяцев осмотр врача-колопроктолога с обязательным трансректальным пальцевым исследованием для исключения перианальных проявлений БК, наружных кишечных свищей, свищей с полыми органами, межкишечных свищей, стриктуры кишечника. Каждые 6 месяцев - общий (клинический) анализ крови развернутый, исследование уровня СРБ, определение уровня ФК.
- Рутинное (ежегодное) эндоскопическое исследование при отсутствии клинических показаний (сомнений в диагнозе, необходимости исключения сопутствующих состояний, нарастания клинических проявлений, подозрений на осложнения, необходимости контроля после оперативного лечения) в большинстве случаев не проводится
- При ухудшении состояния, нарастании уровня маркеров воспаления (C-реактивного белка, фекального кальпротектина) следует выполнять колоноскопию для оценки активности заболевания, затем осмотр врачом-гастроэнтерологом и/или врачом-колопроктологом с полным объективным обследованием.
При необходимости определения локализации, протяженности, степени активности воспалительного процесса, для исключения осложнений основного заболевания в виде инфильтратов брюшной полости, межкишечных, межорганных свищей, перфораций, стриктур (при отсутствии медицинских противопоказаний к введению контрастных средств), следует выполнять магнитно-резонансную томографию и/или компьютерную томографию органов брюшной полости и малого таза с внутривенным контрастированием.
- Периодичность и объем диспансерного наблюдения определяется индивидуально, но у большинства пациентов рекомендовано выполнять исследование уровня C-реактивного белка в сыворотке крови, а также исследование уровня кальпротектина в кале каждые 3 месяца [74].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- Пациентам, получающим иммуносупрессоры, рекомендовано ежемесячно выполнять исследование уровня эритроцитов, лейкоцитов, тромбоцитов крови, свободного и связанного билирубина, креатинина, мочевины, определение активности аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, амилазы в крови для оценки функции печени [74].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- Пациентам рекомендовано ежегодно выполнять рентгенологическое или МР-исследование кишечника для исключения образования стриктур и развития иных осложнений [74].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- Пациентам рекомендовано ежегодно выполнять местный осмотр перианальной области и пальцевое исследование прямой кишки для исключения перианальных осложнений, а также при необходимости - ЭУЗИ [29, 59].
Уровень убедительности рекомендации - C (уровень достоверности рекомендации - 5)
- Пациентам при динамическом нарастании уровня маркеров воспаления (CРБ, ФК) рекомендуется выполнять (илео) колоноскопию для оценки активности заболевания [208].
Уровень убедительности рекомендации - B (уровень достоверности рекомендации - 3)
Комментарий: рутинное (ежегодное) эндоскопическое исследование при отсутствии клинических показаний (сомнений в диагнозе, необходимости исключения сопутствующих состояний, нарастания клинических проявлений, подозрений на осложнения) в большинстве случаев не требуется. При отсутствии показаний, связанных с БК, периодичность илеоколоноскопии определяется клиническими рекомендациями по раннему выявлению злокачественных новообразований толстой кишки.
5.1 Профилактика венозных тромбозов
- Пациентам с БК в период госпитализации, а также на амбулаторном этапе в период обострения, при наличии других известных факторов риска венозных тромбозов рекомендовано проведение профилактики венозных тромбоэмболических осложнений (ВТЭО) [218].
Уровень убедительности рекомендации C (уровень достоверности рекомендации - 5)
Комментарий. У больных БК в два и более раза повышен риск развития венозных тромбозов [219]. Риск венозных тромбозов увеличивается в период активности заболевания и при госпитализации по любой причине. Тромбопрофилактику после выписки из стационара следует рассматривать только у пациентов с большими факторами риска ВТЭО [218]. Для оценки вероятности их развития у госпитализированных нехирургических пациентов рекомендуется использовать шкалы Padua [220] и IMPROVE VTE, у хирургических пациентов шкалу Caprini [221]. Для тромбопрофилактики у больных БК рекомендуется использовать нефракционированный гепарин (НФГ), низкомолекулярный гепарин (НМГ) (AXT B01AB), в профилактических дозах. При наличии противопоказаний к применению НФГ, НМГ и высоком риске геморрагических осложнений по шкалам HAS-BLED, RIETE рекомендовано применение механических способов профилактики.
5.2 Вакцинация
Стратегиями по нивелированию рисков присоединения и/или реактивации различных инфекций для пациента с БК признаны своевременная диагностика инфекций и их специфическая профилактика, прежде всего, в виде вакцинации [222, 223, 224].
Всем пациентам с БК рекомендовано выполнить оценку вакцинального статуса на этапе установления диагноза с последующим регулярным мониторингом в ходе дальнейшего консультирования. Документированная привитость заменяет серологический скрининг напряженности иммунного ответа, который проводится в случае отсутствия документов, подтверждающих проведение иммунизации [223].
Вакцины (инактивированные) применяют у пациентов с БК независимо от применяемого лечения [224]. Планирование иммунизации живыми вакцинами следует осуществлять до назначения иммуносупрессивной терапии, если начало лечения можно безопасно отсрочить, или вводить вакцины в период минимальной дозы препарата, обладающего иммуносупрессивным действием [223]. При высоком риске заражения вакцинопредотвратимой инфекцией и развития тяжелого течения, следует взвесить обе потенциальные угрозы жизни и здоровью пациента и предусмотреть возможность проведения вакцинации (в том числе живыми вакцинами) на фоне проводимой терапии БК [225].
Кроме того, следует вакцинировать родных и близких, тесно контактирующих с больными БК, что является важной стратегией защиты пациентов с ВЗК от тяжелых вакцинопредотвратимых инфекций. Этот подход называется "кокон-вакцинацией" [223].
У пациентов с БК наиболее высок риск тяжелого течения инфекций, вызванных пневмококком, вирусами гриппа, гепатита B, кори, краснухи, эпидемического паротита, ветряной оспы, что требует приоритетной вакцинации к этим возбудителям.
- Рекомендовано пациентам с БК, при диагностике заболевания оценить вакцинальный статус, риск заражения и последствия перенесенной инфекции с целью определения необходимости и вида вакцинации [222].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: также следует уточнить, были ли ранее у пациента вакцинопредотвратимые инфекции (например, корь, краснуха, ветряная оспа, эпидемический паротит и др.). В дальнейшем в ходе наблюдения и лечения следует регулярно мониторировать вакцинальный статус пациента (не реже 1 раза в год).
- Рекомендовано пациентам с БК проведение вакцинации в соответствии с национальным календарем профилактических прививок с целью предотвращения/уменьшения вероятности тяжелого (осложненного) течения инфекций, с учетом периода заболевания и получаемой терапии [222, 223, 224, 226].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарий: пациентам, не получающим иммуносупрессивную терапию, могут применяться любые вакцины в соответствии с инструкцией (инактивированные и живые). Пациентам, получающим иммуносупрессивную терапию, инактивированные вакцины назначаются без ограничений, живые вакцины - с ограничениями.
В настоящее время нет однозначных данных об оптимальном интервале между возможным применением живых вакцин после завершения иммуносупрессивной терапии.
Дозой ГКС, вызывающей иммуносупрессию, является для преднизолона** 2 мг/кг/сут, принимаемой в течение 14 дней и более; введение живых вакцин этим пациентам допускается через 1 месяц и более после окончания терапии [Методическим указаниям МУ 3.3.1.1095-02. "Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок"]. Использование такой дозы в течение менее 2 недель или меньших доз в течение более длительного периода не ведет к развитию выраженной иммуносупрессии.
При этом в других руководствах рекомендуются более длительные интервалы между назначением живых вакцин после завершения иммуносупрессивной терапии - не ранее чем через 1 - 3 мес, а в случае применения высоких доз глюкокортикоидов, интервал после окончания лечения может составлять до 6 месяцев и зависит от того, как это зафиксировано в инструкции по применению препарата [222, 223].
Необходимую иммунизацию с использованием вакцин (в том числе, живых) следует, при возможности, проводить до старта иммуносупрессивной терапии. В ином случае, иммунизация может быть продолжена при установлении контроля над заболеванием, при необходимости его поддержания - на фоне назначения базисной терапии, строгого соблюдения диетологических и других рекомендаций гастроэнтеролога. При этом иммуносупрессивное лечение может быть начато не ранее, чем через 3 - 4 недели после введения живых вакцин, без интервала - после введения неживых вакцин [222, 223].
У ряда пациентов с БК сохраняется риск недостаточного иммунного ответа после проведения стандартной схемы вакцинации, в связи с чем возможно рассмотреть проведение выборочного контроля напряженности иммунитета не ранее, чем через 1 месяц после завершенной вакцинации (например, после вакцины для профилактики вирусного гепатита B** - Определение антител к поверхностному антигену (anti-HBs) вируса гепатита B (Hepatitis B virus) в крови, количественное исследование) с последующим введением бустерной дозы вакцины при отсутствии защитных титров антител [222, 227].
5.2.1 Вакцинация против приоритетных инфекций
- Вакцинацию против пневмококковой инфекции пациентам с БК с профилактической целью рекомендовано проводить последовательно, начиная с однократной дозы конъюгированной вакцины для профилактики пневмококковых инфекций** (ПКВ13 или иной вакциной наиболее широкой валентности) с последующим введением полисахаридной вакцины для профилактики пневмококковых инфекций** (например, ППВ23) с минимальным интервалом 8 недель. Повторная вакцинация предусмотрена также с применением пневмококковой полисахаридной вакцины (ППВ23) через 5 лет [223].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендовано пациентам с БК проведение ежегодной вакцинации против гриппа при подготовке к сезону гриппа с применением квадривалентных вакцин (инактивированных)** с профилактической целью [222, 223, 228].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
- Рекомендовано пациентам с БК перед назначением иммуносупрессивной терапии при отсутствии подтверждения перенесенной инфекции или выполненной вакцинации против гепатита B, ветряной оспы, кори, краснухи и эпидемического паротита проведение соответствующей вакцинации [222, 223].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарии: вакцинация проводится в соответствии с инструкциями.
Пациентам с ВЗК для профилактики новой коронавирусной инфекции COVID-19 вакцинация комбинированной векторной вакциной** рекомендована с осторожностью с целью предотвращения/уменьшения вероятности тяжелого (осложненного) течения инфекции, с учетом активности и вида терапии основного заболевания. [229].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
Комментарий: Кратность вакцинации определяется нормативными документами Минздрава России.
Нет данных об ухудшении течения основного заболевания на фоне вакцинации [230, 231, 232].
Следует отметить, что вопросы вакцинации против SARS-CoV-2 в настоящее время нужно решать индивидуально и с осторожностью, с учетом показателя польза/риск. Это объясняется изменением характера течения инфекции, быстрой мутацией вируса и отсутствием модифированных вакцин, т.к. существующие в РФ вакцины были разработаны к первоначальным штаммам вируса.
Рекомендована вакцинация пациенток с БК в рамках подготовки к беременности, а также во время беременности в соответствии с национальным календарем профилактических прививок с целью предотвращения/уменьшения вероятности тяжелого (осложненного) течения любых инфекций, с учетом периода заболевания и получаемой терапии [222, 223, 224, 226].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5)
6. Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, организуется и оказывается согласно:
1) в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
2) в соответствии с порядками оказания помощи по профилям "гастроэнтерология", "колопроктология", обязательным для исполнения на территории Российской Федерации всеми медицинскими организациями;
3) на основе настоящих клинических рекомендаций;
4) с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь оказывается врачом-гастроэнтерологом, врачом-колопроктологом и иными врачами-специалистами в медицинских организациях, имеющих лицензию на оказание соответствующих видов медицинской деятельности.
При подозрении или выявлении у пациента БК врачи-терапевты, врачи-терапевты участковые, врачи общей практики (семейные врачи), врачи-специалисты, средние медицинские работники в установленном порядке направляют пациента на консультацию в медицинскую организацию, имеющую в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника (при наличии в субъекте возможна организация на функциональной основе) для оказания ему первичной специализированной медико-санитарной помощи. Консультация в указанных структурных подразделениях медицинской организации должна быть проведена не позднее 14 рабочих дней с даты выдачи направления на консультацию, а в случаях тяжелых форм БК не позднее 3 рабочих дней с даты выдачи направления на консультацию.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника организуют выполнение диагностических исследований, необходимых для установления диагноза, включая определение степени выраженности воспалительного процесса, протяженности поражения, наличия кишечных и внекишечных проявлений, в том числе взятие биопсийного материала.
В случае невозможности выполнения диагностических исследований, необходимых для установления диагноза, включая определение степени выраженности воспалительного процесса, протяженности поражения, наличия кишечных и внекишечных проявлений, в том числе взятие биопсийного материала, а также при наличии показаний для оказания медицинской помощи в стационарных условиях, пациент направляется лечащим врачом в гастроэнтерологическое отделение, колопроктологическое отделение, центр диагностики и лечения воспалительных заболеваний кишечника или иную медицинскую организацию, оказывающую медицинскую помощь в стационарных условиях пациентам по профилю "гастроэнтерология", "колопроктология".
При подозрении и (или) выявлении у пациента БК в ходе оказания ему скорой медицинской помощи таких пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь по профилю "гастроэнтерология", "колопроктология" для определения тактики ведения и необходимости применения дополнительно других методов специализированного лечения, включая проведение таргетной биологической терапии.
Врач-гастроэнтеролог, врач-колопроктолог медицинской организации, имеющей в своем составе кабинет врача-гастроэнтеролога, врача-колопроктолога, амбулаторный гастроэнтерологический центр (отделение), амбулаторный колопроктологический центр (отделение), центр диагностики и лечения воспалительных заболеваний кишечника направляет пациента в медицинские организации, имеющие для оказания медицинской помощи в стационарных условиях в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника для уточнения диагноза (в случае невозможности установления диагноза при оказании первичной специализированной медико-санитарной помощи) и оказания специализированной, в том числе высокотехнологичной, медицинской помощи. Срок начала оказания специализированной, за исключением высокотехнологичной, медицинской помощи определяется по решению комиссии по отбору пациентов для госпитализации в зависимости от тяжести БК, характера течения, распространенности воспалительного процесса. Срок не должен превышать 30 календарных дней с даты выдачи направления на госпитализацию.
Специализированная, в том числе высокотехнологичная, медицинская помощь при БК оказывается врачами-гастроэнтерологами, врачами-колопроктологами в медицинских организациях, имеющих в своем составе гастроэнтерологическое отделение и/или колопроктологическое отделение, и/или центр диагностики и лечения воспалительных заболеваний кишечника, имеющих лицензию, необходимую материально-техническую базу, сертифицированных специалистов, в стационарных условиях и условиях дневного стационара и включает в себя профилактику, диагностику, лечение БК, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию.
В случае необходимости применения методов лечения, не выполняемых в медицинских организациях, осуществляющих деятельность в сфере обязательного медицинского страхования в рамках территориальной программы обязательного медицинского страхования, необходимости дополнительного обследования в диагностически сложных случаях и (или) в случаях комплексной предоперационной подготовки у пациентов с осложненными формами заболевания и (или) коморбидными заболеваниями для последующего лечения, а также необходимости повторной госпитализации по рекомендации федеральной медицинской организации пациент направляется в федеральную медицинскую организацию оказывающую медицинскую помощь в стационарных условиях пациентам по профилю "гастроэнтерология", "колопроктология" для оказания высокотехнологичной медицинской помощи в соответствии с порядком организации оказания высокотехнологичной медицинской помощи с применением единой государственной информационной системы в сфере здравоохранения.
Показания для госпитализации в круглосуточный или дневной стационар медицинской организации, оказывающей специализированную, в том числе высокотехнологичную медицинскую помощь при БК определяются консилиумом врачей-гастроэнтерологов и врачей-колопроктологов, с привлечением при необходимости иных врачей-специалистов.
Показанием для госпитализации пациента в медицинскую организацию в экстренной или неотложной форме является:
1) наличии осложнений БК, требующих оказания ему специализированной медицинской помощи в экстренной и неотложной форме;
2) наличие осложнений лечения БК (хирургическое вмешательство, биологическая терапия, гормональная и цитостатическая терапия и т.д.).
Показанием для госпитализации в медицинскую организацию в плановой форме является:
1) необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
2) наличие показаний к специализированному лечению БК (хирургическое вмешательство, гормональная и цитостатическая терапия, биологическая и таргетная терапия), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показанием к выписке пациента из медицинской организации является:
1) завершение курса лечения, или одного из этапов оказания специализированной, в том числе высокотехнологичной медицинской помощи, в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей лечение БК при условии отсутствия осложнений основного заболевания и/или от лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
3) необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Прогностически неблагоприятными факторами при БК являются курение, дебют заболевания в детском возрасте, перианальные поражения, пенетрирующий фенотип заболевания и распространенное поражение тонкой кишки. С пациентом-курильщиком в обязательном порядке должна быть проведена беседа о необходимости прекращения табакокурения.
Планирование беременности необходимо осуществлять в период ремиссии ВЗК, что позволяет улучшать исходы беременности. Применение беременными большинства препаратов для лечения ВЗК сопряжено с низким риском неблагоприятного воздействия на плод, за исключением #МТ**. Отмена анти-ФНО возможна лишь у ограниченного числа пациенток с низким риском реактивации БК. Лечение ГИБП, не противопоказанными при беременности (см. инструкцию по применению препарата), может быть продолжено, если польза для матери превышает потенциальные риски для плода.
Критерии оценки качества медицинской помощи
Критерии оценки качества первичной медико-санитарной помощи взрослым при болезни Крона
|
N п/п
|
Критерии оценки качества
|
Оценка выполнения
|
|
1.
|
Выполнен прием (осмотр, консультация) врача-гастроэнтеролога и/или врача-колопроктолога с обязательным трансректальным пальцевым исследованием (при наличии свищей и/или перианальных проявлениях болезни Крона, наружных кишечных свищей, свищей с полыми органами, межкишечных свищей, стриктуры кишечника)
|
Да/Нет
|
|
2.
|
Выполнена колоноскопия с исследованием терминального отдела подвздошной кишки (при установлении диагноза)
|
Да/Нет
|
|
3.
|
Выполнена биопсия слизистой оболочки кишечника (при установлении диагноза)
|
Да/Нет
|
|
4.
|
Выполнена магнитно-резонансная томография и/или компьютерная томография органов брюшной полости и малого таза с внутривенным контрастированием (при необходимости определения локализации, протяженности, степени активности воспалительного процесса, для исключения осложнений основного заболевания в виде инфильтратов брюшной полости, межкишечных, межорганных свищей, перфораций, стриктур при отсутствии медицинских противопоказаний к введению контрастных средств)
|
Да/Нет
|
|
5.
|
Выполнено назначение антибактериальных препаратов системного действия (при выявлении воспалительного инфильтрата брюшной полости или внекишечных проявлений заболевания)
|
Да/Нет
|
Критерии оценки качества специализированной медицинской помощи взрослым при болезни Крона
|
N п/п
|
Критерии оценки качества
|
Оценка выполнения
|
|
1.
|
Выполнен прием (осмотр, консультация) врача-колопроктолога и/или врача-гастроэнтеролога с обязательным трансректальным пальцевым исследованием (при наличии свищей и/или перианальных проявлениях болезни Крона, наружных кишечных свищей, свищей с полыми органами, межкишечных свищей, стриктуры кишечника)
|
Да/Нет
|
|
2.
|
Выполнена колоноскопия с исследованием терминального отдела подвздошной кишки (если не проводилась в течение 6 месяцев до момента госпитализации)
|
Да/Нет
|
|
3.
|
Выполнена биопсия слизистой оболочки кишечника (при установлении диагноза в случае, если не была выполнена в амбулаторных условиях)
|
Да/Нет
|
|
4.
|
Выполнена обзорная рентгенография органов брюшной полости в течение 2 часов с момента госпитализации или компьютерная томография органов брюшной полости и забрюшинного пространства (при наличии клинических признаков кишечной непроходимости)
|
Да/Нет
|
|
5.
|
Выполнена магнитно-резонансная томография и/или компьютерная томография органов брюшной полости и малого таза с внутривенным контрастированием (при необходимости определения локализации, протяженности, степени активности воспалительного процесса, для исключения осложнений основного заболевания в виде инфильтратов брюшной полости, межкишечных, межорганных свищей, перфораций, стриктур, при отсутствии медицинских противопоказаний к введению контрастных средств)
|
Да/Нет
|
|
6.
|
Проведена терапия кортикостероидами системного действия или ингибиторами фактора некроза опухоли альфа (ФНО-альфа) или устекинумабом или ведолизумабом или упадацитинибом или азатиоприном или меркаптопурином
|
Да/Нет
|
|
7.
|
Проведена терапия антибактериальными препаратами системного действия (при выявлении воспалительного инфильтрата брюшной полости или внекишечных проявлений заболевания)
|
Да/Нет
|
|
8.
|
Выполнено назначение средств противорецидивной терапии: азатиоприн или меркаптопурин или инфликсимаб или адалимумаб или цертолизумабапэгол или устекинумаб или ведолизумаб или упадацитиниб (после хирургического вмешательства или после достижения медикаментозной ремиссии)
|
Да/Нет
|
|
9.
|
Рекомендован осмотр/консультация врача-колопроктолога или врача-хирурга (при наружных кишечных свищах, свищах с полыми органами, межкишечных свищах, стриктурах кишечника, проявлениях, кровотечениях)
|
Да/Нет
|
Клинические рекомендации по диагностике и лечению болезни Крона (К 50, взрослые) обсуждены 31 марта 2023 г. на совместном заседании Комиссий по хирургическим и терапевтическим наукам научного совета ОМедН РАН, а также на открытых заседаниях Правления Общероссийской общественной организации "Ассоциация колопроктологов России" и заседании профильной комиссии по специальности "Колопроктология"
Список литературы
1. Sandborn WJ, Feagan BG, Hanauer SB, Lochs H,  R, Modigliani R, et al. A review of activity indices and efficacy endpoints for clinical trials of medical therapy in adults with Crohn"s disease. Gastroenterology 2002; 122: 512 - 30.
R, Modigliani R, et al. A review of activity indices and efficacy endpoints for clinical trials of medical therapy in adults with Crohn"s disease. Gastroenterology 2002; 122: 512 - 30.
2.  F, Dignass A, Annese V, et al. 3rd European Evidence-based Consensus on the Diagnosis and Management of Crohn"s Disease 2016: Part 1: Diagnosis and Medical Management. J Crohns Colitis. 2017; 11(1): 3 - 25.
F, Dignass A, Annese V, et al. 3rd European Evidence-based Consensus on the Diagnosis and Management of Crohn"s Disease 2016: Part 1: Diagnosis and Medical Management. J Crohns Colitis. 2017; 11(1): 3 - 25.
3. Peyrin-Biroulet L. Transmural healing as a therapeutic goal in Crohn"s disease: a systematic review. Lancet Gastroenterol Hepatol. 2021; 6(8): 659 - 667.
4. Министерство здравоохранения Российской Федерации. Клинические рекомендации "Ревматоидный артрит". Available: https://cr.minzdrav.gov.ru/schema/250_2.
5. de Souza HS, Fiocchi C. Immunopathogenesis of IBD: current state of the art. Nat Rev Gastroenterol Hepatol. 2016; 13(1): 13 - 27.
6. Pascal V, Pozuelo M, Borruel N, et al. A microbial signature for Crohn"s disease. Gut. 2017; 66(5): 813 - 822.
7. Mak WY, Zhao M, Ng SC, et al. The epidemiology of inflammatory bowel disease: East meets West. Journal of Gastroenterology and Hepatology. 2020; 35: 380 - 389.
8. Burisch J., Jess T., Martinato M., Lakatos P. on behalf of ECCO-EpiCom. The burden of inflammatory bowel disease in Europe. JCC, 2013; 7: 322 - 337.
9. Ng SC, Shi HY, Hamidi N et al. Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies. Lancet 2017; 390: 2769 - 78.
10. Burisch J, Pedersen N,  S, et al. East-West gradient in the incidence of inflammatory bowel disease in Europe: The ECCO-EpiCom inception cohort. Gut, 2014; 63(4): 588 - 97.
S, et al. East-West gradient in the incidence of inflammatory bowel disease in Europe: The ECCO-EpiCom inception cohort. Gut, 2014; 63(4): 588 - 97.
11. Князев О.В., Шкурко Т.В., Фадеева Н.А. и соавт. Эпидемиология хронических воспалительных заболеваний кишечника. Вчера, сегодня, завтра. Экспериментальная и клиническая гастроэнтерология. 2017; 3(139): 4 - 12.
12. Плотникова Е.Ю., Чашкова Е.Ю. Некоторые аспекты лечения воспалительных заболеваний кишечника. Лечащий врач. 2019; 8: 14 - 20.
13. Чашкова Е.Ю., Коротаева Н.С., Пак В.Е. и соавт. Клинико-эпидемиологические аспекты язвенного колита в Иркутской области. Колопроктология. 2023; 22(1): 108 - 116.
14. Белоусова Е.А., Шелыгин Ю.А., Ачкасов С.И. и соавт. Клинико-демографические характеристики и лечебные подходы у пациентов с воспалительными заболеваниями кишечника (болезнь Крона, язвенный колит) в РФ. Первые результаты анализа Национального регистра. Колопроктология. 2023; 22(1): 65 - 82. doi: 10.33878/2073-7556-2023-22-1-65-822023.
15. Silverberg MS, Satsangi J, Ahmad T, et al. Toward an integrated clinical, molecular and serological classification of inflammatory bowel disease: Report of a Working Party of the 2005 Montreal World Congress of Gastroenterology. Can J Gastroenterol. 2005; 19(Suppl A): 5 - 36.
16. Cosnes J, Cattan S, Blain A, et al. Long-term evolution of disease behavior of Crohn"s disease. Inflamm Bowel Dis. 2002; 8: 244 - 50.
17. Best WR, Becktel JM, Singleton JW, Kern F Jr. Development of a Crohn"s disease activity index. National Cooperative Crohn"s Disease Study. Gastroenterology. 1976; 70(3): 439 - 44.
18. Harvey RF, Bradshaw JM. A simple index of Crohn"s-disease activity. Lancet 1980; 315 (8167): 514.
19. Белоусова Е.А. Рекомендации по диагностике и лечению болезни Крона. Фарматека. 2009; 13: 38 - 44;
20. Harbord M, Annese V, Vavricka SR, et al. The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease. J Crohns Colitis. 2016,10(3): 239 - 254.
21. Vavricka SR, Schoepfer A, Scharl M, et al. Extraintestinal manifestations of inflammatory bowel disease. Inflam Bowel Dis. 2015; 21 (8): 1982 - 1992.
22. Egeberg A, Mallbris L, Warren RB, et al. Association between psoriasis and inflammatory bowel disease: a Danish nationwide cohort study. Br J Dermatol. 2016 Sep; 175(3): 487 - 92.
23. Белоусова Е.А., Халиф И.Л., Абдулганиева Д.И. и соавт. Социально-демографическая характеристика, особенности течения и варианты лечения воспалительных заболеваний кишечника в России. Результаты двух многоцентровых исследований. Альманах клинической медицины. 2018; 46(6): 445 - 463. doi: 10.18786/2072-0505-2018-46-6.
24. Lichtenstein GR, Loftus EV, Isaacs KL et al. ACG Clinical Guideline: Management of Crohn"s Disease in Adults. Am J Gastroenterol. 2018; 113(4): 481 - 517. doi: 10.1038/ajg.2018.27.
25. Чашкова Е.Ю., Владимирова А.А., Неустроев В.Г. и соавт. Воспалительные заболевания толстой кишки - аспекты диагностики. Бюллетень Восточно-Сибирского научного центра СО РАМН. 2011; 4-2: 209 - 221.
26. Lennard-Jones JE. Classification of inflammatory bowel disease. Scand J Gastroenterol Suppl. 1989; 170: 2 - 6.
27. Daperno M, D"Haens G, Van Assche G et al. Development and validation of a new, simplified endoscopic activity score for Crohn"s disease: the SES-CD. Gastrointest Endosc. 2004; 60(4): 505 - 12. doi: 10.1016/s0016-5107(04)01878-4.
28. Тертычный А.С., Андреев А.И., Гебоэс К. Современные подходы к морфологической диагностике воспалительных заболеваний кишечника на материале эндоскопических биопсий. Архив патологии. 2011; 1(73): 40 - 47.
29. Шелыгин Ю.А., Благодарный Л.А. Справочник по колопроктологии. "Литтерра", 2012. 608 с.
30. Dignass AU, Gasche C, Bettenworth D, et al. European consensus on the diagnosis and management of iron deficiency and anaemia in inflammatory bowel diseases. J Crohns Colitis 2015; 9: 211 - 22.
31. Vermeire S, Van Assche G, Rutgeerts P. C-reactive protein as a marker for inflammatory bowel disease. Inflamm.Bowel.Dis. 2004; 10: 661 - 665.
32. D"Inca R, Dal Pont E, Di Leo V, et al. Calprotectin and lactoferrin in the assessment of intestinal inflammation and organic disease. Int J Colorectal Dis 2007; 22: 429 - 37.
33. Jensen M.D., Kjeldsen J., Nathan T. Fecal calprotectin is equally sensitive in Crohn"s disease affecting the small bowel and colon. Scand. J. Gastroenterol. 2011; 46: 694 - 700. doi: 10.3109/00365521.2011.560680.
34. Menees SB, Powell C, Kurlander J et al. A meta-analysis of the utility of C-reactive protein, erythrocyte sedimentation rate, fecal calprotectin, and fecal lactoferrin to exclude inflammatory bowel disease in adults with IBS. Am J Gastroenterol 2015; 110: 444 - 454.
35. Kennedy NA, Clark A, Walkden A et al. Clinical utility and diagnostic accuracy of faecal calprotectin for IBD at first presentation to gastroenterology services in adults aged 16 - 50 years. J Crohns Colitis 2015; 9: 41 - 49.
36. Issa M, Vikayapal A, Gracham MB et al. Impact of Clostridium difficile in inflammatory bowel disease patients. Clin Gastroenterol Hepatol. 2007; 5: 345 - 351.
37. Rodeman JF, Dubberke ER, Reske KA et al. Incidence of Clostridium difficile in inflammatory bowel disease. Clin Gastroenterol Hepatol. 2007; 5: 339 - 344.
38. Issa M, Ananthakrishnan AN, Binion DG. Clostridium difficile and inflammatory bowel disease. Inflamm Bowel Dis. 2008; 14: 1432 - 42.
39. Nguyen GC, Kaplan GG, Harris ML et al. A national survey of the prevalence and impact of Clostridium difficile infection among hospitalized inflammatory bowel disease patients. Am J Gastroenterol. 2008; 103: 1443 - 50.
40. Сухина М.А., Юдин С.М., Загайнова А.В. и соавт. Практические рекомендации по лабораторной диагностике анаэробной инфекции. М.: "Триада", 2022, 84 с.
41. Kim JJ, Simpson N, Klipfel N. et al. Cytomegalovirus infection in patients with active inflammatory bowel disease. Dig Dis Sci. 2010 Apr; 55(4): 1059 - 65. doi: 10.1007/s10620-010-1126-4.
42. Mylonaki M, Langmead L, Pantes A, et al. Enteric infection in relapse of inflammatory bowel disease: importance of microbiological examination of stool. Eur J Gastroenterol Hepatol 2004; 16: 775 - 8.
43. Nolan DJ. Radiology of inflammatory bowel disease. Br J Hosp Med. 1986; 36(2): 128 - 32.
44. Long B, Robertson J, Koyfman A. Emergency Medicine Evaluation and Management of Small Bowel Obstruction: Evidence-Based Recommendations. J Emerg Med. 2019; 56(2): 166 - 176. doi: 10.1016/j.jemermed.2018.10.024.
45. Coremans G, Rutgeerts P, Geboes K, et al. The value of ileoscopy with biopsy in the diagnosis of intestinal Crohn"s disease. Gastrointest Endosc 1984; 30: 167 - 72.
46. Carter MJ, Lobo AJ, Travis SP. Guidelines for the management of inflammatory bowel disease in adults. Gut. 2004; 53 Suppl 5: V1 - 16.
47. Marshall JK, Cawdron R, Zealley I, et al. Prospective comparison of small bowel meal with pneumocolon versus ileo-colonoscopy for the diagnosis of ileal Crohn"s disease. Am J Gastroenterol. 2004; 99: 1321 - 9.
48. Magro F, Langner C, Driessen A, et al. European consensus on the histopathology of inflammatory bowel disease. J Crohns Colitis. 2013; 7(10): 827 - 51. doi: 10.1016/j.crohns.2013.06.001.
49. Khanna R, Zou G, Stitt L, et al. Responsiveness of Endoscopic Indices of Disease Activity for Crohn"s Disease. Am J Gastroenterol. 2017; 112(10): 1584 - 1592. doi: 10.1038/ajg.2016.580.
50. Cameron DJ. Upper and lower gastrointestinal endoscopy in children and adolescents with Crohn"s disease: a prospective study. J Gastroenterol Hepatol. 1991; 6(4): 355 - 8.
51. Thakkar K, Lucia CJ, Ferry GD, et al. Repeat endoscopy affects patient management in pediatric inflammatory bowel disease. Am J Gastroenterol. 2009; 104(3): 722 - 7. doi: 10.1038/ajg.2008.111.
52. Church PC, Kuint RC, Ledder O, et al. Magnetic Resonance Enterography Cannot Replace Upper Endoscopy in Pediatric Crohn Disease: An Imagekids Sub-study. J Pediatr Gastroenterol Nutr. 2018; 67(1): 53 - 58. doi: 10.1097/MPG.0000000000001869.
53. Horsthuis K, Bipat S, Bennink RJ, Stoker J. Inflammatory bowel disease diagnosed with US, MR, scintigraphy, and CT: metaanalysis of prospective studies. Radiology 2008; 247(1): 64 - 79.
54. Bettenworth D, Bokemeyer A, Baker M, et al. Assessment of Crohn"s disease-associated small bowel strictures and fibrosis on cross-sectional imaging: a systematic review. Gut. 2019; 68(6): 1115 - 1126. doi: 10.1136/gutjnl-2018-318081.
55. Chidi VN, Schwartz DA. Imaging of perianal fistulizing Crohn"s disease. Expert Rev Gastroenterol Hepatol. 2015; 9(6): 797 - 806. doi: 10.1586/17474124.2015.1031110.
56. Sheedy SP, Bruining DH, Dozois EJ, et al. MR Imaging of Perianal Crohn Disease. Radiology. 2017; 282(3): 628 - 645. doi: 10.1148/radiol.2016151491.
57. Zawadzki A, Starck M, Bohe M, et al. A unique 3D endoanal ultrasound feature of perianal Crohn"s fistula: the "Crohn ultrasound fistula sign". Colorectal Dis. 2012; 14(9): 608 - 11. DOI: 10.1111/j.1463-1318.2012.03047.
58. Gecse KB, Bemelman W, Kamm MA, et al. A global consensus on the classification, diagnosis and multidisciplinary treatment of perianal fistulising Crohn"s disease. Gut. 2014; 63: 1381 - 1392. DOI: 10.1136/gutjnl-2013-306709.
59. Alabiso ME, Iasiello F, Pellino G, et al. 3D-EAUS and MRI in the Activity of Anal Fistulas in Crohn"s Disease. Gastroenterol Res Pract. 2016; 2016: 1895694. DOI: 10.1155/2016/1895694.
60. Tandon P, James P, Cordeiro E, et al. Diagnostic Accuracy of Blood-Based Tests and Histopathology for Cytomegalovirus Reactivation in Inflammatory Bowel Disease: A Systematic Review and Meta-Analysis. Inflamm Bowel Dis. 2017; 23(4): 551 - 560. doi: 10.1097/MIB.0000000000001073.
61. Lamb CA, Kennedy NA, Raine T, et al. British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults. Gut. 2019; 68 (Suppl 3): 1 - 106. doi: 10.1136/gutjnl-2019-318484.
62. Fraquelli M, Colli A, Casazza G, et al. Role of US in detection of Crohn disease: meta-analysis. Radiology. 2005; 236: 95 - 101.
63. Martinez MJ, Ripolles T, Paredes JM, et al. Assessment of the extension and the inflammatory activity in Crohn"s disease: comparison of ultrasound and MRI. Abdom Imaging 2009; 34: 141 - 8.
64. Panes J, Bouzas R, Chaparro M, et al. Systematic review: the use of ultrasonography, computed tomography and magnetic resonance imaging for the diagnosis, assessment of activity and abdominal complications of Crohn"s disease. Aliment Pharmacol Ther. 2011; 34: 125 - 45.
65. Воробьев Г.И., Орлова Л.П., Самсонова Т.В., и соавт. Возможности ультразвукового исследования в диагностике болезни Крона. Ультразвуковая и функциональная диагностика. 2010; 1: 29 - 36.
66. Самсонова Т.В., Орлова Л.П. Ультразвуковая семиотика болезни Крона тонкой кишки. Колопроктология. 2014; 1(47): 60 - 68.
67. Dionisio PM, Gurudu SR, Leighton JA, et al. Capsule endoscopy has a significantly higher diagnostic yield in patients with suspected and established small-bowel Crohn"s disease: a meta-analysis. Am J Gastroenterol. 2010; 105(6): 1240 - 8. doi: 10.1038/ajg.2009.713.
68. Spada C, Riccioni ME, Costamagna G. Patients with known small bowel stricture or with symptoms of small bowel obstruction secondary to Crohn's disease should not perform video capsule endoscopy without previously tested for small bowel patency. Am J Gastroenterol. 2007; 102: 1542 - 3.
69. Spada C, Shah SK, Riccioni ME et al. Video capsule endoscopy in patients with known or suspected small bowel stricture previously tested with the dissolving patency capsule. J Clin Gastroenterol. 2007; 42: 576 - 82.
70. Schulz C,  K, Salheiser M, et al. Double-balloon enteroscopy in the diagnosis of suspected isolated Crohn"s disease of the small bowel. Dig Endosc. 2014; 26(2): 236 - 42. doi: 10.1111/den.12142.
K, Salheiser M, et al. Double-balloon enteroscopy in the diagnosis of suspected isolated Crohn"s disease of the small bowel. Dig Endosc. 2014; 26(2): 236 - 42. doi: 10.1111/den.12142.
71. Tontini GE, Vecchi M, Pastorelli L, et al. Differential diagnosis in inflammatory bowel disease colitis: State of the art and future perspectives. World J Gastroenterol. 2015; 21(1): 21 - 46.
72. IBD Mimics: Most Common Conditions Misdiagnosed as IBD. https://www.crohnscolitisfoundation.org/ClinicalPearls2020.
73. Gecse KB, Vermeire S. Differential diagnosis of inflammatory bowel disease: imitations and complications. Lancet Gastroenterol Hepatol 2018; 3(9): 644 - 653. doi: 10.1016/S2468-1253(18)30159-6.
74. Dignass A, Van Assche G, Lindsay JO, et al. The second European evidence-based Consensus on the diagnosis and management of Crohn"s disease: Current management. J Crohns Colitis. 2010; 4(1): 28 - 62.
75. Peyrin-Biroulet L, Sandborn W, Sands BE, et al. Selecting Therapeutic Targets inflammatory Bowel Disease (STRIDE): determining therapeutic goals for treat-to-target. Am J Gastroenterol.2015; 110(9): 1324 - 1338. https://doi.org/10.1038/ajg.2015.233.
76. Turner D, Ricciuto A, Lewis A. et al. International Organization for the Study of IBD. STRIDE-II: An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD): Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology. 2021; 160(5): 1570 - 1583. doi: 10.1053/j.gastro.2020.12.031.
77. Халиф И.Л. Лечебная тактика при язвенном колите. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2006; 3(16): 58 - 62.
78. Colombel JF, Panaccione R, Bossuyt P, et al. Effect of tight control management on Crohn's disease (CALM): a multicentre, randomised, controlled phase 3 trial. Lancet. 2018; 390(10114): 2779 - 2789. doi: 10.1016/S0140-6736(17)32641-7.
79.  F, Dignass A, Annese V, et al. 3rd European Evidence-based Consensus on the Diagnosis and Management of Crohn"s Disease 2016: Part 1: Diagnosis and Medical Management. J Crohns Colitis. 2017; 11(1): 3 - 25. doi: 10.1093/ecco-jcc/jjw168.
F, Dignass A, Annese V, et al. 3rd European Evidence-based Consensus on the Diagnosis and Management of Crohn"s Disease 2016: Part 1: Diagnosis and Medical Management. J Crohns Colitis. 2017; 11(1): 3 - 25. doi: 10.1093/ecco-jcc/jjw168.
80. Абдулганиева Д.И., Бакулев А.Л., Белоусова Е.А., и соавт. Раннее назначение генно-инженерных биологических препаратов при иммуновоспалительных заболеваниях: возможности и перспективы. Позиция экспертов. Альманах клинической медицины. 2020; 48(6): 422 - 36. doi: 10.18786/2072-0505-2020-48-050.
81. Tay GS, Binion DG, Eastwood D, et al. Multivariate analysis suggests improved perioperative outcome in Crohn"s disease patients receiving immunomodulator therapy after segmental resection and/or strictureplasty. Surgery. 2003; 34: 565 - 72.
82. Coward S, Kuenzig ME, Hazlewood G, et al. Comparative Effectiveness of Mesalamine, Sulfasalazine, Corticosteroids, and Budesonide for the Induction of Remission in Crohn"s Disease: A Bayesian Network Meta-analysis. Inflamm Bowel Dis. 2017; 23(3): 461 - 472. doi: 10.1097/MIB.0000000000001023.
83. Rezaie A, Kuenzig ME, Benchimol EI, et al. Budesonide for induction of remission in Crohn"s disease. Cochrane Database Syst Rev. 2015; (6): CD000296. doi: 10.1002/14651858.CD000296.pub4.
84. Ford AC, Kane SV, Khan KJ, et al. Efficacy of 5-aminosalicylates in Crohn"s disease: systematic review and meta-analysis. Am J Gastroenterol. 2011; 106: 617 - 29.
85. Torres J, Bonovas S, Doherty G, et al. ECCO guidelines on therapeutics in Crohn's disease: medical treatment. J Crohns Colitis. 2020; 14: 4 - 22.
86. Sandborn W, Sutherland L, Pearson D, et al. Azathioprine or 6-mercaptopurine for inducing remission of Crohn"s disease. Cochrane Database Syst Rev. 2000; (2): CD000545. doi: 10.1002/14651858.CD000545.
87. Herfarth HH, Kappelman MD, Long MD, et al. Use of Methotrexate in the Treatment of Inflammatory Bowel Diseases. Inflamm Bowel Dis. 2016; 22: 224 - 33.
88. Chande N, Patton PH, Tsoulis DJet al. Azathioprine or 6-mercaptopurine for maintenance of remission in Crohn"s disease. Cochrane Database Syst Rev. 2015; (10): CD000067.
89. Benchimol EI, Seow CH, Steinhart AH, et al. Traditional corticosteroids for induction of remission in Crohn"s disease. Cochrane Database Syst Rev 2008; 2: CD006792.
90. Khan KJ, Ullman TA, Ford AC, et al. Antibiotic therapy in inflammatory bowel disease: a systematic review and meta-analysis. Am J Gastroenterol. 2011; 106: 661 - 73.
91. Ho GT, Chiam P, Drummond H, et al. The efficacy of corticosteroid therapy in inflammatory bowel disease: analysis of a 5-year UK inception cohort. Aliment Pharmacol Ther. 2006; 24: 319 - 30.
92. Pearson DC, May GR, Fick GR, et al. Azathioprine for maintaining remission of Crohn"s disease. Cochrane Database Syst Rev. 2000(2): CD000067.
93. Hazlewood GS, Rezaie A, Borman M, et al. Comparative effectiveness of immunosuppressants and biologics for inducing and maintaining remission in Crohn"s disease: a network meta-analysis. Gastroenterology. 2015; 148(2): 344 - 54.
94. Singh S, Fumery M, Sandborn WJ, et al. Systematic review and network meta-analysis: first- and second-line biologic therapies for moderate-severe Crohn"s disease. Aliment Pharmacol Ther. 2018; 48(4): 394 - 409.
95. Cholapranee A, Hazlewood GS, Kaplan GG, et al. Systematic review with meta-analysis: comparative efficacy of biologics for induction and maintenance of mucosal healing in Crohn"s disease and ulcerative colitis controlled trials. Aliment Pharmacol Ther. 2017; 45(10): 1291 - 1302.
96. Sandborn WJ, Feagan BG, Loftus EV Jr, et al. Efficacy and Safety of Upadacitinib in a Randomized Trial of Patients With Crohn"s Disease. Gastroenterology. 2020; 158(8): 2123 - 2138. doi: 10.1053/j.gastro.2020.01.047.
97. Johnson AM, Barsky M, Ahmed W, et al. The Real-World Effectiveness and Safety of Ustekinumab in the Treatment of Crohn"s Disease: Results From the SUCCESS Consortium. Am J Gastroenterol. 2023; 118(2): 317 - 328. doi: 10.14309/ajg.0000000000002047.
98. Alric H, Amiot A, Kirchgesner J, et al. The effectiveness of either ustekinumab or vedolizumab in 239 patients with Crohn"s disease refractory to anti-tumour necrosis factor. Aliment Pharmacol Ther. 2020; 51(10): 948 - 957. doi: 10.1111/apt.15706.
99. Biemans VBC, van der Woude CJ, Dijkstra G, et al. Ustekinumab is associated with superior effectiveness outcomes compared to vedolizumab in Crohn"s disease patients with prior failure to anti-TNF treatment. Aliment Pharmacol Ther. 2020; 52(1): 123 - 134. doi: 10.1111/apt.15745
100. Loftus E.V.,  J, Lacerda A.P. et al. Upadacitinib Induction and Maintenance Therapy for Crohn"s Disease. Clinical Trial N Engl J Med. 2023; 388(21): 1966 - 1980. doi: 10.1056/NEJMoa2212728.
J, Lacerda A.P. et al. Upadacitinib Induction and Maintenance Therapy for Crohn"s Disease. Clinical Trial N Engl J Med. 2023; 388(21): 1966 - 1980. doi: 10.1056/NEJMoa2212728.
101. Sands BE, Irving PM, Hoops T, et al. Ustekinumab versus adalimumab for induction and maintenance therapy in biologic-naive patients with moderately to severely active Crohn"s disease: a multicentre, randomised, double-blind, parallel-group, phase 3b trial. Lancet. 2022; 399(10342): 2200 - 2211. doi: 10.1016/S0140-6736(22)00688-2. PMID: 35691323.
102. Prefontaine E, Macdonald JK, Sutherland LR. Azathioprine or 6-mercaptopurine for induction of remission in Crohn"s disease. Cochrane Database Syst Rev. 2009: CD000545.
103. Colombel JF, Sandborn WJ, Reinisch W, et al. Infliximab, azathioprine, or combination therapy for Crohn"s disease. N Engl J Med. 2010; 362(15): 1383 - 95. doi: 10.1056/NEJMoa0904492.
104.  O, Blumenstein I, Schulte-Bockholt A, et al. Combining infliximab and methotrexate in fistulizing Crohn"s disease resistant or intolerant to azathioprine. Aliment Pharmacol Ther. 2004; 19(3): 295 - 301.
O, Blumenstein I, Schulte-Bockholt A, et al. Combining infliximab and methotrexate in fistulizing Crohn"s disease resistant or intolerant to azathioprine. Aliment Pharmacol Ther. 2004; 19(3): 295 - 301.
105. Bressler B, Yarur A, Silverberg M et al. Vedolizumab and Anti-Tumour Necrosis Factor 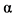 Real-World Outcomes in
Real-World Outcomes in  Inflammatory Bowel Disease Patients: Results from the EVOLVE Study. J Crohns Colitis. 2021; 15(10): 1694 - 1706. doi: 10.1093/ecco-jcc/jjab058.
Inflammatory Bowel Disease Patients: Results from the EVOLVE Study. J Crohns Colitis. 2021; 15(10): 1694 - 1706. doi: 10.1093/ecco-jcc/jjab058.
106. Huang Z, Ba Y, Kamble P, et al. P267 Sequencing of anti-TNF agents and gut-selective anti-lymphocyte trafficking (GSALT) therapy in the treatment of Crohn's disease (CD). J Crohns Colitis. 2021; 15: 302 - 303. doi:10.1093/ecco-jcc/jjab076.392.
107. Zhuleku E, Antolin-Fontes B, Borsi A, et al. Real-world outcomes associated with switching to anti-TNFs versus other biologics in Crohn"s Disease patients: A retrospective analysis using German claims data. Therap Adv Gastroenterol. 2022; 15: 17562848221130554. doi: 10.1177/17562848221130554.
108. Reinisch W, Gecse K, Halfvarson J et al Clinical Practice of Adalimumab and Infliximab Biosimilar Treatment in Adult Patients With Crohn"s Disease. Inflamm Bowel Dis. 2021; 27(1): 106 - 122. doi: 10.1093/ibd/izaa078.
109. Roblin X, Williet N, Boschetti G, et al. Addition of azathioprine to the switch of anti-TNF in patients with IBD in clinical relapse with undetectable anti-TNF trough levels and antidrug antibodies: a prospective randomised trial. Gut. 2020; 69(7): 1206 - 1212. doi: 10.1136/gutjnl-2019-319758.
110. Casanova MJ, Chaparro M,  M, et al. Effectiveness and Safety of the Sequential Use of a Second and Third Anti-TNF Agent in Patients With Inflammatory Bowel Disease: Results From the Eneida Registry. Inflamm Bowel Dis. 2020; 26(4): 606 - 616. doi: 10.1093/ibd/izz192.
M, et al. Effectiveness and Safety of the Sequential Use of a Second and Third Anti-TNF Agent in Patients With Inflammatory Bowel Disease: Results From the Eneida Registry. Inflamm Bowel Dis. 2020; 26(4): 606 - 616. doi: 10.1093/ibd/izz192.
111. Cordon JP, Arranz EM, Ramirez L, et al. What is the best strategy after failure to anti-TNF? Ustekinumab or other anti-TNF? J Crohns Colitis. 2020; 14 (Supplement_1): 554 - 554.
112. Ledder O, Turner D. Antibiotics in IBD: Still a Role in the Biological Era? Inflamm Bowel Dis. 2018; 24(8): 1676 - 1688.
113. Gionchetti P, Dignass A, Danese S, et al. 3rd European Evidence-based Consensus on the Diagnosis and Management of Crohn"s Disease 2016: Part 2: Surgical Management and Special Situations on behalf of ECCO. J Crohns Colitis. 2017; 11: 135 - 149.
114. Kawalec P, Mikrut A,  N, et al. Meta-analysis/systematic review tumor necrosis
N, et al. Meta-analysis/systematic review tumor necrosis 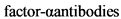 (infliximab, adalimumab and certolizumab) in Crohn"s disease: systematic review and meta-analysis. Arch Med Sci. 2013; 9: 765 - 779.
(infliximab, adalimumab and certolizumab) in Crohn"s disease: systematic review and meta-analysis. Arch Med Sci. 2013; 9: 765 - 779.
115. Khorrami S, Ginard D,  I, et al. Ustekinumab for the treatment of refractory Crohn"s disease the Spanish experience in a large multicentre open-label cohort. Inflamm Bowel Dis. 2016; 22: 1662 - 1669.
I, et al. Ustekinumab for the treatment of refractory Crohn"s disease the Spanish experience in a large multicentre open-label cohort. Inflamm Bowel Dis. 2016; 22: 1662 - 1669.
116. Prantera C, Zannoni F, Scribano ML, et al. An antibiotic regimen for the treatment of active Crohn"s disease: a randomized, controlled clinical trial of metronidazole plus ciprofloxacin. Am J Gastroenterol 1996; 91: 328 - 32.
117. Steinhart AH, Panaccione R, Targownik L, et al. Clinical Practice Guideline for the Medical Management of Perianal Fistulizing Crohn"s Disease: The Toronto Consensus. Inflamm Bowel Dis. 2019; 25(1): 1 - 13. doi: 10.1093/ibd/izy247.
118. Dewint P., Hansen B.E., Verhey E. et al. Adalimumab combined with ciprofloxacin is superior to adalimumab monotherapy in perianal fistula closure in Crohn"s disease: a randomised, double-blind, placebo controlled trial (ADAFI). Gut.2014; 63(2): 292 - 9. doi: 10.1136/gutjnl-2013-304488.
119. Tandon P, Rhee GG, Schwartz D, et al. Strategies to Optimize Anti-tumor Necrosis Factor Therapy for Perianal Fistulizing Crohn"s Disease: A Systematic Review. Dig Dis Sci. 2019; 64(11): 3066 - 3077. doi: 10.1007/s10620-019-05635-1.
120. Feuerstein JD, Ho EY, Shmidt E, et al. AGA Clinical Practice Guidelines on the Medical Management of Moderate to Severe Luminal and Perianal Fistulizing Crohn"s Disease. Gastroenterology. 2021; 160(7): 2496 - 2508. doi: 10.1053/j.gastro.2021.04.022.
121. Rahier JF, Magro F, Abreu C, et al. Second European evidence-based consensus on the prevention, diagnosis and management of opportunistic infections in inflammatory bowel disease. J Crohns Colitis. 2014; 8(6): 443 - 68. doi: 10.1016/j.crohns.2013.12.013.
122. Rutgeerts P, Feagan BG, Lichtenstein GR, et al. Comparison of scheduled and episodic treatment strategies of infliximab in Crohn"s disease. Gastroenterology 2004; 126: 402 - 13.
123. Guideline on similar biological medicinal products containing biotechnology-derived proteins as active substance: quality issues (revision 1). Available at: https://www.ema.europa.eu/en/documents/scientific-guideline/guideline-similar-biological-medicinal-products-containing-biotechnology-derived-proteins-active_en-2.pdf. Last accessed: September 2022.
124. IQVIA. The impact of biosimilar competition in Europe. 2021. Available at: https://www.iqvia.com/-/media/iqvia/pdfs/library/white-papers/the-impact-of-biosimilar-competition-in-europe-2021.pdf. Last accessed: 17 October 2022.
125. Humphry N. The Rise of Anti-TNF Biosimilars: Guidelines, Real-World Evidence, and Challenges to Acceptance. EMJ Gastroenterol. 2022; 11: 2 - 10. doi:10.33590/emjgastroenterol/10106137.
126. Danese S, Fiorino G, Raine T, et al. ECCO Position Statement on the Use of Biosimilars for Inflammatory Bowel Disease - An Update. J Crohns Colitis. 2017; 11(1): 26 - 34. doi: 10.1093/ecco-jcc/jjw198.
127. Cohen HP, Blauvelt A, Rifkin RM, et al. Switching Reference Medicines to Biosimilars: A Systematic Literature Review of Clinical Outcomes. Drugs. 2018; 78(4): 463 - 478. doi: 10.1007/s40265-018-0881-y.
128. Massimi D, Barberio B, Bertani L. et al. Switching from infliximab originator to SB2 biosimilar in inflammatory bowel diseases: a multicentric prospective real-life study. Ther Adv Gastroenterol. 2021; 14: 1 - 11.
129. Trystram N, Abitbol V, Tannoury J. et al. Outcomes after double switching from originator infliximab to biosimilar CT-P13 and biosimilar SB2 inpatients with inflammatory bowel disease: a 12-month prospective cohort study. Aliment Pharmacol Ther. 2021; 53: 887 - 99.
130. Mahmmod S, Schultheiss JPD, van Bodegraven AA. et al. Outcome of reverse switching from CT-P13 to originator infliximab in patients with inflammatory bowel disease. Inflamm Bowel Dis. 2021; 27: 1954 - 62.
131. Kaniewska M, Rosolowski M, Moniuzsko A. et al. Biosimilar infliximab versus originator in Crohn's disease 
 and
and  patients. Prz Gastroenterol. 2021; 16: 207 - 12.
patients. Prz Gastroenterol. 2021; 16: 207 - 12.
132. Morris GA, McNikol M, Boyle B. et al. Increasing biosimilar utilization at a pediatric inflammatory bowel disease center and associated cost savings: show me the money. Inflamm Bowel Dis. 2022; 28: 531 - 8.
133. Barberio B. Cingolani L, Canova C. et al. A propensity score-weighted comparison between adalimumab originator and its biosimilars, ABP501 and SB5, in inflammatory bowel disease: a multicenter Italian study. Ther Adv Gastroenterol. 2021; 14: 175 - 82.
134. Kurki P, Barry S., Bourges I. et al. Safety, immunogenicity and interchangeability of biosimilar monoclonal antibodies and fusion proteins: a regulatory perspective. Drugs. 2021; 81: 1881 - 96.
135. Billioud V, Ford AC, Tedesco ED, et al. Preoperative use of anti-TNF therapy and postoperative complications in inflammatory bowel diseases: a meta-analysis. J Crohns Colitis. 2013; 7(11): 853 - 67. doi: 10.1016/j.crohns.2013.01.014.
136. Aberra FN, Lewis JD, Hass D, et al. Corticosteroids and immunomodulators: post-operative infectious complication risk in inflammatory bowel disease patients. Gastroenterology. 2003; 125: 320 - 327.
137. Lightner AL, McKenna NP, Tse CS, et al. Postoperative outcomes in vedolizumab-treated Crohn's disease patients undergoing major abdominal operations. Aliment Pharmacol Ther. 2018; 47: 573 - 580.
138. Kotze PG, Ghosh S, Bemelman WA, Panaccione R. Preoperative use of anti-tumor necrosis factor therapy in Crohn's disease: promises and pitfalls. Intest Res. 2017; 15: 160 - 165.
139. Kotze PG, Saab MP, Saab B, et al. Tumor necrosis factor alpha inhibitors did not influence postoperative morbidity after elective surgical resections in Crohn's disease. Dig Dis Sci. 2017; 62: 456 - 464.
140. Law CCY, Narula A, Lightner AL, et al. Systematic review and meta-analysis: preoperative vedolizumab treatment and postoperative complications in patients with inflammatory bowel disease. J Crohns Colitis. 2018; 12: 538 - 545.
141. Lightner AL, McKenna NP, Tse CS, et al. Postoperative outcomes in ustekinumab-treated patients undergoing abdominal operations for Crohn's disease. J Crohns Colitis. 2018; 12: 402 - 407.
142. Novello M, Stocchi L, Holubar S, et al. Surgical outcomes of patients treated with ustekinumab vs. vedolizumab in inflammatory bowel disease: a matched case analysis. Int J Colorectal Dis. 2019; 34: 451 - 457.
143. Ahmed Ali U, Martin ST, Rao AD, et al. Impact of preoperative immunosuppressive agents on postoperative outcomes in Crohn's disease. Dis Colon Rectum. 2014; 57: 663 - 674.
144. McKenna NP, Habermann EB, Glasgow AE, et al. Intra-abdominal sepsis after ileocolic resection in Crohn's disease: the role of combination immunosuppression. Dis Colon Rectum. 2018; 61: 1393 - 1402.
145. Podugu A, Tandon K, Castro FJ. Crohn's disease presenting as acute gastrointestinal hemorrhage. World J Gastroenterol. 2016; 22: 4073 - 4078.
146. Raphaeli T, Menon R. Current treatment of lower gastrointestinal hemorrhage. Clin Colon Rectal Surg. 2012; 25: 219 - 227.
147. Korzenik JR. Massive Lower Gastrointestinal Hemorrhage in Crohn"s Disease. Curr Treat Options Gastroenterol. 2000; 3(3): 211 - 216. doi: 10.1007/s11938-000-0024-9.
148. Liu RQ, Guo D, Qiao SH, et al. Comparison of primary anastomosis and staged surgery in emergency treatment of complicated Crohn"s disease. J Dig Dis. 2020; 21: 724 - 734.
149. Шелыгин Ю.А., Ачкасов С.И., Решетов И.В., и соавт. Консенсус по спорным вопросам хирургического лечения болезни Крона с применением Дельфийского метода. Колопроктология. 2023; 22 (2): 172 - 183 doi: 10.33878/2073-7556-2023-22-2-172-183.
150. Werbin N, Haddad R, Greenberg R, et al. Free perforation in Crohn"s disease. Isr Med Assoc J. 2003; 5(3): 175 - 7.
151. Papi C, Festa V, Fagnani C, et al. Evolution of clinical behaviour in Crohn"s disease: predictive factors of penetrating complications. Dig Liver Dis. 2005; 37(4): 247 - 53. doi: 10.1016/j.dld.2004.10.012.
152. Bemelman WA, Warusavitarne J, Sampietro GM, et al. ECCO-ESCP Consensus on Surgery for Crohn"s Disease. J Crohns Colitis. 2018; 12(1): 1 - 16. doi: 10.1093/ecco-jcc/jjx061.
153. Agha FP, Ghahremani GG, Panella JS, et al. Appendicitis as the initial manifestation of Crohn"s disease: radiologic features and prognosis. AJR Am J Roentgenol. 1987; 149(3): 515 - 8. doi: 10.2214/ajr.149.3.515.
154. Kaplan GG, Jackson T, Sands BE, et al. The risk of developing Crohn"s disease after an appendectomy: a meta-analysis. Am J Gastroenterol. 2008; 103(11): 2925 - 31. doi: 10.1111/j.1572-0241.2008.02118.x.
155. Quaresma AB, Miranda EF, Kotze PG. Management of ileocecal Crohn's disease during surgical treatment for acute appendicitis: a systematic review. Arquivos De Gastroenterologia. 2021; 4(58): 560 - 565.
156. Adamina M, Bonovas S, Raine T, et al. ECCO Guidelines on Therapeutics in Crohn"s Disease: Surgical Treatment. J Crohns Colitis. 2020; 14(2): 155 - 168. doi: 10.1093/ecco-jcc/jjz187.
157. Clancy C, Boland T, Deasy J, et al. A Meta-analysis of Percutaneous Drainage Versus Surgery as the Initial Treatment of Crohn"s Disease-related Intra-abdominal Abscess. J Crohns Colitis. 2016; 10(2): 202 - 8. doi: 10.1093/ecco-jcc/jjv198.
158.  L,
L,  F, Miranda-Bautista
F, Miranda-Bautista  , et al. Safety and Efficacy of
, et al. Safety and Efficacy of  Treatment in Crohn"s Disease Patients with Abdominal Abscesses. Hepatogastroenterology. 2015; 62(139): 647 - 52.
Treatment in Crohn"s Disease Patients with Abdominal Abscesses. Hepatogastroenterology. 2015; 62(139): 647 - 52.
159. Mascolino A, Scerrino G, Gullo R, et al. Large retroperitoneal abscess extended to the inferior right limb secondary to a perforated ileal Crohn"s disease: the importance of the multidisciplinary approach. G Chir. 2016; 37(1): 37 - 41. doi: 10.11138/gchir/2016.37.1.037.
160. Варданян А.В., Шапина М.В., Полетова А.В., и соавт. Факторы риска развития осложнений у пациентов, оперированных по поводу осложненной формы болезни Крона. Хирург. 2021; 3(4): 44 - 52.
161. He X, Lin X, Lian L, et al. Preoperative percutaneous drainage of spontaneous intra-abdominal abscess in patients with Crohn's disease: a meta-analysis. J Clin Gastroenterol. 2015; 9(49): 82 - 90.
162. Jawhari A, Kamm MA, Ong C, et al. Intra-abdominal and pelvic abscess in Crohn"s disease: results of noninvasive and surgical management. Br J Surg. 1998; 85(3): 367 - 71. doi: 10.1046/j.1365-2168.1998.00575.x.
163. Poggioli G, Stocchi L, Laureti S, et al. Conservative surgical management of terminal ileitis: side-to-side enterocolic anastomosis. Dis Colon Rectum. 1997; 40(2): 234 - 7. doi: 10.1007/BF02054994.
164. Melton GB, Fazio VW, Kiran RP, et al. Long-term outcomes with ileal pouch-anal anastomosis and Crohn"s disease: pouch retention and implications of delayed diagnosis. Ann Surg. 2008; 248(4): 608 - 16. doi: 10.1097/SLA.0b013e318187ed64.
165. Panes J, Bouhnik Y, Reinisch W, et al. Imaging techniques for assessment of inflammatory bowel disease: joint ECCO and ESGAR evidence-based consensus guidelines. J Crohns Colitis. 2013; 7(7): 556 - 85. doi: 10.1016/j.crohns.2013.02.020.
166. Rieder F, Zimmermann EM, Remzi FH, et al. Crohn's disease complicated by strictures: a systematic review. Gut. 2013; 62: 1072 - 1084.
167. Navaneethan U, Lourdusamy V, Njei B, et al. Endoscopic balloon dilation in the management of strictures in Crohn's disease: a systematic review and meta-analysis of non-randomized trials. Surg Endosc 2016; 30: 5434 - 5443.
168. Варданян А.В., Кашников В.Н., Болихов К.В., и соавт. Лапароскопическая илеостомия при болезни Крона. Колопроктология, 2011; 3(37): 20 - 23.
169. Воробьев Г.И., Болихов К.В., Варданян А.В. Место лапароскопической илеостомии в лечении болезни Крона толстой кишки (обзор литературы). Колопроктология, 2009; 3(29): 52 - 58.
170. Stocchi L, Milsom JW, Fazio VW. Long-term outcomes of laparoscopic versus open ileocolic resection for Crohn's disease: follow-up of a prospective randomized trial. Surgery. 2008; 144: 622 - 627.
171. Maartense S, Dunker MS, Slors JF, et al. Laparoscopic-assisted versus open ileocolic resection for Crohn's disease: a randomized trial. Ann Surg. 2006; 243: 143 - 150.
172. Sagar PM, Dozois RR, Wolff BG. Long-term results of ileal pouch-anal anastomosis in patients with Crohn"s disease. Dis Colon Rectum. 1996; 39(8): 893 - 8. doi: 10.1007/BF02053988.
173. Simillis C, Purkayastha S, Yamamoto T, et al. A meta-analysis comparing conventional end-to-end anastomosis vs. other anastomotic configurations after resection in Crohn"s disease. Dis Colon Rectum. 2007; 50(10): 1674 - 87. doi: 10.1007/s10350-007-9011-8.
174. Stocchi L, Milsom JW, Fazio VW. Long-term outcomes of laparoscopic versus open ileocolic resection for Crohn"s disease: follow-up of a prospective randomized trial. Surgery. 2008; 144(4): 622 - 7. doi: 10.1016/j.surg.2008.06.016.
175. Tekkis PP, Purkayastha S, Lanitis S, et al. A comparison of segmental vs subtotal/total colectomy for colonic Crohn"s disease: a meta-analysis. Colorectal Dis. 2006; 8(2): 82 - 90. doi: 10.1111/j.1463-1318.2005.00903.x.
176. Teeuwen PH, Stommel MW, Bremers AJ, et al. Colectomy in patients with acute colitis: a systematic review. J Gastrointest Surg. 2009; 13: 676 - 686.
177. de Groof EJ, van der Meer JHM, Tanis PJ, et al. Persistent Mesorectal Inflammatory Activity is Associated With Complications After Proctectomy in Crohn"s Disease. J Crohns Colitis. 2019; 13(3): 285 - 293. doi: 10.1093/ecco-jcc/jjy131.
178. Mege D., Panis Y. Laparoscopic surgery for inflammatory bowel disease. Колопроктология. 2018; 2(64): 14 - 24.
179. Singh S, Ding NS, Mathis KL, et al. Systematic review with meta-analysis: faecal diversion for management of perianal Crohn"s disease. Aliment Pharmacol Ther. 2015; 42(7): 783 - 92.
180. Щукина О.Б., Собко В.Ю., Горбачева Д.Ш., и соавт. Прогнозирование хирургического лечения болезни Крона. Колопроктология. 2015; 4(54): 33 - 40.
181. Tichansky D, Cagir B, Yoo E, et al. Strictureplasty for Crohn's disease: meta-analysis. Dis Colon Rectum. 2000; 43: 911 - 9.
182. Shivashankar R, Edakkanambeth Varayil J, Scott Harmsen W, et al. Outcomes of endoscopic therapy for luminal strictures in Crohn's disease. Inflamm Bowel Dis. 2018; 24: 1575 - 1581.
183. Wibmer AG, Kroesen AJ,  J, et al. Comparison of strictureplasty and endoscopic balloon dilatation for stricturing Crohn's disease-review of the literature. Int J Colorectal Dis. 2010; 25: 1149 - 1157.
J, et al. Comparison of strictureplasty and endoscopic balloon dilatation for stricturing Crohn's disease-review of the literature. Int J Colorectal Dis. 2010; 25: 1149 - 1157.
184. Reese GE, Purkayastha S, Tilney HS, et al. Strictureplasty vs. resection in small bowel Crohn's disease: an evaluation of short-term outcomes and recurrence. Colorectal Dis. 2007; 9: 686 - 94.
185. Yamamoto T, Fazio VW, Tekkis PP. Safety and efficacy of strictureplasty for Crohn's disease: a systematic review and meta-analysis. Dis Colon Rectum. 2007; 50: 1968 - 86.
186. Dietz DW, Laureti S, Strong SA, et al. Safety and longterm efficacy of strictureplasty in 314 patients with obstructing small bowel Crohn"s disease. J Am Coll Surg. 2001; 192(3): 330 - 7. doi: 10.1016/s1072-7515(01)00775-x.
187. Шелыгин Ю.А., Халиф И.Л, Кашников В.Н., и соавт. Илеостомия в лечении болезни Крона толстой кишки с перианальными поражениями. Колопроктология. 2011; 3(37): 33.
188. Шапина М.В., Халиф И.Л., Нанаева Б.А. Применение цертолизумаба пэгола при болезни Крона. Обзор литературы. Колопроктология. 2016; 3(57): 102 - 108.
189. van Dongen LM, Lubbers EJC. Perianal fistulas in patients with Crohn's disease. Arch Surg. 1986; 121: 1187 - 90.
190. Yamamoto T, Allan RN, Keighley MR. Effect of fecal diversion alone on perianal Crohn's disease. World J Surg. 2000; 24: 1258 - 62.
191. El-Gazzaz G, Hull T, Church JM. Biological immunomodulators improve the healing rate in surgically treated perianal Crohn"s fistulas. Colorectal Dis. 2012; 14(10): 1217 - 23. DOI:10.1111/j.1463-1318.2012.02944.x.
192. Thornton M, Solomon MJ. Long-term indwelling seton for complex anal fistulas in Crohn's disease. Dis Colon Rectum. 2005; 48(3): 459 - 63.
193. Stellingwerf ME, van Praag EM, Tozer PJ, et al. Systematic review and meta-analysis of endorectal advancement flap and ligation of the intersphincteric fistula tract for cryptoglandular and Crohn"s high perianal fistulas. BJS Open. 2019; 3: 231 - 241. DOI: 10.1002/bjs5.50129.
194. Adegbola SO, Sahnan K, Tozer PJ, et al. Symptom Amelioration in Crohn"s Perianal Fistulas Using Video-Assisted Anal Fistula Treatment (VAAFT). J Crohns Colitis. 2018; 12: 1067 - 1072. DOI: 10.1093/ecco-jcc/jjy071.
195. Cao D, Li W, Ji Y, et al. Efficacy and safety of FiLaCTM for perianal fistulizing Crohn"s disease: a systematic review and meta-analysis. Tech Coloproctol. 2022; 26(10): 775 - 781. DOI: 10.1007/s10151-022-02682-1.
196. Rutgeerts P, Geboes K, Vantrappen G, et al. Predictability of the postoperative course of Crohn"s disease. Gastroenterology 1990; 99: 956 - 63.
197. Loftus Jr EV. Clinical epidemiology of inflammatory bowel disease: Incidence, prevalence, and environmental influences. Gastroenterology 2004; 126(6): 1504 - 17.
198. Полетова А.В., Шапина М.В., Халиф И.Л., и соавт. Эффективность послеоперационной противорецидивной терапии Адалимумабом и азатиоприном при болезни Крона. Колопроктолгия. 2018; 2(64): 73 - 77.
199. Peyrin-Biroulet L, Deltenre P, Ardizzone S, et al. Azathioprine and 6-mercaptopurine for the prevention of postoperative recurrence in Crohn"s disease: a meta-analysis. Am J Gastroenterol. 2009; 104(8): 2089 - 96. doi: 10.1038/ajg.2009.301.
200. Regueiro M, Schraut W, Baidoo L, et al. Infliximab prevents Crohn's disease recurrence after ileal resection. Gastroenterology. 2009; 136: 441 - 50.
201. Malchow H, Ewe K, Brandes JW, et al. European co-operative Crohn"s disease study (ECCDS): results of drug treatment. Gastroenterology 1984; 86: 249 - 66.
202. Savarino E, Bodini G, Dulbecco P, et al. Adalimumab is more effective than azathioprine and mesalamine at preventing postoperative recurrence of Crohn"s disease: a randomized controlled trial. Am J Gastroenterol. 2013; 108(11): 1731 - 42. doi: 10.1038/ajg.2013.287.
203. Yamada A, Komaki Y, Patel N, et al. The Use of Vedolizumab in Preventing Postoperative Recurrence of Crohn"s Disease. Inflamm Bowel Dis. 2018; 24(3): 502 - 509.
204. Lu TX, Cohen RD. Maneuvering Clinical Pathways for Crohn"s Disease. Curr Gastroenterol Rep. 2019; 21(5): 20.
205. Bhattacharya A, Shen B, Regueiro M. Endoscopy in Postoperative Patients with Crohn"s Disease or Ulcerative Colitis. Does It Translate to Better Outcomes? Gastrointest Endosc Clin N Am. 2019; 29(3): 487 - 514. doi: 10.1016/j.giec.2019.02.013.
206. Chu KF, Moran CJ, Wu K, et al. Performance of Surveillance MR Enterography (MRE) in Asymptomatic Children and Adolescents With Crohn"s Disease. J Magn Reson Imaging. 2019; 50(6): 1955 - 1963. doi: 10.1002/jmri.26811.
207. Deepak P, Axelrad JE, Ananthakrishnan AN. The Role of the Radiologist in Determining Disease Severity in Inflammatory Bowel Diseases. Gastrointest Endosc Clin N Am. 2019; 29(3): 447 - 470. doi: 10.1016/j.giec.2019.02.006.
208. Brand EC, Elias SG, Minderhoud IM, et al. Systematic Review and External Validation of Prediction Models Based on Symptoms and Biomarkers for Identifying Endoscopic Activity in Crohn"s Disease. Clin Gastroenterol Hepatol. 2020; 18(8): 1704 - 1718. doi: 10.1016/j.cgh.2019.12.014.
209. Terdiman JP. Prevention of postoperative recurrence in Crohn"s disease. Clin Gastroenterol Hepatol. 2008; 6(6): 616 - 20. doi: 10.1016/j.cgh.2007.08.020.
210. Papamichael K, Archavlis E, Lariou C, et al. Adalimumab for the prevention and/or treatment of post-operative recurrence of Crohn"s disease: a prospective, two-year, single center, pilot study. J Crohns Colitis. 2012; 6(9): 924 - 31. doi: 10.1016/j.crohns.2012.02.012.
211. Халиф И.Л., Варданян А.В., Шапина М.В., и соавт. Противорецидивная терапия болезни Крона в послеоперационном периоде (обзор литературы). Колопроктология. 2017; 3(61): 63 - 70.
212. Loly C, Belaiche J, Louis E. Predictors of severe Crohn"s disease. Scand J Gastroenterol 2008; 43: 948 - 54.
213. Министерство здравоохранения Российской федерации. Клинические рекомендации "Язвенный колит". Available: https://cr.minzdrav.gov.ru/schema/193_1
214. Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., и соавт. Современные возможности улучшения функционального состояния запирательного аппарата у пациентов с наличием превентивных кишечных стом. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2015; 5: 77 - 83.
215. Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., и соавт. Современные возможности улучшения функционального состояния запирательного аппарата у пациентов с наличием превентивных кишечных стом. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2015; 5: 77 - 83.
216. Фоменко О.Ю., Ачкасов С.И., Титов А.Ю., и соавт. Роль аноректальной манометрии, БОС-терапии и тибиальной нейромодуляции в диагностике и консервативном лечении анальной инконтиненции у пожилых. Клиническая геронтология. 2015; 5 - 6: 16 - 20.
217. Froslie KF, Jahnsen J, Moum BA, et al. Mucosal healing in inflammatory bowel disease: results from a Norwegian population-based cohort. Gastroenterology 2007; 133: 412 - 22.
218. Olivera P.A., Zuily S., Kotze P.G., et al. International consensus on the prevention of venous and arterial thrombotic events in patients with inflammatory bowel disease. Gastroenterology & Hepatology. 2021; 18: 858 - 873.
219. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений (ВТЭО) Флебология, 2015; 4(22).
220. Barbar S, Noventa F, Rossetto V, et al. A risk assessment model for the identification of hospitalized medical patients at risk for venous thromboembolism: the Padua Prediction Score. J Thromb Haemost. 2010; 8(11): 2450 - 7. doi: 10.1111/j.1538-7836.2010.04044.x.
221. Caprini J.A. Risk assessment as a guide to thrombosis prophylaxis. Curr Opin Pulm Med. 2010; 16(5): 448 - 52. doi: 10.1097/MCP.0b013e32833c3d3e.
222. Ishige T, Shimizu T, Watanabe K, et al. Expert consensus on vaccination in patients with inflammatory bowel disease in Japan. J Gastroenterol. 2023; 58(2): 135 - 157. doi: 10.1007/s00535-022-01953-w.
223. Kucharzik T, Ellul P, Greuter T, et al. ECCO Guidelines on the Prevention, Diagnosis, and Management of Infections in Inflammatory Bowel Disease. J Crohns Colitis. 2021; 15(6): 879 - 913. doi: 10.1093/ecco-jcc/jjab052.
224. Rubin LG, Levin MJ, Ljungman P, et al. 2013 IDSA clinical practice guideline for vaccination of the immunocompromised host. Clin Infect Dis. 2014; 58(3): 309 - 18.
225. Вакцины и иммунопрофилактика в современном мире: руководство для врачей/под ред. Л.С. Намазовой-Барановой, Н.И. Брико, И.В. Фельдблюм. - М.: ПедиатрЪ, 2021. - 646 с.
226. Приказ МЗ РФ от 06.12.2021 N 1122н "Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям", Методические указания МУ 3.3.1.1095-02. Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок.
227. Санитарные правила и нормы СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней" Постановление главного санитарного врача от 28 января 2021 г. N 4.
228. Стратегия развития иммунопрофилактики инфекционных заболеваний на период до 2035 года, утверждена распоряжением Правительства Российской Федерации от 18 сентября 2020 г. N 2390-р.
229. Временные методические рекомендации "Порядок проведения вакцинации против новой коронавирусной инфекции (COVID-19)" Москва 2022 г. Available: https://static-0.minzdrav.gov.ru/system/attachments/attaches/system/attachments/attaches/000/060/087/original/Методические_рекомендации_02062022_%282%29.pdf?1655803717
230. Jena A, James D, Singh AK, et al. Effectiveness and Durability of COVID-19 Vaccination in 9447 Patients With IBD: A Systematic Review and Meta-Analysis. Clin Gastroenterol Hepatol. 2022; 20(7): 1456 - 1479.
231. Kubas A, Malecka-Wojciesko E. COVID-19 Vaccination in Inflammatory Bowel Disease (IBD). J Clin Med. 2022; 11(9): 2676. doi: 10.3390/jcm11092676.
232. Временные методические рекомендации: "Болезни органов пищеварения в условиях пандемии новой коронавирусной инфекции (COVID-19)". Версия 2. Консенсус экспертов Межрегиональной общественной организации "Общество гастроэнтерологов и гепатологов "Северо-Запад", Российского общества профилактики неинфекционных заболеваний и Профильной комиссии по терапии и общей врачебной практике Минздрава России. Профилактическая медицина. 2021; 5(24): 4 - 41.
233. D'Haens G,  J, Louis E, et al. Upadacitinib Was Efficacious and Well-tolerated Over 30 Months in Patients With Crohn's Disease in the CELEST Extension Study. Clinical Gastroenterology and Hepatology 2022; 20: 2337 - 2346.
J, Louis E, et al. Upadacitinib Was Efficacious and Well-tolerated Over 30 Months in Patients With Crohn's Disease in the CELEST Extension Study. Clinical Gastroenterology and Hepatology 2022; 20: 2337 - 2346.
234. Stavem K. Switching from one reference biological to another in stable patients for non-medical reasons: a literature search and brief review. J Mark Access Health Policy. 2021; 9(1): 1964792. Published online 2021Aug 20. DOI: 10.1080/20016689.2021.1964792
235. Князев О.В., Звяглова М.Ю., Каграманова А.В. и соавт. Потеря ответа и частота нежелательных явлений у пациентов с язвенным колитом и болезнью Крона при переходе с оригинального препарата инфликсимаб на его биосимиляры. Терапевтический архив. 2021; 93 (2): 150 - 157. DOI: 10.26442/00403660.2021.02.200624.
236. Madanchi M, Fagagnini S, Fournier N et al.Swiss IBD Cohort Study Group, The Relevance of Vitamin and Iron Deficiency in Patients with Inflammatory Bowel Diseases in Patients of the Swiss IBD Cohort, Inflammatory Bowel Diseases, Volume 24, Issue 8, August 2018, Pages 1768 - 1779
237. Issa M, Vikayapal A, Gracham MB et al. Impact of Clostridium difficile in inflammatory bowel disease patients. Clin Gastroenterol Hepatol. 2007; 5: 345 - 351.
238. Rodeman JF, Dubberke ER, Reske KA et al. Incidence of Clostridium difficile in inflammatory bowel disease. Clin Gastroenterol Hepatol. 2007; 5: 339 - 344.
239. Issa M, Ananthakrishnan AN, Binion DG. Clostridium difficile and inflammatory bowel disease. Inflamm Bowel Dis. 2008; 14: 1432 - 42.
240. Buttgereit F, Brand MD, Burmester GR. Equivalent doses and relative drug potencies for non-genomic glucocorticoid effects: a novel glucocorticoid hierarchy. Biochem Pharmacol. 1999 Jul 15; 58(2): 363 - 8.
241. Mager DE, Lin SX, Blum RA, et al. Dose equivalency evaluation of major corticosteroids: pharmacokinetics and cell trafficking and cortisol dynamics. J Clin Pharmacol. 2003 Nov; 43(11): 1216 - 27.
242. Janier M, Hegyi V, Dupin N,et al. 2014 European guideline on the management of syphilis. J Eur Acad Dermatol Venereol. 2014 Dec; 28(12): 1581 - 93.
243. van der Have M, Belderbos TD, Fidder HH, Dutch Initiative on Crohn and Colitis (ICC). Screening prior to biological therapy in Crohn"s disease: adherence to guidelines and prevalence of infections. Results from a multicentre retrospective study. Dig Liver Dis. 2014 Oct; 46(10): 881 - 6.
244. Velayos FS, Sandborn WJ. Use of azathioprine and 6MP in postoperative Crohn"s: changing natural history or just along for the ride? Am J Gastroenterol. 2009 Aug; 104(8): 2097 - 9.
245. De Cruz P, Kamm MA, Hamilton AL et al. Efficacy of thiopurines and adalimumab in preventing Crohn"s disease recurrence in high-risk patients - a POCER study analysis. Aliment Pharmacol Ther. 2015 Oct; 42(7): 867 - 79.
246. Vader JP, Froehlich F, Juillerat P, Burnand B, Felley C, Gonvers JJ, Mottet C, Pittet V, Dubois RW, Wietlisbach V, Michetti P. Appropriate treatment for Crohn"s disease: methodology and summary results of a multidisciplinary international expert panel approach--EPACT. Digestion. 2006; 73(4): 237 - 48
247. Kappelman MD, Palmer L, Boyle BM, et al. Quality of care in inflammatory bowel disease: a review and discussion. Inflamm Bowel Dis. 2010 Jan; 16(1): 125 - 33.
248. Fiorino G, Allocca M, Chaparro M, et al.'Quality of Care' Standards in Inflammatory Bowel Disease: A Systematic Review, Journal of Crohn"s and Colitis. 2019 Jan, 13(1): 127 - 137.
249. Tulchinsky H. et al. Comprehensive pouch clinic concept for follow-up of patients after ileal pouch anal anastomosis: report of 3 years" experience in a tertiary referral center.Inflamm Bowel Dis, 2008. 14(8): 1125 - 32.
250. Calvet X,  J, Alfaro N, et al. Delphi consensus statement: Quality Indicators for Inflammatory Bowel Disease Comprehensive Care Units. J Crohns Colitis. 2014 Mar; 8(3): 240 - 51.
J, Alfaro N, et al. Delphi consensus statement: Quality Indicators for Inflammatory Bowel Disease Comprehensive Care Units. J Crohns Colitis. 2014 Mar; 8(3): 240 - 51.
251. Meima-van Praag EM, Buskens CJ, Hompes R, et al. Surgical management of Crohn"s disease: a state of the art review. Int J Colorectal Dis. 2021 Jun; 36(6): 1133 - 1145.
252. Cosnes J, Bourrier A, Laharie D, et al. Groupe d"Etude  des Affections Inflammatoires du Tube Digestif (GETAID). Early administration of azathioprine vs conventional management of Crohn"s Disease: a randomized controlled trial. Gastroenterology. 2013 Oct; 145(4): 758 - 65 .e2; quiz e14-5.
des Affections Inflammatoires du Tube Digestif (GETAID). Early administration of azathioprine vs conventional management of Crohn"s Disease: a randomized controlled trial. Gastroenterology. 2013 Oct; 145(4): 758 - 65 .e2; quiz e14-5.
253. Rayer, C., Nachury, M., Bourreille, A. et al. Efficacy of ustekinumab, vedolizumab, or a second anti-TNF agent after the failure of a first anti-TNF agent in patients with Crohn's disease: a multicentre retrospective study. BMC Gastroenterol 22, 498 (2022)
254. Sharip MT, Nishad N, Pillay L, Goordoyel N, Goerge S, Subramanian S. Ustekinumab or Vedolizumab after Failure of Anti-TNF Agents in Crohn"s Disease: A Review of Comparative Effectiveness Studies. J Clin Med. 2024 Apr 10; 13(8): 2187.
255. Barberio B, Gracie DJ, Black CJ, Ford AC. Efficacy of biological therapies and small molecules in induction and maintenance of remission in luminal Crohn"s disease: systematic review and network meta-analysis. Gut. 2023 Feb; 72(2): 264 - 274.
256. Singh S, Murad MH, Fumery M, Sedano R, Jairath V, Panaccione R, Sandborn WJ, Ma C. Comparative efficacy and safety of biologic therapies for moderate-to-severe Crohn"s disease: a systematic review and network meta-analysis. Lancet Gastroenterol Hepatol. 2021 Dec; 6(12): 1002 - 1014.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ
И ПЕРЕСМОТРУ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
|
N
|
Ф.И.О.
|
Ученая степень
|
Ученое звание
|
Профессиональная ассоциация
|
|
1.
|
Абдулганиева Диана Ильдаровна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
2.
|
Абдулхаков Рустем Аббасович
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
3.
|
Адамян Лейла Владимировна
|
д.м.н.
|
Профессор, Академик РАН
|
Ассоциация колопроктологов России
|
|
4.
|
Алексеева Ольга Поликарповна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
5.
|
Алексеенко Сергей Алексеевич
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
6.
|
Александров Тимофей Леонидович
|
Российская гастроэнтерологическая ассоциация
|
||
|
7.
|
Аносов Иван Сергеевич
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
8.
|
Ачкасов Сергей Иванович
|
д.м.н.
|
Профессор, член-корр. РАН
|
Ассоциация колопроктологов России
|
|
9.
|
Бакулин Игорь Геннадьевич
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
10.
|
Барышева Ольга Юрьевна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
11.
|
Белоусова Елена Александровна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
12.
|
Болихов Кирилл Валерьевич
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
13.
|
Варданян Армен Восканович
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
14.
|
Веселов Виктор Владимирович
|
д.м.н.
|
Профессор
|
Ассоциация колопроктологов России
|
|
15.
|
Головенко Олег Владимирович
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
16.
|
Губонина Ирина Владимировна
|
к.м.н.
|
Доцент
|
Российская гастроэнтерологическая ассоциация
|
|
17.
|
Долгушина Анастасия Ильинична
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
18.
|
Драпкина Оксана Михайловна
|
д.м.н.
|
Профессор, Академик РАН
|
Российская гастроэнтерологическая ассоциация
|
|
19.
|
Ивашкин Владимир Трофимович
|
д.м.н.
|
Профессор, Академик РАН
|
Российская гастроэнтерологическая ассоциация
|
|
20.
|
Жигалова Татьяна Николаевна
|
к.м.н.
|
Российская гастроэнтерологическая ассоциация
|
|
|
21.
|
Каграманова Анна Валерьевна
|
к.м.н.
|
Российская гастроэнтерологическая ассоциация
|
|
|
22.
|
Кашников Владимир Николаевич
|
д.м.н.
|
Доцент
|
Ассоциация колопроктологов России
|
|
23.
|
Князев Олег Владимирович
|
д.м.н.
|
Российская гастроэнтерологическая ассоциация
|
|
|
24.
|
Костенко Николай Владимирович
|
д.м.н.
|
Профессор
|
Ассоциация колопроктологов России
|
|
25.
|
Ликутов Алексей Александрович
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
26.
|
Ливзан Мария Анатольевна
|
д.м.н.
|
Профессор, член-корр. РАН
|
Российская гастроэнтерологическая ассоциация
|
|
27.
|
Ломакина Екатерина Юрьевна
|
Российская гастроэнтерологическая ассоциация
|
||
|
28.
|
Лоранская Ирина Дмитриевна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
29.
|
Маев Игорь Вениаминович
|
д.м.н.
|
Профессор, академик РАН
|
Российская гастроэнтерологическая ассоциация
|
|
30.
|
Макарчук Павел Александрович
|
к.м.н.
|
Российская гастроэнтерологическая ассоциация
|
|
|
31.
|
Мингазов Айрат Фанилевич
|
Ассоциация колопроктологов России
|
||
|
32.
|
Москалев Алексей Игоревич
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
33.
|
Намазова-Баранова Лейла Сеймуровна
|
д.м.н.
|
Профессор, академик РАН
|
Ассоциация колопроктологов России
|
|
34.
|
Назаров Илья Владимирович
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
35.
|
Нанаева Бэлла Александровна
|
к.м.н
|
Ассоциация колопроктологов России
|
|
|
36.
|
Никитина Наталья Васильевна
|
к.м.н.
|
Российская гастроэнтерологическая ассоциация
|
|
|
37.
|
Одинцова Альфия Харисовна
|
к.м.н
|
Российская гастроэнтерологическая ассоциация
|
|
|
38.
|
Осипенко Марина Федоровна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
39.
|
Ощепков Андрей Владимирович
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
40.
|
Разумовский Александр Юрьевич
|
д.м.н.
|
Профессор, член-корр. РАН
|
Ассоциация колопроктологов России
|
|
41.
|
Ревишвили Амиран Шотаевич
|
д.м.н.
|
Профессор, академик РАН
|
Ассоциация колопроктологов России
|
|
42.
|
Решетов Игорь Владимирович
|
д.м.н.
|
Профессор, академик РАН
|
Ассоциация колопроктологов России
|
|
43.
|
Павленко Владимир Васильевич
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
44.
|
Полуэктова Елена Александровна
|
к.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
45.
|
Родоман Григорий Владимирович
|
д.м.н.
|
Профессор
|
Ассоциация колопроктологов России
|
|
46.
|
Сажин Александр Вячеславович
|
д.м.н.
|
Профессор, член-корр. РАН
|
Ассоциация колопроктологов России
|
|
47.
|
Ситкин Станислав Игоревич
|
к.м.н.
|
Доцент
|
Российская гастроэнтерологическая ассоциация
|
|
48.
|
Скалинская Мария Игоревна
|
к.м.н.
|
Российская гастроэнтерологическая ассоциация
|
|
|
49.
|
Сурков Андрей Николаевич
|
д.м.н.
|
Ассоциация колопроктологов России
|
|
|
50.
|
Сушков Олег Иванович
|
д.м.н.
|
Ассоциация колопроктологов России
|
|
|
51.
|
Тарасова Лариса Владимировна
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
52.
|
Успенская Юлия Борисовна
|
д.м.н
|
Российская гастроэнтерологическая ассоциация
|
|
|
53.
|
Темирбулатов Виль Мамилович
|
д.м.н.
|
Профессор, член-корр. РАН
|
Ассоциация колопроктологов России
|
|
54.
|
Фролов Сергей Алексеевич
|
д.м.н.
|
Доцент
|
Ассоциация колопроктологов России
|
|
55.
|
Хатьков Игорь Евгеньевич
|
д.м.н.
|
Профессор, академик РАН
|
Ассоциация колопроктологов России
|
|
56.
|
Хлынова Ольга Витальевна
|
д.м.н.
|
Профессор, член-корр. РАН
|
Российская гастроэнтерологическая ассоциация
|
|
57.
|
Чашкова Елена Юрьевна
|
к.м.н
|
Ассоциация колопроктологов России
|
|
|
58.
|
Шабунин Алексей Васильевич
|
д.м.н.
|
Профессор, академик РАН
|
Ассоциация колопроктологов России
|
|
59.
|
Шелыгин Юрий Анатольевич
|
д.м.н.
|
Профессор, академик РАН
|
Ассоциация колопроктологов России
|
|
60.
|
Шифрин Олег Самуилович
|
д.м.н.
|
Профессор
|
Российская гастроэнтерологическая ассоциация
|
|
61.
|
Шкурко Татьяна Всеволодовна
|
к.м.н.
|
Ассоциация колопроктологов России
|
|
|
62.
|
Щукина Оксана Борисовна
|
д.м.н.
|
Российская гастроэнтерологическая ассоциация
|
Конфликты интересов у всех перечисленных авторов отсутствуют.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врачи-гастроэнтерологи
2. Врачи-колопроктологи
3. Врачи-хирурги
4. Врачи-терапевты
5. Врачи общей практики (семейные врачи)
6. Врачи-эндоскописты
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
|
УДД
|
Расшифровка
|
|
1
|
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований с применением метаанализа
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Таблица П2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД
|
Расшифровка
|
|
1
|
Систематический обзор рандомизированных клинических исследований с применением метаанализа
|
|
2
|
Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа
|
|
3
|
Нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследование "случай-контроль"
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Таблица П3. Шкала оценки уровней убедительности рекомендаций (УРР) для методов профилактики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УРР
|
Расшифровка
|
|
A
|
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР (клинических рекомендации) но не чаще 1 раз в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ
И ДОЗ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ, ИНСТРУКЦИИ
ПО ПРИМЕНЕНИЮ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, организуется и оказывается согласно:
Федеральному закону от 21.11.2011 г. N 323-ФЗ (с изменениями на 13.06.2023 г.) "Об основах охраны здоровья граждан в Российской Федерации"
Постановлению Правительства Российской Федерации от 17.11.2021 г. N 1968 "Об утверждении Правил поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 - 9 и 11 статьи 37 Федерального закона "Об основах охраны здоровья граждан в Российской Федерации"
Приказу Министерства здравоохранения Российской Федерации от 2 апреля 2010 г. N 206н (ред. от 21.02.2020) "Об утверждении порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля"
Приказу Министерства здравоохранения Российской Федерации от 12 ноября 2012 г. N 906н "Об утверждении Порядка оказания медицинской помощи населению по профилю "гастроэнтерология"
Приказу Министерства здравоохранения Российской Федерации от 14.02.2022 N 76н "Об утверждении стандарта медицинской помощи взрослым при болезни Крона (диагностика и лечение)"
Приказу Министерства здравоохранения Российской Федерации от 15.03.2022 N 168н "Об утверждении порядка проведения диспансерного наблюдения за взрослыми"
Приказу Министерства здравоохранения Российской Федерации от 23.12.2020 N 1363н "Об утверждении Порядка направления застрахованных лиц в медицинские организации, функции и полномочия учредителей в отношении которых осуществляют Правительство Российской Федерации или федеральные органы исполнительной власти, для оказания медицинской помощи в соответствии с едиными требованиями базовой программы обязательного медицинского страхования"
Приказу Министерства здравоохранения Российской Федерации от 10.05.2017 N 203н "Об утверждении критериев оценки качества медицинской помощи"
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
- Статьей 76 Федерального Закона Российской Федерации от 21 ноября 2011 г. N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации", в части разработки и утверждении медицинскими профессиональными некоммерческими организациями клинических рекомендаций (протоколов лечения) по вопросам оказания медицинской помощи
- Постановления Правительства Российской Федерации от 29 декабря 2022 г. N 2497 "О Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2023 год и на плановый период 2024 и 2025 годов"
- Приказом Министерства здравоохранения Российской Федерации от 2 апреля 2010 г. N 206н (ред. от 21.02.2020) "Об утверждении порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля"
- Приказом Министерства здравоохранения Российской Федерации от 12 ноября 2012 г. N 906н "Об утверждении Порядка оказания медицинской помощи населению по профилю "гастроэнтерология"
- Приказом Министерства здравоохранения Российской Федерации от 15.03.2022 г. N 168н "Об утверждении порядка проведения диспансерного наблюдения за взрослыми"
- Приказом Министерства здравоохранения Российской Федерации от 14.02.2022 г. N 76н "Об утверждении стандарта медицинской помощи взрослым при болезни Крона (диагностика и лечение)"
- Приказом Министерства здравоохранения Российской Федерации от 10 мая 2017 г. N 203н "Об утверждении критериев оценки качества медицинской помощи"
- Приказом Министерства здравоохранения Российской Федерации от 23.12.2020 N 1363н "Об утверждении Порядка направления застрахованных лиц в медицинские организации, функции и полномочия учредителей в отношении которых осуществляют Правительство Российской Федерации или федеральные органы исполнительной власти, для оказания медицинской помощи в соответствии с едиными требованиями базовой программы обязательного медицинского страхования".
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
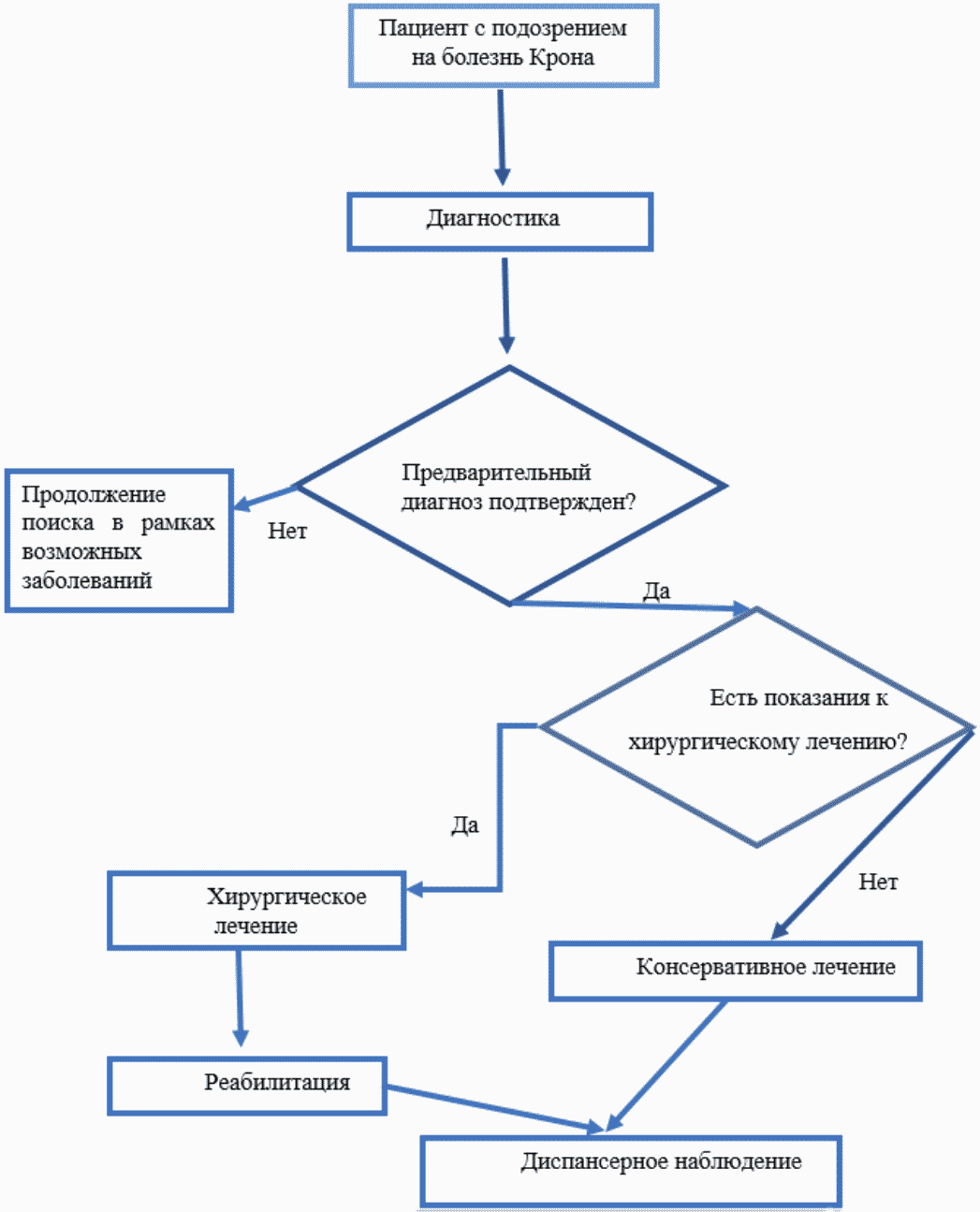
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
БК - хроническое воспалительное заболевание ЖКТ, которое может затрагивать любой отдел ЖКТ, от рта до заднего прохода. На настоящий момент способа полностью исцелиться от этого заболевания не существует, поэтому при БК в большинстве случаев проводится постоянная терапия различными лекарствами, чтобы подавить и ограничить распространение воспаления, а также, чтобы предотвратить развитие осложнений. При БК чередуются периоды усиления заболевания (рецидивы) и периоды улучшения самочувствия (наступает ремиссия). У очень небольшой части больных ремиссия может сохраняться и без лечения, однако, в подавляющем большинстве случаев без постоянной терапии развиваются частые обострения и, главное, прогрессирует необратимое повреждение кишечной стенки. Со временем это приводит к осложнениям, которые включают сужение кишки (стриктуру), свищи (гнойные ходы из кишечника на кожу, во влагалище, в мочевой пузырь или в другую петлю кишки), анальные поражения, общее истощение организма (кахексию) и даже рак. Эти осложнения могут угрожать жизни и часто требуют операции с удалением части кишечника, нередко - с формированием кишечной стомы.
Поскольку БК - достаточно редкое заболевание, человек с этой болезнью должен по возможности наблюдаться у врача, специализирующегося на лечении именно данной патологии, и строго следовать его рекомендациям по длительной, нередко, пожизненной, лекарственной терапии. Вы также можете облегчить течение заболевания, отказавшись от курения, если вы курите. Ни уровень физической нагрузки, ни прием конкретных продуктов питания, не влияют на риск обострения БК так, как влияет на него нерегулярный прием лекарств и несвоевременное обращение к специалисту.
Приложение Г1 - ГN
ШКАЛЫ ОЦЕНКИ,
ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ СОСТОЯНИЯ
ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Нет