МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
ПСИХИЧЕСКИЕ И ПОВЕДЕНЧЕСКИЕ РАССТРОЙСТВА,
ВЫЗВАННЫЕ УПОТРЕБЛЕНИЕМ ПСИХОАКТИВНЫХ ВЕЩЕСТВ. СИНДРОМ
ОТМЕНЫ ПСИХОАКТИВНЫХ ВЕЩЕСТВ (АБСТИНЕНТНОЕ СОСТОЯНИЕ,
ВЫЗВАННОЕ УПОТРЕБЛЕНИЕМ ПСИХОАКТИВНЫХ ВЕЩЕСТВ)
МКБ10: F11.3, F12.3, F13.3, F14.3, F15.3, F16.3, F18.3, F19.3
Год утверждения (частота пересмотра): 2018 (пересмотр каждые 3 года)
ID: 32
URL
Профессиональные ассоциации
- Ассоциация наркологов России (Профессиональное сообщество врачей-наркологов)
Ключевые слова
- Синдром отмены
- Абстинентный синдром
- ПАВ
- Опиоиды
- Каннабиноиды
- Седативные или снотворные вещества
- Кокаин
- Психостимуляторы
- Кофеин
- Галлюциногены
- Летучие растворители (ингалянты)
Список сокращений
ААС - алкогольный абстинентный синдром
АД - артериальное давление
АС - абстинентный синдром
ВНС - вегетативная нервная система
ВОЗ - Всемирная Организация Здравоохранения
ВЭЖХ - высокоэффективная жидкостная хроматография
ГАМК - гамма-аминомасляная кислота
ГХ - газовая хроматография
ДА - Дофамин
ИФА - иммунно-ферментный анализ
КА - катехоламины
ЛС - лекарственные средства
ЛСД (LSD) - диэтиламид лизергиновой кислоты, lysergic acid diethylamide. Аббревиатура сохранилась от нем.: 
МЗ РФ - Министерство здравоохранения Российской Федерации
МКБ-10 - международная классификация болезней 10-го пересмотра
МПП - минимально переносимое потребление
МС - масс-спектрометрия
НА - норадреналин
НД - наркологический диспансер
НПВС - нестероидные противовоспалительные средства
НЯ - нежелательное явление
ОАС - опийный абстинентный синдром
ПАВ - психоактивное вещество
ПВН - патологическое влечение к наркотику
ПР - побочная реакция
СЗ - синдром зависимости
СО - синдром отмены
ТГК - тетрагидроканнабиноиды
УЗИ - ультразвуковое исследование
УНП ООН - Организация Объединенных Наций, Управление по наркотикам и преступности
ЦНС - центральная нервная система
ЧДД - число дыхательных движений
ЧСС - частота сердечных сокращений
ЭКГ - электрокардиограмма
Эхо-ЭГ - эхоэнцефалография
ЭЭГ - электроэнцефалограмма
DSM-5 (Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition) - Диагностическая и статистическая классификация психических болезней, пятый пересмотр
EFSA - European Food Safety Authority (Европейское Агентство по безопасности продуктов, Европа)
FDA - Food and Drug Administration (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, США)
MDMA (МДМА) - methylenedioxymethamphetamine (метилендиоксиметамфетамин)
MDA (МДА) - methylenedioxyamphetamine (метилендиоксиамфетамин)
Rg - рентгенография
5-HT (5-hydroxytriptamine) - 5-гидрокситриптамин, серотониновый рецептор
Термины и определения
Абстинентный синдром (физическая зависимость) - это комплекс вегетативных, соматических, неврологических и психических нарушений, возникающих у больных алкоголизмом/наркоманией (токсикоманией) вслед за прекращением или резким сокращением более или менее длительной и массивной алкогольной/наркотической интоксикации.
Мидриаз (лат. mydriasis) - расширение зрачка, диаметр более 2,5 мм
Миоз (лат. miosis) - сужение зрачка, диаметр менее 2,5 мм
Синдром зависимости - это сочетание физиологических, поведенческих и когнитивных явлений, при которых употребление ПАВ или класса веществ занимает в системе ценностей больного ведущее место (определение по МКБ-10).
Синдром патологического влечения (психическая зависимость) - это определенная (патологическая) психическая деятельность, имеющая следующие составляющие: идеаторную (мыслительную), поведенческую, аффективную (эмоциональную), вегетативную и сенсорную.
Тремор (лат. tremor, "дрожание") - это ритмические, быстрые сокращения мышц туловища или конечностей непроизвольного характера.
1. Краткая информация
1.1 Определение
Синдром отмены (СО) или абстинентный синдром (АС) - это группа симптомов различного сочетания и степени тяжести, возникающих при полном прекращении приема вещества или снижении его дозы после неоднократного, обычно длительного и/или в высоких дозах употребления данного вещества. Начало и течение синдрома отмены ограничены во времени и соответствуют типу вещества и дозе, непосредственно предшествующей воздержанию.
1.2. Этиология и патогенез
Влияние наркотиков на организм человека, его жизнедеятельность и функции, проявляется в трех различных направлениях:
1) психоактивные вещества (ПАВ) специфически влияют на определенные системы и структуры мозга, вызывая, таким образом, развитие синдрома зависимости (СЗ). Именно этот синдром является ведущим, стержневым в клинической картине наркологических заболеваний;
2) ПАВ обладают токсическим воздействием практически на все внутренние органы и системы организма. Несмотря на то, что токсическое поражение различных органов не связано напрямую с проявлением синдрома зависимости, в то же время временная нетрудоспособность, инвалидизация и смертность больных наркологической патологией чаще всего обусловлены именно последствиями и осложнениями токсических эффектов ПАВ;
3) сформированный СЗ у родителей влияет на потомство. Многочисленными медико-генетическими исследованиями доказано, что у детей, родившихся от больных алкоголизмом или наркоманиями, существенно повышен риск развития этих заболеваний. Кроме того, у большинства из них выступают те или иные характерологические и поведенческие расстройства: повышенная возбудимость, агрессивность, склонность к риску, развитию депрессивных состояний и т.д. Потребление алкоголя матерью в период беременности приводит к развитию алкогольного синдрома плода, а использование ею наркотиков может стать причиной рождения ребенка с сформировавшейся наркотической зависимостью [1].
Механизм развития СЗ от наркотиков при экзогенном их введении, по сути своей, едины [1], на современном этапе это уже считается доказанным фактом. В патогенезе наркоманий участвуют, в основном, следующие нейромедиаторные системы [1, 2, 3, 4]:
1) катехоламиновая (КА), дофаминовая (ДА) системы в лимбических структурах мозга;
2) эндогенная опиоидная система;
3) ГАМК-ергическая система (ГАМК - гамма-аминомасляная кислота);
4) N-метил-D-аспартатная система;
5) эндогенные лиганды каннабиноидных рецепторов (анандамид и палмитоилэтаноламид).
В патогенезе СЗ от опиоидов, различных психостимуляторов основную роль играют 1 - 3 системы (см. информацию выше). При длительном приеме ПАВ развивается дефицит нейромедиаторов. В качестве механизма компенсации выступает усиленный синтез КА и подавление активности ферментов их метаболизма, в первую очередь монооксидазы и 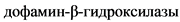 , контролирующей превращение дофамина (ДА) в норадреналин (НА). Происходит формирование ускоренного кругооборота КА. При прекращении приема ПАВ усиленное высвобождение КА из депо прекращается, но остается ускоренным их синтез. Вследствие изменения активности ферментов в биологических жидкостях и тканях (главным образом в мозге) происходит накопление ДА. Именно этот процесс обусловливает развитие основных клинических признаков СО. Уровень ДА в крови четко коррелирует с клинической тяжестью СО: превышение его исходных показателей в два раза сочетается с картиной тяжелого СО, при превышении в три раза, как правило, развивается острое психотическое состояние [1]. При развитии СО уровень ДА повышается независимо от принадлежности ПАВ, вызвавшего зависимость, к той или иной химической группе. Поэтому основная мишень терапевтического воздействия при всех типах зависимости от ПАВ - регуляция и нормализация функций мезолимбической дофаминовой системы мозга.
, контролирующей превращение дофамина (ДА) в норадреналин (НА). Происходит формирование ускоренного кругооборота КА. При прекращении приема ПАВ усиленное высвобождение КА из депо прекращается, но остается ускоренным их синтез. Вследствие изменения активности ферментов в биологических жидкостях и тканях (главным образом в мозге) происходит накопление ДА. Именно этот процесс обусловливает развитие основных клинических признаков СО. Уровень ДА в крови четко коррелирует с клинической тяжестью СО: превышение его исходных показателей в два раза сочетается с картиной тяжелого СО, при превышении в три раза, как правило, развивается острое психотическое состояние [1]. При развитии СО уровень ДА повышается независимо от принадлежности ПАВ, вызвавшего зависимость, к той или иной химической группе. Поэтому основная мишень терапевтического воздействия при всех типах зависимости от ПАВ - регуляция и нормализация функций мезолимбической дофаминовой системы мозга.
При СЗ от каннабиноидов основная роль принадлежит каннабиноидным рецепторам (5 система, см. информацию выше), которые распределены неодинаково в разных участках мозга. Большинство из них расположено в базальных ядрах, гиппокампе и коре головного мозга. В целом, до настоящего времени роль каннабиноидной системы выяснена недостаточно, но предполагается что она играет роль в познании, запоминании, воспроизведении, восприятии и моторной координации.
Патогенез СЗ от седативно-снотворных средств близок к патогенезу алкогольной зависимости и также связан с влиянием на системы 1 - 4 (см. информацию выше).
Патогенез СЗ от галлюциногенов открыт с 1950-х годов, связан с нарушением серотонинергической передачи. Галлюциногены имеют структуру, сходную с серотонином (5-HT). Выраженность галлюциногенного действия коррелирует со степенью сродства к постсинаптическому 5-HT2-рецептору. Галлюциногены способны угнетать спонтанную активность самих серотонинергических нейронов. За счет этого уровень нейромедиатора в центральной нервной системе (ЦНС) не только не понижается, но, напротив, существенно возрастает. В результате происходит смещение баланса процессов торможения и возбуждения внутри самой серотонинергической системы.
Механизм действия ингалянтов, а, соответственно, и звенья патогенеза СЗ от ингалянтов до конца пока еще неясен. Имеются указания на схожесть действия отдельных ингалянтов с эффектом этанола. Они основаны на стимуляции ГАМК [5] и глицин-a1 рецепторов, а также на ингибировании N-метил-D-аспартат рецепторов, приводящих к подавлению ЦНС [6].
С клинической точки зрения каждый рецептор можно рассматривать как мишень воздействия только одного нейротрансмиттера. Следовательно, дифференциальная диагностика синдрома отмены строится на понимании роли каждого нейротрансмиттера (Приложение З).
1.3. Эпидемиология
Представление о распространенности СО можно составить, исходя из общей распространенности наркологических заболеваний, так как СО является облигатной, неотъемлемой частью СЗ. Считается, что развитие СО является наиболее частой причиной обращения за специализированной медицинской помощью, однако следует отметить, что точечные эпидемиологические данные отсутствуют.
Алкоголь, конечно, остается наиболее употребляемым ПАВ в мире, его потребление занимает особое место в перечне ведущих факторов риска популяционного здоровья человечества [7, 8].
Из незаконных наркотиков самым распространенным в мире по-прежнему остается каннабис. Потребление каннабиса растет и продолжает оставаться на высоком уровне в Западной и Центральной Африке, Западной и Центральной Европе, и Океании, а также в Северной Америке [9]. Кроме того, различные страны сообщают о продолжающемся росте как количества, так и многообразия синтетических каннабиноидов. В ежегодном докладе по наркотикам УНП ООН (Управление по наркотикам и преступности Организации Объединенных Наций) 2013 года сообщалось, что на долю синтетических каннабиноидов среди всех новых ПАВ приходилось 23%. По состоянию на декабрь 2014 года информационная система раннего предупреждения УНП ООН получила от 95 стран и территорий сообщения о 541 новых ПАВ, доля синтетических каннабиноидов в структуре новых ПАВ составляла уже 39% [9, 10]. В 2016 году каннабис также оставался самым распространенным наркотиком. Согласно данным УНП ООН, число людей, употребляющих каннабис, продолжает расти: за период 2006 - 2016 оно выросло на  , что соответствует приросту мирового населения за тот же период [11].
, что соответствует приросту мирового населения за тот же период [11].
Кокаин и амфетамины являются вторыми после каннабиноидов в мире [10, 12, 13]. Наиболее распространено употребление амфетаминов в Америке, странах Океании, растет число пользователей амфетаминов, метамфетаминов в станах Азии, в Западной и Центральной Европе и Латинской Америке наблюдается рост потребителей "экстази" [11].
На третьем месте по частоте употребления находятся опиоиды [12], однако тяжесть последствий их употребления сложно переоценить. Так, например, в доле смертей, связанных с употреблением наркотиков, на опиоиды приходится 76% [11]. Средняя распространенность употребления опиоидов с высоким уровнем риска среди взрослых от 15 до 64 лет в Европе в 2014 году оценивалась на уровне 0,4%, что эквивалентно 1,3 миллионам употребляющих опиоиды с высоким уровнем риска [12].
По числу обращений за медицинской помощью по поводу злоупотребления ПАВ, лица с зависимостью от ингалянтов находятся на четвертом месте. В настоящее время в мире с той или иной частотой потребляют наркотические средства 13,1% детей, подростков и молодежи в возрасте 11 - 24 года. Это примерно 4 миллиона человек. Ингалянты хотя бы один раз пробовали 9% учащихся 15 - 16 лет [14].
В настоящее время злоупотребление барбитуратами распространено не широко. Более частое употребление седативно-снотворных препаратов сейчас регистрируется в среде пациентов, участвующих в программах заместительной опиоидной терапии. Например, во Франции злоупотребляют бензодиазепинами 45% пациентов, в Германии - до 70%. Частота злоупотребления бензодиазепинами увеличивается с продолжительностью заместительного лечения. Высокие цифры злоупотребления седативно-снотворными средствами отмечаются среди потребителей опиоидов в тюрьмах. Так, в 2014 году, в 38 итальянских тюрьмах было обнаружено, что 85% потребителей опиоидов злоупотребляли бензодиазепинами. Ирландия, Финляндия и Румыния являются странами, не более 5% пациентов в 2014 году сообщили о применение седативно-снотворных средств в качестве основного наркотика. Данная тенденция сохраняется и в настоящее время [11]. До недавнего времени в США и ряде других стран прием таблеток барбитуратов в повышенных дозах был одним из самых распространенных способов самоубийства [15, 16, 17].
Распространенность зависимости от галлюциногенов невелика. Развивается, благодаря психоделическому движению в современной культуре. Психологическая привлекательность употребления галлюциногенов заключается в том, что в состоянии интоксикации у человека обостряется восприятие мира, возникают необычные, ранее не испытанные чувства, оживляются воспоминания далекого прошлого, нередко происходит отреагирование прежних психических травм. Эпидемиологические исследования последних лет показали, что употребляют галлюциногены не реже 2 - 3 раз в неделю (что может служить косвенным признаком сформированного синдрома зависимости) 5,6% подростков и молодежи [14].
В России в отношении распространенности наркоманий наблюдаются следующие тенденции [18, 19]. В 2015 г. специализированными наркологическими учреждениями зарегистрировано 311 785 человек (213,2 на 100 тыс. населения), а в 2016 г. - 292 407 человек (199,5 на 100 тыс. населения), то есть данный показатель снизился на 6%. Среди зарегистрированных пациентов с синдромом зависимости от наркотиков большинство составили лица с опиоидной зависимостью (2015 г. - 74,0%; 2016 г. - 69,6%). Второе ранговое место заняла группа пациентов с полинаркоманией и зависимых от других наркотиков (галлюциногены, седативно-снотворные средства, летучие растворители): 2015 г. - 12,9%, 2016 г. - 15,8%. Больные с зависимостью от каннабиса заняли третье ранговое место: 2015 г. - 9,0%, 2016 г. - 9,6%. На четвертом месте - группа пациентов с зависимостью от психостимуляторов (амфетамины, кокаин и т.п.): 2015 г. - 4,1%, 2016 г. - 4,9% [18, 19].
Поскольку кофеин часто употребляется у населения во всех возрастных, социальных и гендерных группах, <1> синдром отмены кофеина рассмотрен отдельно. Источником кофеина являются различные пищевые продукты, <2> медикаментозные средства, <3> биологически активные добавки. Эпидемиологические данные по распространенности кофеиновой токсикомании отсутствуют, хотя в имеющихся литературных источниках она оценивается, как низкая [20].
1.4. Кодирование по МКБ-10
В Международной классификации болезней 10 пересмотра (МКБ-10) <4> синдром отмены от различных видов ПАВ (алкоголь, опиоиды, каннабиноиды, седативные и снотворные средства, кокаин, другие психостимуляторы, включая кофеин, галлюциногены, никотин, ингалянты) рассматривается в одном разделе: F1x.3. Уточнение вида употребляемого ПАВ проводится по третьему знаку, а абстинентного состояния (синдрома отмены) - по четвертому, при этом наличие диагностических критериев для постановки диагноза обязательно (Таблица 1).
Таблица 1 - Формализация диагноза по МКБ-10.
|
Код
|
Соответствие коду
|
|
F11.3
|
Синдром отмены опиоидов
|
|
F12.3
|
Синдром отмены каннабиноидов
|
|
F13.3
|
Синдром отмены седативных или снотворных веществ (F13.3-T; F13.3-H)
|
|
F14.3
|
Синдром отмены кокаина
|
|
F15.3
|
Синдром отмены других стимуляторов, включая кофеин (F15.3-T; F15.3-H)
|
|
F16.3
|
Синдром отмены галлюциногенов (F16.3-T; F16.3-H)
|
|
F18.3
|
Синдром отмены летучих растворителей (F18.3-T; F18.3-H)
|
|
F19.3
|
Синдром отмены при одновременном употреблении нескольких наркотических средств и использовании других психоактивных веществ (F19.3-T; F19.3-H)
|
1.5. Классификация
Формулировка диагноза по МКБ-10 имеет большое значение в юридическом (ограничение видов деятельности в связи учетом в наркологическом диспансере (НД)), статистическом и клиническом аспектах.
СО является частью СЗ (F1x.2) и кодируется самостоятельно в том случае, когда состояние отмены является непосредственной причиной обращения к врачу-специалисту в случае выраженной тяжести расстройств.
СО входит в структуру СЗ, и этот последний диагноз также надо устанавливать.
В случае употребления больным более чем одного ПАВ диагноз устанавливается по веществу (или классу веществ), которое употреблялось наиболее часто.
В случае хаотичного приема ПАВ, когда последствия употребления клинически не разделимы, применяется код F19.
Как особая рубрика в МКБ-10 выделен СО, осложненный судорожными припадками. Судорожные припадки возникают, главным образом, у лиц, страдающих зависимостью от ПАВ, которые обладают противосудорожными свойствами. К таким веществам относят барбитураты, бензодиазепины и, в меньшей степени, алкоголь.
Диагноз "Наркомания" устанавливается только в том случае, если ПАВ включено в "Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации (Список 1, 2, 3)" <5>. То есть, в случаях зависимости от седативных или снотворных веществ (F13), стимуляторов (F15), галлюциногенов (F16), летучих растворителей (F18), употребления нескольких седативных веществ (F19), в коде психические расстройства ставится русская буква "Н". В противном случае расстройство квалифицируется как "токсикомания" и обозначается русской буквой "Т"; данные буквы устанавливаются в конце шифра.
1.6. Клиническая картина
Клиническая картина СО включает в себя три составляющие:
1) токсикогенную симптоматику, она мало специфична. Проявления СО диаметрально противоположны прямому фармакологическому эффекту потребляемого вещества. Эти расстройства по сравнению с собственно токсикогенной симптоматикой более нозологически специфичны, так как они говорят о длительном злоупотреблении ПАВ и отражают их неодинаковые фармакологические свойства. Связаны эти проявления с нарушенным гомеостазом организма в условиях хронической интоксикации;
2) собственно адциктивную симптоматику, которая является нозологически специфичной и включает проявления патологического влечения к ПАВ - аффективные и поведенческие расстройства;
3) признаки обострения разнообразной латентной патологии - органической недостаточности головного мозга, функциональной слабости печени и др., - которая связана как с сопутствующими заболеваниями, так и с накопившимися соматическими последствиями хронической интоксикации ПАВ (Таблица 2) [1].
Таблица 2 - Составляющие клинической картины абстинентного синдрома
|
Категория
|
Описание
|
|
Токсикогенная симптоматика синдрома отмены
|
Определяет индивидуальные различия синдрома отмены, связанные как с типом ПАВ, являющегося предметом зависимости, так и с этапом развития заболевания. Ее проявления:
- постинтоксикационная симптоматика: головная боль, разбитость, слабость, чувство внутреннего дискомфорта;
- симптоматика, связанная со сформированными в ответ на систематически повторяющуюся интоксикацию механизмами восстановления нарушенного гомеостаза. В этих условиях прекращение приема ПАВ вновь нарушает баланс, что приводит к развитию нарушений, диаметрально противоположных прямому фармакологическому эффекту потребляемого вещества.
|
|
Аддиктивная симптоматика синдрома отмены
|
Отражает общность всех клинических вариантов синдрома отмены. В отличие от токсикогенной симптоматики, имеет нозологически специфичный характер, свойственный только болезни зависимости, что дает возможность дифференцировать абстинентное состояние от других патологических состояний с похожими симптомами. Среди этих признаков:
- разнообразные аффективные нарушения, имеющие смешанный характер и отличающиеся атипией синдромальной структуры;
- психопатоподобное поведение (отказ от соблюдения режима или лечения, капризы, назойливость и конфликтность, стремление тайно раздобыть ПАВ, оппозиционность к медицинскому персоналу, истерические реакции и требования дополнительного назначения снотворных и успокоительных средств).
|
|
Признаки обострения скрытой патологии
|
Связаны как с наличием сопутствующих заболеваний, так и с накопившимися соматическими последствиями хронической интоксикации ПАВ. СО обычно тем тяжелее, чем старше пациент и чем больше общая продолжительность хронической интоксикации. Учитывать эту патологию необходимо при планировании дифференцированной терапии СО.
|
Примечание: ПАВ - психоактивное вещество; СО - абстинентный синдром.
2. Диагностика
2.1. Жалобы и анамнез
- Рекомендуется при выяснении жалоб и сборе анамнеза обращать внимание на ниже перечисленные диагностические критерии СО <6> [1, 21].
1. Прекращение длительного умеренного или сильного употребления ПАВ (в течение нескольких недель и дольше), снижение потребляемого количества, либо введение специфического антагониста (если таковой имеется) в период употребления ПАВ или вслед за прекращением их употребления, за которым наблюдается определенная клиническая картина (см. информацию ниже).
2. Отсутствие связи с каким-либо соматическим или другим психическим расстройством.
3. Облегчение после приема данного вида ПАВ, либо вещества, имеющего с ним перекрестную толерантность.
Уровень GPP.
2.1.1. Клинические признаки опийного абстинентного синдрома (F11.3)
- Рекомендуется диагностировать не менее трех из клинических проявлений синдрома отмены опиоидов [1, 21]:
- страстное желание принять наркотик;
- тошнота или рвота;
- боли в мышцах;
- слезотечение или риноррея (насморк);
- расширение зрачка, пилоэрекция, потливость;
- диарея;
- зевота;
- лихорадка;
- бессонница.
Уровень GPP.
Комментарии: При синдроме зависимости от опиоидов формирование СО (а, соответственно, и 2-й стадии зависимости) как правило, происходит стремительно: эпизодическое употребление может исчерпываться 2 - 3 пробами, а уже через 2 - 4 недели систематического употребления появляются первые признаки СО.
СО опиоидов ("ломка") развивается через 6 - 24 ч после последнего употребления наркотика. Время развития СО зависит от вида опиоидов (так, например, при употреблении уличного, либо медицинского метадона, появление СО отсрочено на 7 - 10 дней), либо от примесей, входящих в наркотик (бензодиазепины, антигистаминные препараты также удлиняют время появления первых признаков СО, могут пролонгировать его длительность). Тяжесть проявлений СО зависит от наркогенности опиоида, считается, что наибольшей наркогенностью обладает героин и уличный метадон, наименьшей - опий-сырец. Клинические проявления СО складываются из психопатологических и сомато-вегетативных нарушений, в структуре последних относительно специфическим характером обладает болевой синдром (Приложение Г, Д).
Пациенты в состоянии отмены опиоидов, как правило, не скрывают осознанное, часто непреодолимое влечение к наркотику. Нередко они неуправляемы, агрессивны, в абстинентном состоянии совершается наибольшее число правонарушений, возрастает опасность суицида.
Тяжело протекает СО у пациентов с длительной, непрерывной формой злоупотребления метадоном, реже героином (более 3 - 4 лет), большой продолжительностью заболевания (более 10 лет), сопутствующими соматическими и неврологическими заболеваниями. При этом у больных резко выражены сомато-вегетативные и болевые расстройства (интенсивные мышечные и суставные боли, гипергидроз, озноб или чувство жара, акатизия, гипертермия, тошнота, рвота, диарея, лабильность АД, частоты сердечных сокращений), психопатологические нарушения (пониженное настроение с дисфорическим оттенком, тревога, чувство страха, двигательное беспокойство, влечение к наркотику, бессонница). Часто наблюдаются водно-электролитные нарушения (гиповолемия, метаболический ацидоз или алкалоз).
Развитие делириозных состояний и судорожного синдрома для СО нехарактерно, если эти осложнения и развиваются, то крайне редко. Как правило, они бывают связаны с определенной коморбидной патологией или сочетанным употреблением других ПАВ.
2.1.2. Клинические признаки синдрома отмены каннабиноидов (F12.3).
- Рекомендуется диагностировать не менее трех из клинических проявлений синдрома отмены каннабиноидов [1, 21]:
- страстное желание употребить каннабиноиды;
- тревога, беспокойство, нервозность;
- дисфория, раздражительность, гнев, агрессия;
- депрессивное настроение;
- нарушения сна (бессонница, тревожные сны);
- отсутствие аппетита или снижение веса;
- по меньшей мере, один из следующих физических симптомов, который вызывает дискомфорт: тремор, потливость, головная боль, озноб/повышение температуры тела.
Уровень GPP.
Комментарии: Формирование СО при систематическом регулярном употреблении каннабиноидов, как правило, занимает длительное время, составляет, в среднем, 2 - 3 года. СО развивается через 4 - 5 часов после курения каннабиса, своего пика абстинентные расстройства достигают на 3 - 5-е сутки, а длительность СО в среднем составляет 7 суток.
На начальном этапе СО представлен преимущественно астеническим симптомокомплексом с явлениями аффективной лабильности, повышенной утомляемости. Отмечаются сонливость и вялость в течение дня с нарушением засыпания в вечерние часы. Вегетативные реакции отличаются разнообразием: головные боли сдавливающего, иногда пульсирующего характера, колющие боли в области сердца, сердцебиение, гипертензия, учащение и лабильность пульса, стойкий красный дермографизм, гипергидроз. Неврологически определяются тремор, оживление сухожильных рефлексов, подергивание отдельных мышечных пучков. Отмечается снижение аппетита. Основными симптомами являются раздражительность, стойкие головные боли, снижение работоспособности. При употреблении каннабиноидов с низким содержанием тетрагидроканнабинола (ТГК) клиника СО ограничивается легкими астеническими расстройствами. При утяжелении и прогрессировании заболевания усложняется и картина СО. Астеническая симптоматика сменяется астенодепрессивной с тяжелыми расстройствами настроения, безразличием, апатией, подавленностью, гнетущей тоской с тягостным чувством сдавления в области сердца, неопределенными ощущениями в животе. Наблюдается упорная бессонница. Мысли о бесперспективности своего будущего, неверие в возможность прекратить прием наркотиков, в успех лечения сопровождаются идеями малоценности и суицидальными высказываниями. Суицидальные попытки чаще демонстративные, но могут быть и истинными. Появление тревоги в картине СО указывает на возможность развития абстинентного психоза. В дальнейшем к астенодепрессивной симптоматике могут присоединяться сенестопатии и парестезии. Превалируют жалобы на неприятные, тягостные ощущения онемения и похолодания конечностей, чувство сдавления в груди, спазмы в животе. На коже в различных участках тела возникают покалывание, жжение, чувство ползания мурашек. Все это сопровождается зудом ("чески") с преимущественной локализацией в конечностях и волосистой части головы (Приложение Г, Д). На этапе полностью сформированного СО для больных становится характерной дисфорическая симптоматика: раздражение, злоба, агрессия.
2.1.3. Клинические признаки синдрома отмены седативных или снотворных средств (F13.3).
- Рекомендуется диагностировать не менее двух из клинических проявлений синдрома отмены седативных или снотворных средств [1, 21]:
- страстное желание употребить седативные или снотворные средства;
- гиперактивность вегетативной нервной системы (ВНС): потливость, тахикардия более 100 уд/мин, ортостатическая гипотония, головная боль, др.
- тремор пальцев вытянутых рук, языка или век;
- тошнота, рвота;
- психомоторное возбуждение;
- транзиторные зрительные, осязательные или слуховые галлюцинации либо иллюзии;
- бессонница;
- тревога;
- большой судорожный припадок.
Уровень GPP
Комментарии: СО при зависимости от седативных или снотворных средств характеризуется быстрым развитием. Средний срок - полгода от формирования систематического приема. Сроки наступления СО и его длительность зависят от периода полувыведения принимаемого лекарственного препарата. Более наркогенными являются препараты, относящиеся к группе производных барбитуровой кислоты.
Учитывая возможность эпилептических припадков и психозов, склонность к суицидам, СО при употреблении седативных или снотворных средств является состоянием, опасным для жизни больного.
СО барбитуратов имеет фазное течение с закономерным нарастанием симптоматики, достижения ее пика на 3 - 4 сутки и возможным развитием осложнений на 3 - 8 сутки отказа от ПАВ в виде больших судорожных припадков или психозов. Абстинентные барбитуровые психозы чаще всего представлены делирием, который по клиническим проявлениям сходен с алкогольным. В отличие от последнего, отмечается большая выраженность тревоги, напряженности, злобности, больший удельный вес слуховых галлюцинаций, наличие мышечных галлюцинаций. Яркие зрительные фантастические галлюцинации встречаются редко. Продолжительность барбитурового психоза - от 2 - 3 суток до 2 недель. Галлюцинаторно-бредовые психозы встречаются редко. Длительность СО вследствие употребления барбитуратов может составлять, в среднем, 4 недели. В случае, если психотическая симптоматика не развивается, то перелом в течении СО можно наблюдать к 10 - 14 дню, когда у пациента появляется аппетит.
Между СО барбитуратов и СО бензодиазепинов есть сходство по структурно-динамическим особенностям. Отличия заключаются в выраженности симптоматики и ее длительности (приложение Г, Д). Риск развития СО бензодиазепинов резко увеличивается при длительном (свыше 6 мес.) их приеме или приеме чрезмерно высоких доз. В ряде случаев, как и при СО барбитуратов, развиваются судорожные припадки или острый психоз. Длительность СО - 2 - 3 недели. Такие проявления, как выраженное влечение к приему ПАВ, неустойчивость эмоционального фона, утомляемость, нарушенный ритм сна, бессонница, могут длиться до 1 - 2 месяца.
Если снотворные или седативные препараты принимались в терапевтических дозах, но длительное время, то СО будет иметь свои особенности, которые заключаются в том, что не развиваются судорожные припадки и психозы. Считается, что СО формируется, если прием препаратов превышает 4 - 6 месяцев. При превышении терапевтических доз СО может манифестировать раньше.
2.1.4. Клинические признаки синдрома отмены кокаина, других психостимуляторов, включая кофеин (F14.3, F15.3).
- Рекомендуется диагностировать не менее трех клинических проявлений синдрома отмены кокаина, других психостимуляторов, включая кофеин [1, 21]:
- страстное желание употребить кокаин, другие психостимуляторы, включая кофеин;
- стойкая дисфория (наиболее постоянный и диагностически значимый признак);
- ангедоническая депрессия с витальной симптоматикой;
- бессонница или сонливость;
- суицидальные мысли;
- идеи отношения и преследования;
- повышенный аппетит;
- яркие, неприятные, кошмарные сновидения;
- психомоторная ажитация или заторможенность.
Уровень GPP.
Комментарии: Проявления СО при сформированной зависимости от кокаина не резко выражены. СО возникает через 24 ч после последнего употребления наркотика, максимальной выраженности расстройства достигают на 3 - 4-е сутки. Острые проявления исчезают в течение 10 - 14 дней, в тяжелых случаях симптомы сохраняются до 1 мес.
Клиника СО представлена преимущественно депрессивно-дисфорическими расстройствами в сочетании с бессонницей или сонливостью, повышением аппетита, психомоторным возбуждением или, реже, заторможенностью. На этом фоне иногда возникают отдельные идеи отношения и преследования, а также суицидальные мысли. Больные отчетливо ощущают неполноценность собственного существования, безысходность, испытывают чувство внутренней пустоты, безрадостность. При этом влечение к наркотику имеет ясное психопатологическое оформление в виде стойкой ангедонической депрессии, нередко принимает непреодолимый характер, что приводит к рецидиву. Особенностью кокаинового СО является чередование периодов послабления и усиления симптоматики. В период послабления улучшается сон, тяга к кокаину ослабевает. Такое состояние сменяется новым приступом дисфории, тревожности, раздражительности и интенсивной потребности в кокаине (приложение Г, Д).
СО амфетаминов возникает через 12 - 24 часа после их последнего употребления амфетаминов, максимальной выраженности расстройства достигают на 2 - 4 сутки. Характерный признак СО психостимуляторов - глубокие депрессивные расстройства. Могут отмечаться отдельные идеи отношения, преследования. Возможны эксплозивные реакции, приступы паники, страха, дисфория, подозрительность, сильное влечение к наркотику. На высоте абстинентных расстройств может развиться психоз по типу делирия или острого параноида с речевым и двигательным возбуждением, встречаются хронические амфетаминовые психозы, продолжающиеся от 2 - 3 недель до нескольких месяцев.
Неврологически СО психостимуляторов проявляется нарушением координации движений, фибриллярными подергиваниями отдельных мышечных групп лица и языка, миозом, слабой реакцией зрачков на свет, нистагмом. Мышечный тонус снижен. Сухожильные рефлексы повышены.
Длительность СО психостимуляторов составляет 7 - 14 дней, но в тяжелых случаях проявления сохраняются до 1 месяца. Наиболее тяжело протекает отмена производных эфедрина (эфедрон, первитин) в связи с его высокой наркогенностью.
Синдром отмены кофеина - редкое явление в клинике наркологических заболеваний. Систематическое употребление кофеина в повышенных дозах (значительно превышающих 250 мг/сутки [21]) способствует формированию кофеиновой токсикомании. Высокими дозами кофеина считаются 5 - 10 г/сутки [21].
Наиболее часто встречается данная патология у лиц, отбывающих наказание в местах тюремного заключения, которые употребляют в виде чифира - напитка, приготовленного путем длительного кипячения больших количеств чая - 100 - 150 г в небольшом количестве воды - 200 - 300 мл (в этом случае дозы кофеина приближаются к летальным, 10 - 14 г/сутки). Справедливости ради стоит отметить, что, как правило, к употреблению чифира прибегают индивидуумы с уже сформированным СЗ (алкоголизм, наркомания).
По данным EFSA (European Food Safety Authority, Европейское Агентство по безопасности продуктов)), FDA (Food and Drug Administration, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов), Министерства здравоохранения Российской Федерации, считается безопасным в целом для здоровой популяции взрослых разовое потребление кофеина до 200 мг в день, регулярное потребление кофеина в дозах до 400 мг/день. Для подростков применимы такие же ограничения, как и для популяции взрослых. Для беременных и кормящих грудью матерей безопасным считается употребление кофеина до 200 мг разово или регулярно в течение дня. Эти привычные дозы употребления кофеина определяют концепцию минимально переносимого потребления (МПП) [20, 22]. Следует учитывать, однако, что существуют большие индивидуальные различия в переносимости и действии кофеина на организм человека.
Развитие СО напрямую зависит от периода полураспада кофеина в организме, который составляет 4 - 6 часов. Спустя данный период времени появляются головные боли, бессонница, кошмарные сновидения. У некоторых больных наблюдаются судорожные подергивания икроножных мышц, дрожание языка, пальцев, нарушения ритма сердечной деятельности, сопровождающиеся тревогой, страхом. Отличительным признаком СО кофеина является головная боль пульсирующего характера, усиливающаяся при двигательной, речевой, даже мимической активности. Определение уровня кофеина в крови может дать важную информацию для постановки диагноза, хотя изолированно не могут являться критерием диагноза с учетом широкого разброса индивидуальной переносимости кофеина.
2.1.5. Клинические признаки синдрома отмены галлюциногенов (F16.3).
Для синдрома зависимости от галлюциногенов СО нехарактерен. Проявления нечеткие, мало дифференцированные, неспецифичные. В DSM-5 (Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition, Диагностическая и статистическая классификация психических болезней, пятый пересмотр) абстинентный синдром, вызванный употреблением галлюциногенов, не рассматривается [21].
- Рекомендуется определять вид употребляемого галлюциногена [1, 21].
Уровень GPP
Комментарии: При хронической интоксикации диссоциативными анестетиками (фенциклидин, "ангельская пыль", кетамин, некоторые другие) серотонинергическими галлюциногенами (ЛСД, псилоцибин, сальвинорин и некоторые другие) и метиловыми амфетаминами (MDA, MDMA и некоторые другие) на первые-вторые сутки лишения возникает умеренная вегетативная дисфункция, соматический дискомфорт в виде ноющих неинтенсивных болевых ощущений без четкой локализации, а также депрессивно-астеническая симптоматика. Длительность данных расстройств также сравнительно небольшая - до 10 - 14 дней. Учитывая малую специфичность симптоматики, СО не описывается.
При употреблении антихолинергических галлюциногенов (скополамин, атропин, циклодол, др.) СО формируется спустя 1 - 1,5 года их систематического употребления в высоких дозах. Развивается, в среднем, через сутки после прекращения приема. Проявляется психопатологическими, неврологическими и соматовегетативными нарушениями. Психопатологические расстройства на начальном этапе представлены астено-депрессивной симптоматикой, которая в динамике СО нарастает. На пике развития симптоматики присоединяется выраженная дисфория, раздражительность, злобность.
Неврологические и вегетативные расстройства проявляются в общем треморе всего тела, повышенном тонусе скелетной мускулатуры, нарастающей скованности движений. Характерны болезненные ощущения в мышцах спины, судорожные подергивания отдельных мышечных групп, непроизвольные движения конечностей, маскообразное лицо. Абстинентные явления продолжаются от 1 до 2 недель, обратное развитие симптоматики также происходит через астено-депрессивный симптомокомплекс. Тремор, мышечная гипертензия, повышенные сухожильные рефлексы могут сохраняться в течение 1,5 - 2 месяцев. Нередко развитие осложнений (эпилептиформных припадков, делирия), особенно при наличии врожденной или приобретенной органической неполноценности головного мозга.
2.1.6. Клинические признаки синдрома отмены летучих растворителей (F18.3).
- Рекомендуется диагностировать не менее четырех клинических проявлений синдрома отмены летучих растворителей [1, 21]:
- дисфория, раздражительность, гнев;
- трудности с концентрацией внимания;
- повышенный аппетит;
- тревога;
- неусидчивость;
- сниженное настроение;
- бессонница.
Уровень GPP.
Комментарии: СО формируется через 6 - 12 мес. систематического употребления летучих растворителей (ингалянтов). Учитывая возрастной фактор (употребление ингалянтов свойственно детям и подросткам), его проявления нередко принимаются за вегетососудистую дистонию. Несмотря на то, что абстинентные расстройства слабо выражены, маскированы под возрастную дисфункциональность ВНС, тем не менее, абстинентная природа состояния подтверждается выраженным влечением к ингалянтам, моментальным восстановлением психофизического благополучия при его приеме.
Ведущее место в структуре СО отводится аффективным и поведенческим расстройствам с дисфорией, раздражительностью, депрессивными и ипохондрическими проявлениями. Вегетативные же нарушения с полиморфной симптоматикой представлены менее ярко.
Динамика развития СО следующая. Спустя сутки после последнего приема на первый план выступают психические расстройства: подавленность, раздражительность, нарушения сна. Снижается аппетит, появляется жажда, больные испытывают отвращение к курению, беспокоит тупая, диффузная головная боль. На 2 - 3-и сутки к этому присоединяются неприятные ощущения в различных частях тела, особенно в грудной клетке, першение в горле, затрудненность вдоха, чувство нехватки воздуха. Появляются жалобы на тошноту, боль в эпигастрии и правой подвздошной области, иногда рвоту. Может быть жидкий стул с частотой 3 - 6 раз в сутки. Могут иметь место гипергидроз, колебания артериального давления (АД), тахикардия, сердечная аритмия. Из неврологических нарушений присутствуют грубо размашистый тремор пальцев рук, дрожание век. В ночное время возникают мышечная боль и судорожные подергивания в мышцах нижних конечностей. Усиливается раздражительность, появляется злобность, частыми становятся дисфорические вспышки. На 5 - 7-е сутки напряжение сменяется астенодепрессивной симптоматикой. Соматические расстройства купируются к концу первой, психические - к началу третьей недели воздержания (приложение Г, Д). СО в тяжелых случаях может осложниться развитием острого делирия, длящегося от нескольких часов до 3-х суток и протекающего с иллюзиями, истинными зрительными и слуховыми галлюцинациями. В среднем, продолжительность синдрома отмены составляет около 2-х недель.
В DSM-5 абстинентный синдром, вызванный употреблением ингалянтов, не рассматривается в связи с его сравнительно нетяжелым течением и редкой встречаемостью (10%) [21].
2.2. Физикальное обследование
Несмотря на то, что данные физикального обследования не являются специфическими при СО ПАВ, тем не менее, тщательное медицинское обследование является подтверждающим дополнением к клинической диагностике, а также позволяет создать ориентиры в определении тяжести состояния. Например, при СО опиоидов у больного выявляются следы от внутривенных инъекций по ходу поверхностных вен, слезотечение, повышение АД, учащение частоты сердечных сокращений (ЧСС) увеличение размеров печени, что в совокупности является свидетельством хронической интоксикации, и т.д. Может изменяться частота дыхательных движений (ЧДД) и пр.
Дифференциально-диагностические критерии СО по реакции зрачка представлены в Приложении Д.
- Рекомендуется обследование соматического состояния пациента: определение состояния кожных покровов, инъецированности склер, мышечного тонуса, пальпация/перкуссия печени, почек, аускультация сердца, измерение АД, ЧСС, ЧДД [1, 23, 24, 25, 26, 27].
Уровень GPP.
- Рекомендуется обследование неврологического состояния пациента: определение реакции зрачков, нистагма, тремора, состояния периферической нервной системы (тактильная и болевая чувствительность), статической и динамической координации [1, 23, 24, 25, 26, 27].
Уровень GPP.
2.3. Лабораторная диагностика
При установлении диагноза СО наиболее важна клиническая диагностика. Лабораторные методы диагностики, такие как иммунно-ферментный анализ (ИФА), газовая хроматография (ГХ), масс-спектрометрия (МС) или высокоэффективная жидкостная хроматография (ВЭЖХ) отражают факт потребления ПАВ, но не позволяют установить диагноз "Синдром зависимости" или "Синдром отмены". С другой стороны, являются важным объективным показателем в дополнение к классической клинической диагностике.
Необходимость в лабораторной диагностике возникает в случаях затруднения определения ПАВ по клинической картине, при проведении дифференциального диагноза, для подтверждения состояния хронической интоксикации ПАВ, либо в рамках медицинского освидетельствования <7>.
В лабораторной диагностике употребления ПАВ используют два основных типа тестирования: иммунологический (такой, как ИФА) и хроматография (такие как ГХ, МС или ВЭЖХ).
- Рекомендуется проведение ИФА при первичном скрининге мочи на содержание ПАВ [28, 29, 30, 31, 32].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
Комментарии: Точность тестирования ИФА варьирует, наиболее высокая она для каннабиса и кокаина, более низкая - для опиоидов и психостимуляторов. Положительные результаты ИФА должны сопровождаться подтверждающим тестированием с использованием ГХ/МС или ВЭЖХ. Каждое ПАВ имеет свою длительность выявления в моче методом ИФА (Таблица 3) [30, 31, 32].
Таблица 3 - Выявление психоактивных веществ при проведении иммунно-ферментного анализа
|
ПАВ
|
Длительность выявления ПАВ при ИФА
|
|
Амфетамины
|
2 - 3 дня
|
|
Фенциклидин
|
7 - 14 дней
|
|
Каннабиноиды
|
Зависит от характера употребления:
Единичное употребление - 3 дня
Эпизодичность употребления до 3 - 4 раз в неделю - 5 - 7 дней
Систематическое употребление - 10 - 15 дней
|
|
Бензодиазепины
|
Короткого действия - 3 дня
Длительного действия - до 30 дней
|
|
Кокаин
|
Зависит от тяжести зависимости:
2 - 3 дня при эпизодическом употреблении
8 дней - при систематическом употреблении
|
|
Опиоиды
|
2 - 3 дня
|
Примечание: ПАВ - психоактивное вещество; ИФА - иммунно-ферментный анализ.
- Рекомендуется подтверждение с помощью ГХ/МС или ВЭЖХ при положительных результатах ИФА [28, 29, 30, 31, 32].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
Комментарии: ИФА используют в качестве первичного скрининга в связи с простотой их использования и малой затратностью, хроматографию - в сложных диагностических случаях, для подтверждения результатов ИФА и для получения высокоточных результатов. Методы хроматографии являются высокоточными, но более дорогостоящими, сложными для выполнения и затратными по времени.
В зарубежной практике, в связи с тем, что распространено употребление большого количества различных полусинтетических и синтетических производных морфина, для определения опиоидов используют расширенную панель, включающую не только основные метаболиты морфина, но и такие часто используемые ПАВ и ЛС, как фентанил, гидрокодон, метадон, оксикодон, бупренорфин, трамадол** [28, 29, 30, 31, 32]. Для России расширение диагностической панели является актуальным лишь в отношении трамадола**.
Для установления факта систематического употребления наркотических средств и психотропных веществ возможно проведение химико-токсикологических исследований волос и ногтей. Основные группы наркотических средств и психотропных веществ могут обнаруживаться в волосах методом тандемной хромато-масс-спектрометрии при регулярном потреблении ПАВ на протяжении нескольких месяцев. При разовом или эпизодическом употреблении ПАВ в волосах могут быть не обнаружены. Для выявления факта систематического употребления наркотических средств и психотропных веществ существуют методы иммуноферментного анализа антител к ПАВ. Но подчеркнем, что наличие положительного результата не является достаточным для установления диагноза.
- Рекомендуется выполнить анализ крови биохимический общетерапевтический, общий (клинический) анализ крови развернутый, анализ мочи общий до начала лечения для оценки безопасности лечения [1, 23, 24, 25, 26, 27]
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Выполнение данных анализов важно как для оценки безопасности проводимой терапии, так и для определения статуса общего соматического здоровья, чтобы иметь возможность исключить острые состояния, требующие оказания специализированной медицинской помощи в первую очередь. Как правило, выполнение рутинных лабораторных анализов проводится до начала назначения терапии.
2.4. Инструментальная диагностика
Возможности использования инструментальной диагностики при СО ограничены, так как отсутствуют специфические физикальные и лабораторные признаки, характерные для СО. Инструментальные методы проводятся по клиническим показаниям.
- Рекомендуется исследование ЭКГ с расшифровкой, описанием и интерпретацией данных до начала лечения для оценки безопасности лечения [1, 27].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Хроническая интоксикация ПАВ пагубно влияет на ЦНС, сопряжена с развитием множества сопутствующих заболеваний соматической сферы, поэтому может быть полезным проведение следующих исследований: электрокардиограмма (ЭКГ), ультразвуковое исследование внутренних органов (УЗИ), электроэнцефалография (ЭЭГ), эхоэнцефалография (Эхо-ЭГ), рентгенография (Rg) черепа, легких и др.
- Рекомендуется определение степени тяжести СО с учетом физикального, инструментального и клинического обследования [1, 23, 24, 25, 27].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Определение степени тяжести СО дает возможность принять взвешенные и рациональные решения в отношении не только условий оказания медицинской помощи, но и терапевтических мероприятий. Ориентировочные клинические критерии степени тяжести СО представлены в Таблице 4.
Таблица 4 - Степень тяжести синдрома отмены от различных ПАВ в зависимости от клинических проявлений
|
Степень тяжести
|
Клинические проявления
|
|
Легкая
|
Вегетативные расстройства: в зависимости от фармакологии ПАВ, могут диагностироваться потливость, головная боль, тошнота, жажда, боль, заложенность носа, риноррея и др.
Соматические расстройства: ЧСС до 100 уд/мин; АД диастолическое до 100 мм рт ст; t °C - до 37 °C. Неврологические расстройства: невыраженный тремор.
Психические расстройства: невыраженное (слабое) влечение к ПАВ.
|
|
Средняя
|
Вегетативные расстройства: потливость, озноб, головная боль, болевые ощущения, тошнота, рвота, тахикардия, тахиаритмия.
Соматические расстройства: ЧСС 100 - 120 уд/мин; АД диастолическое 100 - 110 мм рт ст; t °C - до 38 °C. Неврологические расстройства: тремор, атаксия.
Психические расстройства бессонница, тревога, психомоторное возбуждение, влечение к ПАВ.
|
|
Тяжелая
|
Вегетативные расстройства: гипергидроз, озноб, тошнота, рвота, боли различной локализации, тахикардия, тахиаритмия, аритмия, иные расстройства сердечной деятельности.
Соматические расстройства: ЧСС более 120 уд/мин; АД диастолическое более 110 мм рт ст; t °C - от 38 °C выше.
Неврологические расстройства: тремор, атаксия; возможно развитие судорожных припадков.
Психические расстройства: бессонница, тревога, психомоторное возбуждение, влечение к ПАВ.
Высокая вероятность развития осложнений (неврологических, психических, соматических).
|
Примечание:
АД - артериальное давление;
ЧСС - частота сердечных сокращений;
мм рт ст - миллиметры ртутного столба;
t °C - температура тела по Цельсию.
После постановки диагноза СО необходимо контролировать состояние пациента в динамике для того, чтобы вовремя диагностировать соматическую, либо неврологическую патологию, которая может возникнуть впоследствии.
2.5. Иные методы диагностики
Иные методы диагностики назначаются специалистами, исходя из конкретной клинической ситуации, в соответствии с показаниями.
3. Лечение
3.1. Общие вопросы лечения синдрома отмены
Терапия СО направлена на устранение тех нарушений, которые вызваны, с одной стороны, хронической интоксикацией, с другой - резким прекращением употребления ПАВ (или снижением его дозы). Терапия может осуществляться в стационарных (в т.ч. в условиях дневного стационара) и амбулаторных условиях. Курс лечения индивидуален, определяется тяжестью состояния, в среднем, составляет до 10 суток.
Лечение в стационарных условиях проводится при среднетяжелом и тяжелом состоянии больного, а легкое течение СО предполагает оказание наркологической помощи в амбулаторных условиях.
Задачи терапии: проведение детоксикации (выведение из организма токсинов экзогенного и эндогенного происхождения), восстановление и стабилизация психофизического состояния больного.
Критерий эффективности лечения: восстановление и стабилизация жизненно-важных функций.
Алгоритм лечебных мероприятий:
1) адекватная инфузионная терапия при тяжелом СО (усиление элиминации);
2) назначение энтеросорбентов (уменьшение адсорбции);
3) специфическая терапия (назначение специфических ЛС или антидотов, если таковые имеются).
Использовать ЛС необходимо строго по показаниям и в каждой клинической ситуации проводить оценку "вред-польза", поскольку вероятность возникновения побочных эффектов и осложнений применения ЛС существенно возрастает в связи с возможным наличием в организме ПАВ и их метаболитов.
Некоторые из принципов детоксикации, существенные для наркологической практики:
1) изолированно проведение детоксикации и купирование СО не является адекватным и полным лечением СЗ;
2) программа детоксикации должна быть максимально индивидуализирована;
3) в программах детоксикации предпочтение необходимо отдавать ЛС с коротким периодом полувыведения;
4) в связи с тем, что выбор протоколов детоксикации при СО ПАВ с доказанной высокой эффективностью невелик, следует использовать необходимый арсенал ЛС, относящихся к симптоматической терапии.
Показания к госпитализации:
СО опиоидов, как правило, протекает тяжело. Поэтому уже первые появляющиеся признаки СО служат поводом для госпитализации пациента.
При СО каннабиноидов для определения тяжести состояния ориентируются на выраженность тревожной симптоматики и бессонницы.
СО от седативных или снотворных препаратов - это состояние, представляющее потенциальную угрозу для жизни, поэтому госпитализация желательна в любом случае, независимо от степени тяжести СО.
При СО от кокаина, других психостимуляторов, включая кофеин, как правило, тяжесть состояния оценивают по выраженности психопатологической (чаще всего - аффективной) симптоматики. Высокий риск психических осложнений (психозы, суицидальная настроенность, тяжелые депрессивные расстройства) определяет необходимость стационарного лечения.
При употреблении галлюциногенов, как уже говорилось выше, СО не всегда имеет место быть. К состояниям, требующим госпитализации, относятся психозы, развивающиеся в острой интоксикации, либо рецидивы психотических состояний (флэшбек) или развитие хронических психозов.
При СО летучих растворителей, если таковой диагностирован, показаниями к госпитализации являются его средняя или тяжелая степень, так как велика вероятность развития неврологических и психотических осложнений.
В подавляющем большинстве случаев, стационарное лечение требуется при средней или тяжелой степени СО. При легкой степени СО лечение может быть проведено в амбулаторных условиях.
- Рекомендуется оказание медицинской помощи при средней и тяжелой степени СО - в стационарных условиях, при легкой степени СО - в амбулаторных условиях [1, 23, 24, 25, 27].
Уровень GPP.
- Рекомендуется осмотр врача психиатра-нарколога не позднее 2 часов с момента поступления в стационар.
Уровень GPP.
- Рекомендуется назначение инфузионной терапии препаратами группы "растворы, влияющие на водно-электролитный баланс" при абстинентном синдроме тяжелой степени для коррекции водно-электролитных нарушений [1, 33, 34].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
Комментарии: При тяжелом течении СО вид употребляемого ПАВ носит второстепенный характер, в большей степени инфузионная терапия направлена на поддержание и стабилизацию гомеостаза, улучшение реологии и микроциркуляции сосудистого русла, нарушения которых связаны с нарастающим эндотоксикозом [33, 34]. В связи с этим проведение дезинтоксикационной терапии плазмозамещающими, гипертоническими, противоотечными растворами рекомендовано в объемах 10 - 20 мл/кг [1, 23, 24].
- Рекомендуется проведение экстракорпоральной детоксикации при абстинентном синдроме тяжелой степени [1].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: При длительном стаже употребления наркотиков, высокой толерантности, стойкой резистентности к проводимой терапии, выраженной соматической отягощенности, тяжело протекающем СО используется не только инфузионная терапия, но и экстракорпоральные методы детоксикации (плазмаферез, гемосорбция или их сочетание) [1, 35, 36, 37].
3.2. Частные вопросы терапии синдрома отмены
3.2.1. Опийный абстинентный синдром
В качестве базовой терапии СО опиоидов в настоящее время в России используются агонисты 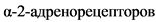 . Существует два основных подхода их использования: либо в качестве самостоятельного средства, либо в сочетании с блокаторами опиатных рецепторов быстрого действия (налоксоном).
. Существует два основных подхода их использования: либо в качестве самостоятельного средства, либо в сочетании с блокаторами опиатных рецепторов быстрого действия (налоксоном).
- Рекомендуется назначение клонидина**# [23, 24, 34, 38, 39, 40, 41, 42, 43, 44, 45].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 2)
Комментарии: Клонидин**# - стимулятор постсинаптических альфа-2-адренорецепторов тормозных структур головного мозга, занимает особое место [34]. Для лечения СО опиоидов данный препарат используется с 1978 года [34]. Несмотря на то, что в показаниях к данному препарату отсутствует СО опиоидов, он широко используется во всем мире в программах опийной детоксикации. Данный феномен можно объяснить существующей научной обоснованностью использования клонидина**# при СО опиоидов. Клонидин**# - средство, снижающее симпатическую гиперстимуляцию при СО опиоидов. Препарат воздействует на центральную нервную систему и периферическую часть вегетативной нервной системы, снижая эндогенное выделение адреналина и НА, которые в состоянии СО присутствуют в организме в избыточном количестве. Центральная адренергическая система тесно связана с дофаминергической и с системой эндогенных опиатов, с чем и связано нормализующее действие клонидина**# на систему катехоламиновой нейромедиации. То есть, по сути, его использование является патогенетической терапией [1, 23, 24, 34, 39].
Методику лечения клонидином**# относят к варианту быстрой детоксикации. Проводится в условиях стационара. Используется в двух вариантах: либо как монотерапия, либо в сочетании с антагонистами опиатных рецепторов короткого действия. Подбор начальной дозы клонидина**# - важный шаг, определяющий эффективность выбранной схемы терапии. В данном случае следует придерживаться правила: подбирается индивидуальная эффективная доза, способная купировать СО опиоидов при минимуме побочных реакций (ПР). Следует обращать внимание на развитие таких ПР, как снижение АД ниже 90/60 мм рт. ст., головокружение, миастения. В случае снижения артериального давления ниже 90/60 мм рт. ст. дозу клофелина уменьшают и назначают кардиотонические средства (кордиамин, кофеин и т.п.).
Минимальная доза клонидина**# составляет, как правило, 0,3 мг. Суточные дозировки препарата не должны превышать 0,6 - 0,9 мг per os на 3 - 4 приема.
Клонидин**# в первую очередь обладает выраженной эффективностью в отношении соматовегетативных расстройств. Отмечено, что влияние клонидина**# на психопатологические и алгические расстройства менее выражено. На неврологическую симптоматику данный препарат влияния не оказывает. Среди побочных эффектов препарата могут быть сухость во рту, выраженная седация.
У больных с длительным стажем заболевания, высокой толерантностью, резистентностью к проводимой терапии, неоднократными безуспешными попытками лечения, выраженными органическими расстройствами для купирования СО опиоидов используется схема детоксикации с применением налоксона гидрохлорида в комбинации с клонидином**#. Схема детоксикации клонидином**# и налоксоном была предложена в 1980 Riordan С.Е., Kleber H.D. [40, 41]. В отечественной практике она нашла применение в несколько переработанном виде, так как дозы клонидина**#, которые приводили Riordan С.Е., Kleber H.D., с современной точки зрения считаются недостаточными, в связи с чем в схемах детоксикации используются дозы клонидина**# от 0,9 мг до 0,45 мг, а налоксона** от 0,2 мг до 0,8 мг в сутки. Длительность приема составляет, как правило, 5 дней с введением тест-дозы налоксона** 0,4 мг в/м. Помимо этого, в данную схему лечения добавляются транквилизаторы в небольших дозах, антипсихотические препараты с преобладанием седативного действия (фенотиазины - с осторожностью!), с целью обеспечения достаточной седации, купирования психомоторного возбуждения и болевых расстройств, свойственных СО опиоидов. Введение налоксона** в данном случае способствует более быстрому выведению опиоидов из организма, что позволяет перевести пациента на лечение блокаторами опиатных рецепотров в возможно короткие сроки [34, 38 - 44].
- Рекомендуется назначение налоксона** в сочетании с клонидином**# пациентам с длительным стажем заболевания, высокой толерантностью, резистентностью к проводимой терапии, неоднократными безуспешными попытками лечения в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [40, 41, 42, 43, 44].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 2).
Комментарии: Налоксон** также используется при отравлениях опийными препаратами (в случае передозировки), для диагностики опийной зависимости и в качестве теста на определение наличия опиоидов в организме (Приложение Е). При передозировках налоксон** вводится внутривенно (всегда в дробных дозах) в зависимости от состояния больного, применяемой дозы наркотиков, видов опиоидов и опыта врача. Первоначально обычно вводится 0,4 мг (1 ампула); в случае необходимости дозу можно повторять через каждые 2 - 3 минуты или увеличить до 1,2 мг, снижая кратность введения до снятия агонистических признаков. Налоксоновую пробу проводят внутримышечно (или подкожно), вводится 0,4 - 1,2 мг налоксона**. Суть проведения налоксоновой пробы заключается в том, чтобы выявить, присутствуют в организме наркотики опийной группы или нет [34, 38, 39, 42, 43, 44].
Достаточно важным вопросом в терапии СО опиоидов является подбор обезболивающих средств. Обезболивающими свойствами обладают ЛС различных фармакологических групп: антагонисты-агонисты опиоидов, ненаркотические анальгетики, некоторые антипсихотики, ингибиторы протеолитических ферментов, холинолитики. В качестве обезболивающих средств в терапии СО опиоидов в настоящее время наиболее широко используются антагонисты-агонисты опиоидных рецепторов. Все препараты этой группы усиливают и потенцируют действие лекарственных средств других групп (антипсихотиков, транквилизаторов, снотворных, других супрессоров ЦНС, нестероидных противовоспалительных средств (НПВС)), поэтому при назначении комплексной терапии необходимо обращать особое внимание на подбор адекватных доз препаратов во избежание развития осложнений.
- Рекомендуется назначение опиоидного ненаркотического анальгетика - трамадола** в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [45, 46, 47, 48, 49, 50].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 2)
Комментарии: Трамадол** воздействует на 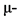 ,
, 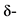 , k-опиатные рецепторы ЦНС. Достаточно давно используется в практике купирования СО опиоидов как в России, так и за рубежом [45 - 50], его эффективность уже не подвергается сомнениям. В первые дни СО при резко выраженном болевом синдроме препарат назначается внутримышечно, затем - перорально. Суточная доза трамадола** в первые 2 - 3 дня СО опиоидов составляет 400 мг. Эта доза считается максимальной. При выраженных болевых расстройствах доза может быть повышена до 600 мг, однако, учитывая, что трамадол** потенцирует действие большинства психотропных препаратов, в высоких дозах препарат может вызывать судороги. Учитывая общий профиль безопасности препарата, назначение доз трамадола**, превышающих рекомендуемые, нежелательно. Доза препарата уменьшается постепенно по мере уменьшения интенсивности болевого синдрома.
, k-опиатные рецепторы ЦНС. Достаточно давно используется в практике купирования СО опиоидов как в России, так и за рубежом [45 - 50], его эффективность уже не подвергается сомнениям. В первые дни СО при резко выраженном болевом синдроме препарат назначается внутримышечно, затем - перорально. Суточная доза трамадола** в первые 2 - 3 дня СО опиоидов составляет 400 мг. Эта доза считается максимальной. При выраженных болевых расстройствах доза может быть повышена до 600 мг, однако, учитывая, что трамадол** потенцирует действие большинства психотропных препаратов, в высоких дозах препарат может вызывать судороги. Учитывая общий профиль безопасности препарата, назначение доз трамадола**, превышающих рекомендуемые, нежелательно. Доза препарата уменьшается постепенно по мере уменьшения интенсивности болевого синдрома.
- Рекомендуется сочетание опиоидного ненаркотического анальгетика с нестероидными противовоспалительными средствами в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 23, 24, 25, 51]
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
Комментарии: Применение опиоидных ненаркотических анальгетиков при лечении СО опиоидов сопряжено с определенными трудностями. У больных достаточно быстро растет толерантность к ним, падает их анальгетическая активность, может развиться лекарственная зависимость. У соматически ослабленных и отягощенных пациентов при применении препаратов с наркотическим действием возможно развитие осложнений в виде общей депривации ЦНС с угнетением дыхания. Поэтому рекомендовано сочетание опиоидных ненаркотических анальгетиков (трамадола**) с ненаркотическими из группы НПВС. При этом, более безопасным является вариант, когда в качестве ведущего ЛС используется НПВС, а опиоидный ненаркотический анальгетик является сопровождающим. Дозы НПВС в наркологической практике используются, как правило, средние и высокие терапевтические [1, 25, 52, 53]. Всемирной организацией здравоохранения (ВОЗ) разработана методика снятия болевого синдрома с помощью легкодоступных средств, она представлена в виде простой и понятной схемы, имеющей название "Лестница обезболивания ВОЗ" [51]. Наиболее важное правило, применяющееся при лечении болевого синдрома - сочетанное использование ненаркотических анальгетиков с наркотическими. То есть, монотерапия наркотическими анальгетиками считается неприменимой.
Чаще всего используются следующие препараты: кеторолак**, лорноксикам**, диклофенак** и некоторые другие.
- Рекомендуется назначение прегабалина в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [54, 55].
Уровень убедительности рекомендаций B (Уровень достоверности доказательств 2)
Комментарии: Использование прегабалина**# становится широко распространенным явлением в наркологической практике. Прегабалин**# - аналог ГАМК, он связывается с дополнительной  субъединицей
субъединицей  потенциалзависимых кальциевых каналов в ЦНС, необратимо замещая [3H]-габапентин. Это позволяет снижать высвобождение глутамата из гипервозбужденных глутататергических нейронов. Предполагается, что такое связывание лежит в основе анальгетического и противосудорожного эффектов препарата.
потенциалзависимых кальциевых каналов в ЦНС, необратимо замещая [3H]-габапентин. Это позволяет снижать высвобождение глутамата из гипервозбужденных глутататергических нейронов. Предполагается, что такое связывание лежит в основе анальгетического и противосудорожного эффектов препарата.
Прегабалин**# используют для купирования болевых расстройств при СО опиоидов. Рекомендуемые дозы - от 60 до 900 мг/сут [54, 55].
По данным пилотных исследований, проведенных в нашей стране, протокол купирования СО опиоидов на основе использования прегабалина**# показал лучшую переносимость лечения, обусловленную менее выраженными, по сравнению с клонидиновым протоколом, центрально-депримирующим действием и астенией [54].
Учитывая то, что данные научных клинических исследований обнадеживают, существует перспектива получения весомых доказательств эффективности в купировании болевых, тревожных расстройств в структуре СО опиоидов. Тем не менее, следует принимать во внимание риски развития зависимости от самого препарата [56, 57, 58, 59].
- Рекомендуется назначение габапентина# в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [60, 61].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
Комментарии: В отношении габапентина# есть исследования, в которых рекомендуется доза 1600 мг/сут [60], и даже до 1800 мг/сут [61] по тем же клиническим показаниям.
- Рекомендуется назначение препаратов группы "антипсихотические средства" в комплексной терапии СО или в качестве адъювантной терапии СО при наличии показаний (психомоторное возбуждение, суицидальное поведение, агрессия, сверхценные образования, асоциальные тенденции в поведении, другие психопатологические проявления), в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 23, 24, 25, 27, 62, 64, 65, 66].
Уровень убедительности рекомендаций B (Уровень достоверности доказательств 3)
Комментарии: Назначение препаратов группы "антипсихотические средства" (антипсихотики), так же, как и других психотропных препаратов, относится в части случаев к адъювантной терапии <8>, в части случаев - к симптоматической терапии <9>.
При выраженных болевых расстройствах, не поддающихся купированием выше указанных групп средств, тяжелой бессоннице, психомоторном возбуждении, поведенческих расстройствах, сопровождающих влечение к наркотику, назначаются антипсихотические средства [62]. Предпочтительны препараты с преобладанием седативного действия, так как достаточная седация в период абстинентных расстройств является скорее необходимым условием, чем нежелательным явлением [1].
Использование антипсихотических средств в периоде абстинентных расстройств относится к патогенетически ориентированному лечению, основано на механизме действия данной группы препаратов на дофаминергические рецепторы (блокада D2, D4 рецепторов обеспечивает снижение ДА в организме, который в период абстинентных расстройств повышен. Это позволяет уменьшить психопатологический компонент СО опиоидов). Следует обращать внимание на подбор дозы, который всегда индивидуален [1, 23, 24, 25, 65]. Дозы галоперидола** колеблются от 1,5 до 20 мг в течение суток на 1 - 4 приема; левомепромазина** от 25 до 200 мг в течение суток на 1 - 4 приема; хлорпромазина** до 800 мг в течение суток на 3 - 4 приема. Следует подчеркнуть, что в настоящее время в наркологической практике предпочтение отдается атипичным антипсихотикам, как ЛС с лучшим профилем безопасности.
С начала 1990-х годов в схемах купирования СО опиоидов в Европе и в России стали широко использовать атипичный антипсихотик из группы замещенных бензаминов тиаприд (он избирательно блокирует дофаминовые D2 рецепторы) [24, 25, 62, 63]. Тиаприд обладает седативным, противосудорожным, антипсихотическим и, что особенно важно, антиалгическим эффектами. Препарат способствует уменьшению, а часто и купированию раздражительности, вспыльчивости, пониженного настроения, тревоги, улучшает сон, что позволяет говорить о снижении выраженности патологического влечения к наркотикам (ПВН). Основными показаниями к его назначению являются психомоторное возбуждение, агрессивное состояние. В отдельных случаях препарат вызывает развитие невыраженного нейролептического синдрома, который купируется либо незначительным снижением дозы препарата, либо добавлением в терапевтические схемы корректоров. Средние суточные дозы тиаприда при СО опиоидов составляют 400 - 600 мг.
Имеются данные об эффективности применения в СО опиоидов другого атипичного антипсихотика - кветиапина**# [64]. Препарат способствует редукции патологического влечения к опиоидам, уменьшает тревогу, снижает проявления болевого синдрома. Препарат назначался по 25 - 50 мг каждые 4 часа при жалобах на влечение к ПАВ, либо каких-либо других симптомах отмены. Максимальная суточная доза кветиапина составляла 200 мг. [64].
При грубых поведенческих расстройствах, состояниях ажитации, повышенного беспокойства, враждебности и агрессивности показал свою эффективность зуклопентиксол** в суточных дозах от 25 - 150 мг [65].
При наличии депрессивных состояний, напряжении, беспокойстве, нарушениях сна используется хлорпротиксен в суточных дозах от 30 до 150 мг [23, 24, 25, 62].
В качестве симптоматической терапии по соответствующим показаниям в СО также могут использоваться и другие антипсихотические препараты, такие как перициазин** (показания: тревожное состояние, психомоторное возбуждение, агрессивное или опасное импульсивное поведение), тиоридазин** (показания: психомоторное возбуждение, тяжелые нарушения поведения, связанные с агрессивностью, состояния страха, тревоги), рисперидон**# (показания: агрессивное поведение), некоторые другие.
Список используемых препаратов широк [1, 23, 24, 25, 62, 65], однако до настоящего времени наблюдается явный дефицит сравнительных клинических исследований, позволяющих сделать однозначные выводы об эффективности и безопасности использования антипсихотических препаратов в терапии не только СО опиоидов, но и других СО.
- Рекомендуется назначение препаратов группы "производные бензодиазепина" в комплексной терапии СО в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 42].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
- Рекомендуется назначение препаратов групп "барбитураты", "барбитураты в комбинации с другими препаратами" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 42].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
Комментарии: В терапии СО опиоидов наиболее часто используются следующие ЛС: диазепам, бромдигидрохлорфенилбензодиазепин, комбинированные препараты: диазепам 0,01 + циклобарбитал 0,1. Применяются данные ЛС по показаниям: нарушения сна, тревога [1, 24, 42] в дозах, определенных инструкцией к препарату.
- Рекомендуется назначение препаратов группы "противоэпилептические средства" в комплексной терапии СО в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 4)
Комментарии: Использование препаратов группы "противоэпилептические средства" (нормотимиков) в лечении СО опиоидов до настоящего времени дискутабельно. Существуют данные о полезности использования карбамазепина** при проявлениях дисфории, эмоциональной лабильности, которые имеют место быть в структуре ПВН [1, 24, 62].
- Рекомендуется у пожилых пациентов купировать СО опиоидов в соответствии с общепринятой практикой [42, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
Комментарии: СО опиоидов у пожилых купируется в соответствии с общепринятой практикой, с учетом возможной корректировки доз препаратов, связанной с возрастными изменениями метаболизма и высоким удельным весом соматической коморбидной патологии. Предпочтение отдается ЛС, имеющим короткий период полувыведения [42, 66].
- Рекомендуется лицам, моложе 18 лет, использовать психосоциальную, семейную психотерапию [42, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
Комментарии: У людей, моложе 18 лет, акцент делается на психосоциальной, семейной терапии. Для определенной части подростков, молодых людей медикаментозное лечение является важным компонентом, несмотря на то, что большинство препаратов, использующихся для купирования ОАС, рекомендованы для лиц старше 18 лет. Любые ЛС назначаются только после оценки "риск/польза" [66].
- Рекомендуется беременным женщинам избегать детоксикацию во втором триместре беременности, она нежелательна в первом триместре, в третьем триместре - с высокой долей осторожности назначение транквилизаторов [42, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5)
3.2.2. Абстинентный синдром, вызванный употреблением каннабиса.
В настоящее время доказательной базы для применения любого вида фармакологического лечения нет. Специфических ЛС для лечения СО, вызванного употреблением каннабиса, нет. Из этого следует вывод, что лечение СО, вызванного употреблением каннабиса, в большей степени симптоматическое.
- Рекомендуется назначение препаратов группы "производные бензодиазепина" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 33, 34, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3)
- Рекомендуется назначение препаратов группы "бензодиазепиноподобные средства" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 33, 34, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3)
Комментарии: ЛС применяются по своим основным показаниям: нарушения сна, тревога [1, 24, 42].
- Рекомендуется назначение препаратов группы "анксиолитики" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 67].
Уровень убедительности рекомендаций B (Уровень достоверности доказательств 3)
- Рекомендуется назначение препаратов группы "антидепрессанты" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [69].
Уровень убедительности рекомендаций B (Уровень достоверности доказательств 3)
Комментарии: Учитывая, что в клинической картине преобладает тревожная симптоматика, базовыми лекарственными средствами являются анксиолитики, снотворные, антидепрессанты. В научной литературе существуют данные об эффективности препаратов этих групп [67, 69]. Однако до настоящего времени результаты данных исследований нельзя назвать однозначными [68], в связи с чем требуется дальнейшее изучение различных групп препаратов [68, 69].
3.2.3. Абстинентный синдром, вызванный употреблением седативных или снотворных препаратов.
Существует сравнительно небольшое количество клинических исследований, позволяющих сделать однозначные заключения в отношении программ терапии СО [70 - 74].
- Рекомендуется ступенчатая отмена психоактивного вещества (gradual dose reduction), к которому развилось привыкание [1, 70, 71, 72, 73, 74].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 1)
Комментарии: Особенностями терапии является ступенчатая отмена препарата, к которому развилось привыкание [1, 70 - 74]. Можно выделить 2 основные стратегии проведения терапии.
1 стратегия: перевод больного на бензодиазепины с более длительным периодом полураспада, такие как клоназепам**, хлордиазепоксид.
2 стратегия: замена препарата, от которого пациент зависим, на фенобарбитал**. В Таблице 5 рассмотрена эквивалентность дозы фенобарбитала** при лечении СО (не то же самое, что терапевтическая эквивалентность) [74].
Таблица 5 - Эквивалент фенобарбитала в абстинентном синдроме, вызванном седативными или снотворными средствами <10>
|
Международное непатентованное наименование <*>
|
Терапевтическая доза, диапазон (мг/день)
|
Доза, эквивалентная 30 мг фенобарбитал для купирования СО (мг)
|
|
Бромдигидрохлорфенилбензодиазепин (Bromdihyarochlorphenylbenzodiazepine)
|
0,5 - 5
|
Нет данных
|
|
Альпразолам (Alprazolam)
|
0,75 - 6
|
1
|
|
Хлордиазепоксид (Chlordiazepoxide)
|
15 - 100
|
25
|
|
Клоназепам (Clonazepam)
|
0.5 - 4
|
2
|
|
Мидазолам (Midazolam)
|
3,5 - 7,5
|
Нет данных
|
|
Диазепам (Diazepam)
|
4 - 40
|
10
|
|
Лоразепам (Lorazepam)
|
1 - 16
|
2
|
|
Оксазепам (Oxazepam)
|
10 - 120
|
10
|
--------------------------------
<*> Препараты, наиболее часто выступающие в роли ПАВ при синдроме зависимости от седативных или снотворных средств
Примечание:
СО - синдром отмены
- Рекомендуется назначение препаратов группы "производные бензодиазепина" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [66, 70, 71, 72, 73].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 1)
- Рекомендуется назначение препаратов группы "барбитураты" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [66, 70, 71, 72, 73, 74].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 1)
- Рекомендуется назначение флумазенила при отсутствии медицинских противопоказаний в соответствии с инструкцией [75, 76]
Уровень убедительности рекомендаций B (Уровень достоверности доказательств 2)
Комментарии: Для больных, зависимых от бензодиазепиновых транквилизаторов, существует терапевтический подход с использованием бензодиазепинового антагониста - флумазенила. Его используют для снижения проявлений СО, тяги к бензодиазепинам [75, 76]. В ряде исследований парентеральное введение флумазенила показало положительный терапевтический эффект при купировании СО бензодиазепинов, данная схема терапии была высоко безопасной для пациентов [75]. В других источниках существуют рекомендации использования флумазенила в том случае, если пациент недавно перенес передозировку бензодиазепинами [66].
- Рекомендуется назначение препаратов группы "противоэпилептические средства" в качестве альтернативной терапии СО в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [77, 78, 79].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
Комментарии: Препараты группы "Противоэпилептические средства" (антиконвульсанты) могут быть использованы в качестве альтернативных ЛС при купировании СО, то есть, вместо бензодиазепинов [77, 78, 79, 80]. Чаще всего используется карбамазепин**. Назначается доза карбамазепина** до 800 мг, а отмена препарата, которым пациент злоупотреблял, проводится одномоментно [80]. Однако в данном случае следует обратить внимание на сравнительно низкое качество доказательств представленных исследований [81].
- Рекомендуется у пожилых пациентов применять программы терапии, соответствующие общепринятым подходам. Длительность постепенного снижения дозы препарата, как правило, увеличивается [66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
- Рекомендуется у пожилых пациентов в качестве препарата-замены использовать препараты группы "производные бензодиазепина" с коротким периодом полувыведения [66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
- Рекомендуется у людей, моложе 18 лет, использовать психосоциальные интервенции [82].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Медикаментозное лечение следует применять только после тщательной оценки "риск/польза" в контексте комплексных программ терапии, включающих различные психосоциальные, психотерапевтические и семейные подходы. В качестве основного ЛС, направленного на купирование СО, рекомендован диазепам** [82]
- Рекомендуется беременных женщин вести совместно с акушером-гинекологом [1].
Уровень GPP.
3.2.4. Абстинентный синдром, вызванный употреблением кокаина, других стимуляторов, включая кофеин
Специфических схем терапии и ЛС для лечения СО, вызванного употреблением кокаина, других психостимуляторов, нет. При анализе имеющихся исследований не было найдено убедительных данных, свидетельствующих о превалировании какого-либо ЛС или метода терапии [66].
Несмотря на то, что СО, вызванный употреблением психостимуляторов, протекает сравнительно мягко, тем не менее, необходимо учитывать высокую вероятность развития суицидально опасных состояний, глубоких дисфорий, в отношении физических страданий в первую очередь, необходимо обращать внимание на сердечно-сосудистую систему.
Терапия в данном случае симптоматическая. Подходы к терапии и алгоритм лечебных мероприятий общий.
- Рекомендуется назначение препаратов групп "производные бензодиазепина" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 62, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
- Рекомендуется назначение препаратов группы "анксиолитики" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 62, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
- Рекомендуется назначение препаратов группы "барбитураты" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [1, 24, 62, 66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 3).
Комментарии: Применяются данные ЛС при по показаниям: нарушения сна, тревога [1, 24, 25, 62, 66]. Дозы соответствуют рекомендованным в инструкции. При некупирующемся возбуждении, судорожном состоянии применяются барбитураты короткого действия (тиопентал натрия** гексобарбитал) под постоянным контролем дыхания и кровообращения).
- Рекомендуется назначение препаратов группы "антидепрессанты" в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний в соответствии с инструкцией [83, 84, 85, 86].
Уровень убедительности рекомендаций B (Уровень достоверности доказательств 2).
Комментарии: При СО, вызванного употреблением кокаина и других психостимуляторов, препаратами выбора являются антидепрессанты [83]. Наиболее широко используются те ЛС, которые влияют на дофаминергическую и серотонинергическую нейромедиацию [84, 85]. В научных клинических исследованиях было показано, что антидепрессанты влияют на влечение к ПАВ в краткосрочной перспективе [24, 25, 86]. Справедливости ради следует отметить, что до настоящего времени однозначного мнения по поводу использования антидепрессантов в терапии синдрома отмены психостимуляторов, нет [87]. Другие психотропные препараты (производные безодиазепина, антипсихотики, противоэпилептические средства) используются по показаниям [62]. Использование ЛС, относящихся к группе "психостимуляторы" в программах терапии синдрома отмены психостимуляторов (в основном, это актуально для зарубежной практики), в настоящее время весьма дискутабельно, так как проведенные мета-анализы не позволяют сделать однозначный вывод об их эффективности [88].
- Рекомендуется для пожилых пациентов применять программы терапии, соответствующие общепринятым подходам [66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Для пожилых лиц, страдающих синдромом зависимости от психостимуляторов, предусмотрены такие же подходы к лечению, как и для взрослого населения с учетом корректировки доз, опирающейся на возрастные фармкокинетические и фармакодинамические особенности, а также свойственной возрасту соматической отягощенности.
- Рекомендуется у людей, моложе 18 лет, использовать психосоциальные интервенции [82].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: У лиц, моложе 18 лет, акцент делается на психосоциальных интервенциях. Медикаментозное лечение следует применять только после тщательной оценки "риск/польза" в контексте комплексных программ терапии, включающих различные психосоциальные, психотерапевтические и семейные подходы [82].
- Беременным женщинам рекомендуется воздерживаться от фармакологического вмешательства [66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Предпочтительны психологические/психотерапевтические программы. Любые ЛС назначаются только после оценки риск/польза [66].
3.2.5. Абстинентный синдром, вызванный употреблением летучих растворителей.
СО при употреблении летучих растворителей (ингалянтов) может протекать тяжело, так как наблюдается большое количество соматических и неврологических осложнений, являющихся по механизму развития (см. информацию выше) проявлениями токсикогенной симптоматика или обострением латентной патологии. К ним относится и грубая неврологическая патология, и поражения внутренних органов - сердца, почек, легких, печени, поджелудочной железы.
Универсального протокола детоксикации нет [66]. Подходы к терапии, группы применяемых лекарственных средств (ЛС) идентичны таковым при алкогольном абстинентном синдроме (ААС), а также при СО, вызванном употреблением седативных или снотворных средств [1, 24, 66]. Лечение проводится симптоматически в соответствии с медицинскими показаниями. Базовые подходы: проведение инфузионной терапии, назначение препаратов групп "аксиолитики", "барбитураты", "другие психостимуляторы и ноотропные препараты". Препараты групп "противоэпилептические средства", "антипсихотические средства" назначаются по показаниям, с осторожностью, с учетом возраста пациента (зависимость от ингалянтов является прерогативой подросткового возраста).
- Рекомендуется у людей, моложе 18 лет, использовать медикаментозное лечение соответствует таковому для взрослого населения с учетом коррекции доз ЛС, основанных на возрастных особенностях метаболизма, влияющих на фармакокинетику и фармакодинамику препаратов [66].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
3.2.6. Абстинентный синдром при полинаркомании
В клинической практике в настоящее время довольно широко распространено такое явление, как синдром зависимости от нескольких ПАВ (см. раздел "эпидемиология"), соответственно, клиническая картина СО представляется пестрой, неоднородной, смешанной. В таких случаях терапевтическая тактика определяется, исходя из превалирующей клинической симптоматики с использованием рекомендованного для каждого ПАВ протокола лечения одновременно или последовательно [1, 66, 89].
3.3. Психотерапия при абстинентном синдроме
В острых состояниях, каковым является СО, психотерапевтическое воздействие резко ограничено. Основная задача психотерапевтического воздействия в этот период: вовлечение пациента и его удержание в лечебной программе, которая не ограничивается рамками купирования АС. Необходимо информировать пациента о дальнейшей терапии синдрома зависимости. В этот период необходимо провести семейное консультирование таким образом, чтобы вовлечь членов семьи и значимых людей в терапевтическую программу.
- Рекомендуется проведение семейной психотерапии всем, у кого в доступе есть родственник/родственники или значимое лицо [90, 91, 92, 93, 94, 95, 96, 97, 98].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 1).
3.3. Психотерапия при абстинентном синдроме
В острых состояниях, каковым является СО, психотерапевтическое воздействие резко ограничено. Основная задача психотерапевтического воздействия в этот период: вовлечение пациента и его удержание в лечебной программе, которая не ограничивается рамками купирования АС. Необходимо информировать пациента о дальнейшей терапии синдрома зависимости. В этот период необходимо провести семейное консультирование таким образом, чтобы вовлечь членов семьи и значимых людей в терапевтическую программу.
- Рекомендуется проведение семейной психотерапии всем, у кого в доступе есть родственник/родственники или значимое лицо [90, 91, 92, 93, 94, 95, 96, 97, 98].
Уровень убедительности рекомендаций A (Уровень достоверности доказательств 1).
3.4. Оценка эффективности и безопасности лечения
- Для оценки эффективности терапии рекомендуется использовать клинический или психометрический методы [1].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Оценка эффективности комплексного лечения проводится, исходя из динамки психопатологических, соматовегетативных и неврологических нарушений СО, что позволяет сделать клинический метод - наблюдение и описание симптоматики.
Критерий эффективности медикаментозного лечения: восстановление и стабилизация жизненно-важных функций.
Критерий эффективности психотерапевтического лечения: удержание пациента в лечебной программе, его согласие на продолжение лечения.
- Оценку безопасности терапии рекомендуется проводить по частоте возникновения и развития нежелательных явлений [1].
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Оценка безопасности и переносимости терапии проводится на всем ее протяжении по частоте возникновения и развития нежелательных явлений (НЯ) <11>
НЯ регистрируются по данным:
- спонтанных сообщений пациентов;
- физикального осмотра и клинически значимых изменений жизненно важных показателей (АД, ЧСС, ЧДД, температура тела) от исходных значений;
- клинически значимых отклонениям показателей лабораторных анализов и инструментальных методов диагностики от исходных значений.
Связь НЯ с ЛС оценивается по алгоритму Наранжо <12> (Приложение Ж). Степень достоверности взаимосвязи "ЛС-НЯ" по алгоритму Наранжо определяется как:
определенная, если 9 и более баллов;
вероятная, если 5 - 8 баллов;
возможная, если 1 - 4 балла;
сомнительная, если 0 баллов и меньше.
При возникновении НЯ врачу необходимо зарегистрировать свои действия в первичной документации, к примеру, назначить дополнительные препараты (какие, в какой дозе, на какой период) и др., а также заполнить соответствующую форму <13>
4. Реабилитация
Реабилитация при СО не проводится.
5. Профилактика
5.1 Профилактика
При сформированном СО наиболее важное значение приобретает третичная (модификационная) профилактика. Она является преимущественно медицинской, индивидуальной, ориентирована на лиц со сформированной зависимостью от ПАВ, направлена на предупреждение дальнейшего развития заболевания, уменьшение вредных последствий и на предупреждение рецидива.
5.2. Диспансерное наблюдение
Диспансерное наблюдение осуществляется в соответствии с Порядком диспансерного наблюдения за лицами с психическими расстройствами и/или расстройствами поведения, связанными с употреблением ПАВ <14>
6. Дополнительная информация, влияющая на течение и исход заболевания
Организация медицинской помощи
- Рекомендуется госпитализация в плановом порядке при СО средней степени тяжести.
Уровень GPP
- Рекомендуется госпитализация по неотложным показаниями при:
- СО тяжелой степени;
- СО средней или тяжелой степени с сопутствующей соматоневрологической патологией в субкомпенсированной стадии;
- СО средней или тяжелой степени, осложненном судорожным припадком/ами, развившимся/имися в течение 24 - 48 часов;
- СО средней или тяжелой степени, осложненном делирием или иным психотическим расстройством.
Уровень GPP.
- Медицинскими показаниями к выписке пациента из стационара рекомендуется считать купирование проявлений СО - восстановление психофизического состояния пациента.
Уровень убедительности рекомендаций C (Уровень достоверности доказательств 5).
Комментарии: Восстановление психофизического состояния пациента предполагает:
- наличие ясного сознания (ориентировка в месте, времени и собственной личности полная, правильная);
- отсутствие слуховых, визуальных и тактильных расстройств;
- отсутствие двигательного возбуждения;
- положительную динамику психопатологических расстройств: редукция тревоги, дисфории, эмоциональной лабильности, восстановление сна и др. (если таковые имелись);
- положительную динамику неврологических расстройств: тремора, головной боли, тяжести в голове и др. (если таковые имелись);
- положительную динамику соматических расстройств: тошноты, рвоты, пароксизмальной потливости, АД, болевых расстройств (если таковые имелись).
Критерии оценки качества медицинской помощи
|
N
|
Критерии качества
|
Уровень достоверности доказательств
|
Уровень убедительности рекомендаций
|
|
1.
|
Выполнен осмотр врачом-психиатром-наркологом не позднее 2 часов с момента поступления в стационар
|
GPP
|
|
|
2.
|
Выполнен общий (клинический) анализ мочи
|
5
|
C
|
|
3.
|
Выполнен общий (клинический) анализ крови развернутый
|
5
|
C
|
|
4.
|
Выполнен анализ крови биохимический общетерапевтический (общий белок, аланинаминотрансфераза, аспартатаминотрансфераза, гамма-глугамилтранспептидаза общий билирубин, прямой билирубин, альбумин, глюкоза, общий холестерин)
|
5
|
C
|
|
5.
|
Выполнена регистрация электрокардиограммы
|
5
|
C
|
|
6.
|
Проведен иммуноферментный анализ при первичном скрининге мочи на содержание психоактивных веществ
|
3
|
C
|
|
7.
|
Проведено подтверждение с помощью газовой хроматографии/масс-спектрометрии или высокоэффективной жидкостной хроматографии при положительных результатах иммуноферментного анализа
|
3
|
C
|
|
8.
|
Проведена терапия клонидином при синдроме отмены опиоидов (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
2
|
A
|
|
9.
|
Проведена терапия сочетанием налоксона и клонидина при синдроме отмены опиоидов (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
2
|
A
|
|
10.
|
Проведена терапия опиоидным ненаркотического анальгетиком - трамадолом при синдроме отмены опиоидов (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
2
|
A
|
|
И.
|
Проведено сочетанное назначение опиоидного ненаркотического анальгетика с нестероидными противовоспалительными средствами при синдроме отмены опиоидов (в зависимости от медицинских показании и при отсутствии медицинских противопоказаний)
|
5
|
C
|
|
12.
|
Проведено назначение прегабалина при синдроме отмены опиоидов (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
2
|
B
|
|
13.
|
Проведена ступенчатая отмена психоактивного вещества (gradual dose reduction), к которому развилось привыкание, при синдроме отмены седативных или снотворных средств
|
1
|
A
|
|
14.
|
Проведена терапия флумазенилом при синдроме отмены седативных или снотворных средств (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
2
|
B
|
|
15.
|
Проведена терапия препаратами группы "антипсихотические средства" в зависимости от медицинских показаний (психомоторное возбуждение, суицидальное поведение, агрессия, сверхценные образования, асоциальные тенденции в поведении, другие психопатологические проявления), при отсутствии медицинских противопоказаний
|
3
|
B
|
|
16.
|
Проведена терапия препаратами группы "производные бензодиазепина" (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
1*
см. примечание
|
|
|
17.
|
Проведена терапия препаратами группы "барбитураты" (в зависимости от медицинских показании и при отсутствии медицинских противопоказаний)
|
2*
см. примечание
|
|
|
18.
|
Проведена терапия препаратами группы "анксиолитики" (в зависимости от медицинских показании и при отсутствии медицинских противопоказаний)
|
3*
см. примечание
|
|
|
19.
|
Проведена терапия препаратами группы "антидепрессанты" (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
4*
см. примечание
|
|
|
20.
|
Проведена терапия препаратами группы "противоэпилептические средства" в качестве альтернативной терапии (в зависимости от медицинских показаний и при отсутствии медицинских противопоказаний)
|
5*
см. примечание
|
Примечание:
(1*):1A - при синдроме отмены седативных и снотворных средств;
3C - при синдроме отмены каннабиноидов;
C3 - при синдроме отмены кокаина и других психостимуляторов;
4C - при синдроме отмены опиоидов
(2*):1A - при синдроме отмены седативных и снотворных средств;
3C - при синдроме отмены кокаина и других психостимуляторов;
5C - при синдроме отмены опиоидов
(3*):3B - при синдроме отмены каннабиноидов;
3C - при синдроме отмены кокаина и других психостимуляторов
(4*):2В - при синдроме отмены кокаина и других психостимуляторов;
3B - при синдроме отмены каннабиноидов
(5*):3C - при синдроме отмены седативных и снотворных средств;
4C - при синдроме отмены опиоидов
Список литературы
Литература
1. Иванец Н.Н., Анохина И.П., Винникова М.А., редакторы. Наркология: национальное руководство. 2-е издание, переработанное и дополненное. М.: ГЭОТАР-Медиа, 2016. 944 с.
2. Pertwee R.G. Ligands that target cannabinoid receptors in the brain: from THC to anandamide and beyond. Addict Biol. 2008 Jun; 13(2): 147 - 159. doi: 10.1111/j.l369-1600.2008.00108.x. URL: https://www.ncbi.nlm.nih.gov/pubmed/18482430/ (https://www.ncbi.nlm.nih.gov/pubmed/18482430/) Дата обращения: 10.07.2018.
3. Di Marzo V., De Petrocellis L., Fezza F., Ligresti A., Bisogno T. Anandamide receptors. Prostaglandins Leukot Essent Fatty Acids. 2002 Feb-Mar; 66(2-3): 377 - 391. URL: https://www.ncbi.nlm.nih.gov/pubmed/12052051. (https://www.ncbi.nlm.nih.gov/pubmed/12052051.) Дата обращения: 10.07.2018.
4. Nader J., Rapino C., Gennequin B., Chavant F., Francheteau M., Makriyannis A., Duranti A., Maccarrone M., Solinas M., Thiriet N. Prior stimulation of the endocannabinoid system prevents methamphetamine-induced dopaminergic neurotoxicity in the striatum through activation of CB2 receptors. Neuropharmacology. 2014 Dec; 87: 214 - 221. doi: 10.1016/j.neuropharm.2014.03.014. URL: https://www.ncbi.nlm.nih.gov/pubmed/24709540. (https://www.ncbi.nlm.nih.gov/pubmed/24709540.) Дата обращения: 10.07.2018.
5. Paez-Martinez N., Aldrete-Audiffred J., Gallardo-Tenorio A., Castro-Garcia M., Estrada-Camarena E., Lopez-Rubalcava C. Participation of GABAA, GABA(B) receptors and neurosteroids in toluene-induced hypothermia: evidence of concentration-dependent differences in the mechanism of action. Eur J Pharmacol. 2013 Jan 5; 698(1-3): p. 178 - 85. doi: 10.1016/j.ejphar.2012.10.004.
6. Shelton K.L. Discriminative Stimulus Effects of Abused Inhalants. Curr. Top. Behav. Neurosci. 2018; 39: 113 - 139. doi: 10.1007/7854 - 2016 - 22 URL: https://www.ncbi.nlm.nih.gov/pubmed/27714629 (https://www.ncbi.nlm.nih.gov/pubmed/27714629) Дата обращения: 10.07.2018.
7. Соловьев А.Г., Вязьмин А.М., Мордовский Э.А. Методологические подходы к учету алкоголь-атрибутивной смертности в России и за рубежом. Обзоры по клинической фармакологии и лекарственной терапии. 2012; N 4 (10): с. 30 - 41.
8. Global status report on alcohol and health - 2014 ed. URL: http: www.who.int(www.who.int) World Health Organization 2014; 86 c. ISBN 978 92 4 069276 3 (PDF) Дата обращения: 28.02.2017.
9. Всемирный доклад о наркотиках. 2015. URL: http://www.unodc.org/documents/wdr2015/WDR15_ExSum_R.pdf (http://www.unodc.org/documents/wdr2015/WDR15_ExSum_R.pdf) Дата обращения: 28.02.2017.
10. Всемирный доклад о наркотиках. 2013. URL: http://www.unodc. org/unodc/secured/wdr/wdr2013/WDR2013ExSum_R.pdf (http://www.unodc.org/unodc/secured/wdr/wdr2013/WDR2013ExSum_R.pdf) Дата обращения: 28.02.2017.
11. Word Drug Report 2018 URL: http://www.unodc.org/wdr2018/prelaunch/WDR18_Booklet_2_GLOBAL.pdf (http://www.unodc.org/wdr2018/prelaunch/WDR18_Booklet_2_GLOBAL.pdf) Дата обращения: 10.07.2018.
12. European Drug Report 2016: Trends and Developments. EMCDDA, Lisbon, May 2016 URL: http://www.emcdda.europa.eu/publications/edr/trends-developments/2016. (http://www.emcdda.europa.eu/publications/edr/trends-developments/2016.) Дата обращения: 28.02.2017.
13. Perspectives On Drugs Cocaine trafficking to Europe. URL: http://www.emcdda.europa.eu/system/files/publications/2702/Cocaine/%20trafficking_POD2016.pdf(http://www.emcdda.europa.eu/system/files/publications/2702/Cocaine%20trafficking_POD2016.pdf) Дата обращения: 28.02.2017.
14. Оценка наркоситуации в среде детей, подростков и молодежи. Часть II URL: http://www.narkotiki.ru/5_5663.htm (http://www.narkotiki.ru/5_5663.htm) Дата обращения: 28.02.2017.
15. Доклад Международного комитета по контролю над наркотиками за 2014 год. URL: http://www.nncn.ru/objects/nncn01/1425384831.pdf (http://www.nncn.ru/objects/nncn01/1425384831.pdf) Дата обращения: 28.02.2017.
16. European Drug Report 2015 Trends and Developments EMCDDA, Lisbon, June 2015 URL: http://www.emcdda.europa.eu/publications/edr/trends-developments/2015 (http://www.emcdda.europa.eu/publications/edr/trends-developments/2015) Дата обращения: 28.02.2017.
17. EMCDDA-Europol 2014 Annual Report on the implementation of Council Decision URL: http://www.emcdda.europa.eu/publications/implementation-reports/2014. (http://www.emcdda.europa.eu/publications/implementation-reports/2014.) Дата обращения: 28.02.2017.
18. Киржанова В.В., Григорова Н.И., Киржанов В.Н., Сидорюк О.В. Основные показатели деятельности наркологической службы в Российской Федерации в 2014 - 2015 годах: статистический сборник. М.: НИИ наркологии - филиал ФГБУ "ФМИЦПН им. В.П. Сербского" Минздрава России; 2016. 177 с.
19. Киржанова В.В., Григорова Н.И., Киржанов В.Н., Сидорюк О.В. Основные показатели деятельности наркологической службы в Российской Федерации в 2015 - 2016 годах: статистический сборник М.: ФГБУ "ФМИЦПН им. В.П. Сербского" Минздрава России; 2017. 183 с.
20. Научно обоснованное мнение о безопасности кофеина. Часть 2. Наркология. 2015; N 9: с. 45 - 59 (пер. EFSA Journal 2015 13(5).
21. Diagnostic and statistical manual of mental disorders.5th ed.; DSM-5; American Psychiatric Association, 2013: p. 481 - 590, 809 - 916.
22. Научно обоснованное мнение о безопасности кофеина. Наркология. 2015; N 8: с. 45 - 58 (пер. EFSA Journal 2015 13(5).
23. Иванец Н.Н., Винникова М.А. Психические и поведенческие расстройства вследствие злоупотребления психоактивными веществами. Психиатрия: национальное руководство. Под редакцией Т.Б. Дмитриевой, В.Н. Краснова, Н.Г. Незнанова, В.Я. Семке, А.С. Тиганова. М.: Гэотар-Медиа; 2009. с. 409 - 442.
24. Рациональная фармакотерапия в психиатрической практике: руководство для практикующих врачей. Под общей редакцией Ю.А. Александровского, Н.Г. Незнанова. М.: Литтера; 2014. 1080 с. (Серия "Рациональная фармакотерапия").
25. Александровский Ю.А., Незнанов Н.Г., редакторы. Психиатрия: национальное руководство. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа; 2018. 1008 с.
26. Гофман А.Г. Клиническая наркология. М.: Миклош; 2003. 215 с.
27. Иванец Н.Н., Даренский И.Д., Стрелец Н.В., Уткин С.И. Лечение алкоголизма, наркоманий, токсикоманий (в таблицах). М.: Анахарсис; 2002. 57 с.
28. Standridge J.B., Adams S.M., Zotos А.Р. Urine Drug Screening: A Valuable Office Procedure. Am. Fam. Physician. 2010 Mar 1; 81(5): p. 635 - 640.
29. Moeller K.E., Lee K.C., Kissack J.C. Urine drug screening: practical guide for clinicians [published correction appears in Mayo Clin Proc. 2008; 83(7): p. 851]. Mayo Clin Proc. 2008; 83(1): p. 66 - 76.
30. Jaffee W.B., Trucco E., Levy S., Weiss R.D. Is this urine really negative? A systematic review of tampering methods in urine drug screening and testing. Subst Abuse Treat. 2007; 33(1): p. 33 - 42.
31. US Department of Health and Human Services. Substance Abuse and Mental Health Services Administration Division of Workplace Programs. Urine specimen collection handbook for federal agency workplace drug testing programs. November 2004. URL:http://workplace.samhsa.gov/DrugTesting/Level_1_Pages/HHS%20Urine%20Specimen%20Collection%20Handbook%20(Eff January 7, 2009. Дата обращения: 28.02.2017.
32. Specimen Validity Testing. Substance Abuse and Mental Health Services Administration Division of Workplace Programs. February 2005. URL: http://workplace.samhsa.gov/DrugTesting/Files_Drug_Testing/Labs/Specimen%20Validity%20Testing%20-%20February%202005.pdf.
(http://workplace.samhsa.gov/DrugTesting/Files_Drug_Testing/Labs/Specimen%20Validity%20Testing%20-%20February%202005.pdf.) Accessed January 7, 2009. Дата обращения: 28.02.2017.
33. Detoxification From Alcohol and Other Drugs. Treatment Improvement Protocol (TIP). Series, No. 19.
URL: https://www.ncbi.nlm.nih.gov/books/NBK64513/ (https://www.ncbi.nlm.nih.gov/books/NBK64513/) Дата обращения: 11.08.2018.
34. Detoxification and Substance Abuse Treatment. Treatment Improvement Protocol (TIP) Series, No. 45. URL:https://www.ncbi.nlm.nih.gov/books/NBK64115/Дата обращения: 11.08.2018.
35. Малин Д.И., Медведев В.М., Общие принципы неотложной терапии критических состояний в психиатрии и наркологии. Психиатрия и психофармакотерапия. 2006; 01: 17 - 20.
36. Костюченко А.Л., редактор. Эфферентная терапия. СПб: Фолиант; 2003. 432 с.
37. Vitaly Pishel (et al) Application of Plasmapheresis in Emergency Treatment of Opiate Withdrawal Syndrome Volume 12, Issue S1 (Abstracts of Scientific Papers - Tenth World Congress on Disaster and Emergency Medicine, 26 - 27 September 1997, Mainz, Germany) September 1997, p. S33.
38. Филибек У., Стерниери Е., Е. де Якобс. Методическое руководство по профилактике и фармакологическому лечению героиновой зависимости URL: http://www.narcom.ru/publ/info/141.(http://www.narcom.ru/publ/info/141.) Дата обращения: 11.08.2018.
39. WHO Library Cataloguing-in-Publication Data Guidelines for the psychosocially assisted pharmacological treatment of opioid dependence. URL: http://new.enpud.org/pdf/2012-01-30_Guidelines%20for%20the%20psychosocially%20assisted%20pharmacological%20treatment%20of%20opioid%20dependence.pdf (http://new. enpud. org/pdf/2012-01-30_Guidelines%20for%20the%20psychosocially%20assisted%20pharmacological%20treatment%20of%20opioid%20dependence.pdf) Дата обращения: 28.02.2017.
40. Riordan C.E., Kleber,H.D. Rapid opiate detoxification with clonidine and naloxone. Lancet. 1980; 1:1079.
41. Kleber H.D. Detoxification from narcotics. In: Lowinson J.H., Ruitz P. eds.: Substance abuse, clinical problems and perspectives. Baltimore: Williams & Wilkins. 1981; 24: 317 - 338.
42. Drug Misuse. Opioid detoxification. National Clinical Practice Guideline Number 52. National Collaborating Centre for Mental Health commissioned by the National Institute for Health & Clinical Excellence published. URL: https://www.ncbi.nlm.nih.gov/books/NBK50622/pdf/Bookshelf_NBK50622.pdf (https://www.ncbi.nlm.nih.gOv/books/NBK50622/pdf/Bookshelf_NBK50622.pdf) Дата обращения: 28.02.2017.
43. Gold M.S., Dackis C.A., Washton A.M. The sequential use of clonidine and naltrexone in the treatment of opiate addicts. Advances in Alcohol and Substance Abuse. 1984; 3(3): 19 - 39. URL: [PubMed] Дата обращения: 28.02.2017.
44. Gowing L., Farrell M., Ali R. (2009b) Alpha2-adrenergic agonists for the management of opioid withdrawal.
Cochrane Database Syst Rev 2: URL: [https://www.ncbi.nlm.nih.gov/pubmed/24683051 (https://www.ncbi.nlm.nih.gov/pubmed/24683051)] Дата обращения: 28.02.2017.
45. Воронин К.Э., Рохлина М.Л., Петракова Л.Б. Клинические проявления и патогенетические методы лечения опийного абстинентного синдрома. В сборнике: Актуальные проблемы медико-социальной реабилитации больных алкоголизмом и наркоманиями. 1994; с. 125 - 129.
46. Dunn K.E., Tompkins D.A., Bigelow G.E., Strain E.C. Efficacy of Tramadol Extended-Release for Opioid Withdrawal: A Randomized Clinical Trial. JAMA Psychiatry. 2017 Sep 1; 74(9): 885 - 893. doi: 10.1001/jamapsychiatry.2017.1838.
47. Полецкий В.М., Куркин С.Д. Обзор подходов к купированию опийного абстинентного синдрома. В сборнике: актуальные проблемы возрастной наркологии материалы региональной междисциплинарной научно-практической конференции. 2012; с. 62 - 66.
48. Ziaaddini H, Ziaaddini A, Asghari N, Nakhaee N, Eslami M. Trial of tramadol plus gabapentin for opioid detoxification. Iran Red Crescent Med J. 2014 Dec 29; 17(1). doi: 10.5812/ircmj. 18202. URL: https://www.semanticscholar.org/paper/Trial-of-Tramadol-Plus-Gabapentin-for-Opioid-Ziaaddini-Ziaaddini/df3f51dda7822b7ac5ff7a6add1f36926c8c0225 (https://www.semanticscholar.org/paper/Trial-of-Tramadol-Plus-Gabapentin-for-Opioid-Ziaaddini-Ziaaddini/df3f51dda7822b7ac5ff7a6add1f36926c8c0225) Дата обращения: 09.09.2018
49. Chawla J.M., Pal H., Lai R., Jain R., Schooler N., Balhara Y.P. Comparison of efficacy between buprenorphine and tramadol in the detoxification of opioid (heroin)-dependent subjects. Journal Opioid Management. 2013 Jan-Feb; 9(1): 35 - 41. URL: https://www.ncbi.nlm.nih.gov/ (https://www.ncbi.nlm.nih.gov/) Дата обращения: 28.02.2017.
50. Zarghami M., Masoum B., Shiran M.R. Tramadol versus methadone for treatment of opiate withdrawal: a doubleblind, randomized, clinical trial. Addict Dis. 2012; 31(2): 112 - 117. URL: https://www.ncbi.nlm.nih.gov/ (https://www.ncbi.nlm.nih.gov/) Дата обращения: 28.02.2017.
51. Абузарова Г.Р., Невзорова Д.В., Кумирова Э.В., Савва Н.Н., Арутюнов Г.П., Багненко С.Ф., Данилов Ал.Б., Данилов А.Б., Куняева Т.А., Молчанов И.В., Падалкин В.П., Поляков В.Г., Пчелинцев М.В., Степаненко С.М. Обезболивание взрослых и детей при оказании медицинской помощи. М.: ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России; 2016. 94 с.
52. Иванец Н.Н., Винникова М.А. Опыт применения ксефокама (лорноксикама) при купировании болевого синдрома у больных героиновой наркоманией. Вопросы наркологии. 2001; 4: 3 - 9.
53. Иванец Н.Н., Винникова М.А., Русинова О.И. Перспективы применения нестероидных противовоспалительных препаратов в наркологической клинике (на примере кетанова). Вопросы наркологии. 2003; 6: 6 - 14.
54. Крупицкий Е.М., Илюк Р.Д., Михайлов А.Д., Казанков К.А., Рыбакова К.В., Скурат Е.П., Гришина О.Г., Заплаткин И.А., Ветрова М.В., Незнанов Н.Г. Рандомизированное контролируемое исследование эффективности прегабалина в терапии синдрома отмены опиатов. Журнал неврологии и психиатрии им. С.С. Корсакова. 2016; 7: 29 - 36.
55.  N., Lemenager T., Grosshans M., Kiefer F., Hermann D. Pregabalin for the reduction of opiate withdrawal symptoms. Psychiatr Prax. 2012 Oct; 39(7): 351 - 352. URL: https://www.ncbi.nlm.nih.gov/pubmed/22689280 (https://www.ncbi.nlm.nih.gov/pubmed/22689280) Дата обращения: 28.02.2017.
N., Lemenager T., Grosshans M., Kiefer F., Hermann D. Pregabalin for the reduction of opiate withdrawal symptoms. Psychiatr Prax. 2012 Oct; 39(7): 351 - 352. URL: https://www.ncbi.nlm.nih.gov/pubmed/22689280 (https://www.ncbi.nlm.nih.gov/pubmed/22689280) Дата обращения: 28.02.2017.
56. Martinotti G. Pregabalin in clinical psychiatry and addiction: pros and cons. Expert Opin Investig Drugs. 2012 Sep; 21(9):1243-1245. URL: https://www.ncbi.nlm.nih.gov/pubmed/22725618 (https://www.ncbi.nlm.nih.gov/pubmed/22725618) Дата обращения: 28.02.2017.
57. Рохлина М.Л., Ненастьева А.Ю., Усманова Н.Н., Захаров Е.Д., Демурова В.Н. Злоупотребление прегабалином (Лирикой). Вопросы наркологии. 2015; 3: 9 - 15.
58. Пискунов М.В., Кривенков А.Н., Рейхель Н.В. Зависимость от прегабалина ("Лирика"): обзор литературы и собственные клинические наблюдения. Наркология. 2013; 4: 52 - 56.
59. Boschen M.J. Pregabalin: Dose-responship in generalized anxiety disorder. Pharmacopsychiatry. 2012; 45(2): 51 - 56.
60. Salehi M., Kheirabadi G.R., Maracy M.R., Ranjkesh M. Importance of gabapentin dose in treatment of opioid withdrawal. Clin Psychopharmacol. 2011 Oct; 31(5): 593 - 596. URL: https://www.ncbi.nlm.nih.gov/pubmed/21869694 (https://www.ncbi.nlm.nih.gov/pubmed/21869694) Дата обращения: 28.02.2017.
61.  J., Sabater A., Perez-Galvez B., Castellano М., Cervera G. Add-on gabapentin in the treatment of opiate withdrawal. Prog Neuropsychopharmacol Biol Psychiatry. 2004 May; 28(3): 599 - 601. URL: https://www.ncbi.nlm.nih.gov/pubmed/15093968 (https://www.ncbi.nlm.nih.gov/pubmed/15093968) Дата обращения: 28.02.2017.
J., Sabater A., Perez-Galvez B., Castellano М., Cervera G. Add-on gabapentin in the treatment of opiate withdrawal. Prog Neuropsychopharmacol Biol Psychiatry. 2004 May; 28(3): 599 - 601. URL: https://www.ncbi.nlm.nih.gov/pubmed/15093968 (https://www.ncbi.nlm.nih.gov/pubmed/15093968) Дата обращения: 28.02.2017.
62. Федеральное руководство по использованию лекарственных средств (формулярная система). Выпуск XVII. М.: Видокс; 2016. с. 313 - 322.
63. Loimer N., Presslich O., Lenz K., Pfersmann D., Schmid R., Fodor G., Aschauer G. "Induced detoxification treatment" of opiate dependent patients - a new therapy concept. Wien Klin Wochenschr. 1989 Jun 23; 101(13): 451 - 454.
64. Pinkofsky H.B., Hahn A.M., Campbell F.A., Rueda J., Daley D.C., Douaihy A.B. Reduction of opioid-withdrawal symptoms with quetiapine. Clin Psychiatry. 2005 Oct; 66(10): 1285 - 1288. URL: https://www.ncbi.nlm.nih.gov/ (https://www.ncbi.nlm.nih.gov/) Дата обращения: 28.02.2017.
65. Иванец Н.Н., Винникова М.А. Применение препарата клопиксол (зуклопентиксол) при лечении больных героиновой наркоманией: сравнительное исследование. Вопросы наркологии. 2002; 3: 13 - 19.
66. Lingford-Hughes A.R., Welch S., Peters L., Nutt D.J. et al. BAP updated guidelines: evidence-based guidelines for the pharmacological management of substance abuse, harmful use, addiction and comorbidity: recommendations from BAP. URL: http://joumals.sagepub.com/doi/full/10.1177/0269881112444324 (http://joumals.sagepub.com/doi/full/10.1177/0269881112444324) Дата обращения: 11.07.2018.
67. McRae-Clark A.L., Carter R.E., Killeen T.K. A placebo-controlled trial of buspirone for the treatment of marijuana dependence. Drug Alcohol Depend. 2009; 105: 132 - 138.
68. McRae-Clark A.L., Baker N.L., Gray K.M., Killeen T.K., Wagner A.M., Brady K.T., DeVane C.L., Norton J. Buspirone treatment of cannabis dependence: A randomized, placebo-controlled trial. Drug Alcohol Depend. 2015 Nov 1; 156: 29 - 37. doi: 10.1016/j.drugalcdep.2015.08.013.
69. Marshall K., Gowing L., Ali R., Le Foll B. Pharmacotherapies for cannabis dependence. Cochrane Database Syst Rev. 2014;(12):CD008940. doi: 10.1002/14651858.CD008940.pub2. URL: https://www.ncbi.nlm.nih.gov/pubmed/25515775 (https://www.ncbi.nlm.nih.gov/pubmed/25515775) Дата обращения: 11.07.2018.
70. Gold J.A., Rimal B., Nolan A. et al. A strategy of escalating doses of benzodiazepines and phenobarbital administration reduces the need for mechanical ventilation in delirium tremens. Crit Care Med. 2007; 35: 724 - 730. [PMC free article] URL: [PubMed] Дата обращения: 28.02.2017
71. Oude Voshaar R.,  J., Van Balkom A. Strategies for discontinuing long-term benzodiazepine use: metaanalysis. Br. J. Psychiatry. 2006; 189: 213 - 220.
J., Van Balkom A. Strategies for discontinuing long-term benzodiazepine use: metaanalysis. Br. J. Psychiatry. 2006; 189: 213 - 220.
72. Denis C, Fatseas M, Lavie E. Pharmacological interventions for benzodiazepine mono-dependence management in outpatient settings. Cochrane Database Syst Rev. 2006 Jul 19; (3): CD005194. URL: https://www.ncbi.nlm.nih.gov/pubmed/16856084 (https://www.ncbi.nlm.nih.gov/pubmed/16856084) Дата обращения: 13.07.2018.
73. Rickels K., Demartinis N., Rynn M., Mandos L. Pharmacologic strategies for discontinuing benzodiazepine treatment. Journal of Clinical Psychopharmacology. 1999; 19(6 Suppl 2): 12S - 16S. URL: [PubMed] Дата обращения: 28.02.2017.
74. Cocaine Use in America: Epidemiologic and Clinical Perspectives. NIDA Research Monograph No. 61. DHHS Publication No. ADM 85-1414. National Institute on Drug Abuse; 1985. 237 p. (p. 193 - 203). URL: https://archives.drugabuse.gov/sites/default/files/monograph61.pdf/ (https://archives.drugabuse.gov/sites/default/files/monograph61.pdf/) Дата обращения: 09/09/.2018.
75. Gerra G., Zaimovic A., Giusti F. Intravenous flumazenil versus oxazepam tapering in the treatment of benzodiazepine withdrawal: a randomized, placebo-controlled study. Addict Biol 2002; 7: 385 - 395.
76. Hood S., O'Neil G., Hulse G. The role of flumazenil in the treatment of benzodiazepine dependence: Physiological and psychological profiles. J Psychopharmacol. 2009; 23: 401 - 409.
77. Di Costanzo E., Rovea A. The prophylaxis of benzodiazepine withdrawal in the elderly: the effectiveness of carbamazepine. Double-blind study v. Placebo. Minerva Psychiatr. 1992; 33: 301 - 304.
78. Garcia-Borreguero D., Bronisch T., Yassouridis A. Treatment of benzodiazepine withdrawal symptoms with carbamazepine. Eur Arch Psychiatry Clin Neurosci. 1991; 241(3): 145 - 150. URL: https://www.ncbi.nlm.nih.gov/pubmed/1686406 (https://www.ncbi.nlm.nih.gov/pubmed/1686406) Дата обращения: 09.09.2018.
79. Schweizer E., Rickels K., Case W.G. Carbamazepine treatment in patients discontinuing long-term benzodiazepine therapy. Effects on withdrawal severity and outcome. Arch Gen Psychiatry. 1991; 8: 448 - 452.
80. Kaendler S.H., Volk S., Pflug B. Benzodiazepine withdrawal with carbamazepine. Nervenarzt. 1996 May; 67(5): 381 - 386.
81. Baandrup L., Ebdrup B.H., Rasmussen J.O., Lindschou J., Gluud C., Glenthoj B.Y. Pharmacological interventions for benzodiazepine discontinuation in chronic benzodiazepine users. Cochrane Database Syst Rev. 2018 Mar 15; 3: CD011481. doi: 10.1002/14651858.CD011481.pub2. URL: https://www.ncbi.nlm.nih.gov/pubmed/29543325 (https://www.ncbi.nlm.nih.gov/pubmed/29543325) Дата обращения: 20.06.2018.
82. Gilvarry E, Britton J (2009) Guidance for the pharmacological management of substance misuse among young people. National Treatment Agency for Substance Misuse. London: National Treatment Agency. URL: http://www.emcdda.europa.eu/ (http://www.emcdda.europa.eu/) Дата обращения: 11.07.2018.
83. Treatment for Stimulant Use Disorders. URL: https://www.ncbi.nlm.nih.gov/books/NBK64337/ (https://www.ncbi.nlm.nih.gov/books/NBK64337/) Дата обращения: 28.02.2017.
84. Srisurapanont M, Jarusuraisin N, Kittirattanapaiboon P (2001) Treatment for amphetamine dependence and abuse. Cochrane Database Syst Rev. URL: http://journals.sagepub.com/doi/full/10.1177/0269881112444324 (http://journals.sagepub.com/doi/full/10.1177/0269881112444324) Дата обращения: 28.02.2017.
85. Mancino M.J., McGaugh J., Chopra M.P., Guise J.B., Cargile C., Williams D.K., Thostenson J., Kosten T.R., Sanders N., Oliveto A. Clinical efficacy of sertraline alone and augmented with gabapentin in recently abstinent cocaine-dependent patients with depressive symptoms. J. Clin. Psychopharmacol. 2014 Apr; 34(2): 234 - 239. doi: 10.1097/JCP.0000000000000062.
86. Newton T.F., Roache J.D., De La Garza R 2nd, Fong T., Wallace C.L., Li S.H., Elkashef A., Chiang N., Kahn R. Bupropion reduces methamphetamine-induced subjective effects and cue-induced craving. Neuropsychopharmacology. 2006 Jul; 31(7): 1537 - 1544.
87. Pani P.P., Trogu E., Vecchi S., Amato L. (2011) Antidepressants for cocaine dependence and problematic cocaine use. Cochrane Database Syst Rev 12. URL: http://journals.sagepub.com/doi/full/10.1177/0269881112444324/ (http://journals.sagepub.com/doi/full/10.1177/0269881112444324/) Дата обращения: 28.02.2017
88.  C., Castells X., Torrens M.,
C., Castells X., Torrens M.,  D., Farre M. Efficacy of psychostimulant drugs for amphetamine abuse or dependence. Cochrane Database Syst Rev. 2013 Sep 2; (9): CD009695. doi: 10.1002/14651858.CD009695.pub2.
D., Farre M. Efficacy of psychostimulant drugs for amphetamine abuse or dependence. Cochrane Database Syst Rev. 2013 Sep 2; (9): CD009695. doi: 10.1002/14651858.CD009695.pub2.
URL: https://www.ncbi.nlm.nih.gov/pubmed/ (https://www.ncbi.nlm.nih.gov/pubmed/) Дата обращения: 13.07.2018.
89. Винникова М.А., Ежкова Е.В., Булатова Р.А. Терапевтические стратегии модификационной профилактики при синдроме зависимости, вызванном сочетанным употреблением ПАВ: обзор литературных данных. Профилактическая медицина. 2018; 21(2): 61 - 67. DOI:10.17116/profmed201821261-67.
90. O'Farrell, T.J., Clements K. Review of outcome research on marital and family therapy in treatment of alcoholism J Marital Fam Ther. 2012; 38(1): 122 - 144.
91. McCrady B.S. Treating alcohol problems with couple therapy. Journal of Clinical Psychology. 2012; 68(5): 514 - 525.
92. Powers, M.B. Vedel E. Emmelkamp P.M.G. Behavioral couples therapy (BCT) for alcohol and drug use disorders: A metaanalysis. Clinical Psychology Review. 2008; 28(6): 952 - 62.
93. Ruff S., McComb J.L., Coker C.J., Sprenkle D.H. Behavioral couples therapy for the treatment of substance abuse: a substantive and methodological review of O'Tarrell, Fals-Stewart, and colleagues" program of research. Fam Process. 2010 Dec; 49(4): 439 - 56. doi: 10.1111/j.1545-5300.2010.01333.x.
94. Schumm J.A., O'Farrell T.J., Kahler C.W., Murphy M.M., Muchowski P. A randomized clinical trial of behavioral couples therapy versus individually based treatment for women with alcohol dependence. Journal of Consulting and Clinical Psychology. 2014; 82(6): 993 - 1004. doi:10.1037/a0037497.
95. Meis L. A., Griffin J.M., Greer N., Jensen A.C., MacDonald R., Carlyle M., Wilt T.J. Couple and family involvement in adult mental health treatment: A systematic review. Clinical Psychology Review. 2013; 33(2): 275 - 286. doi:10.1016/j.cpr.2012.12.003.
96. Horigian V.E., Anderson A.R., Szapocznik J. (). Family-Based Treatments for Adolescent Substance Use. Child and Adolescent Psychiatric Clinics of North America.2016; 25(4): 603 - 628. doi:10.1016/j.chc.2016.06.001.
97. Van der Stouwe T., Asscher J.J., Stams G. J. J. M., Dekovic M., van der Laan P. H. The effectiveness of Multisystemic Therapy (MST): A meta-analysis. Clinical Psychology Review, 2014; 34(6): 468 - 481. doi:10.1016/j.cpr.2014.06.006.
98. Baldwin S.A., Christian S., Berkeljon A., Shadish W. R. The Effects of Family Therapies for Adolescent Delinquency and Substance Abuse: A Meta-analysis. Journal of Marital and Family Therapy. 2011; 38(1): 281 - 304. doi:10.1111/j.1752-0606.2011.00248.x.
Приложение А1
СОСТАВ РАБОЧЕЙ ГРУППЫ
Председатель - Брюн Евгений Алексеевич, д.м.н., профессор.
Секретарь - Поплевченков Константин Николаевич, к.м.н.
Состав рабочей группы:
Агибалова Татьяна Васильевна, д.м.н.
Бедина Инесса Александровна., к.м.н.
Бузик Олег Жанович, д.м.н.
Винникова Мария Алексеевна, д.м.н., проф.
Кошкина Евгения Анатольевна, д.м.н., проф.
Михайлов Михаил Альбертович, к.м.н.
Надеждин Алексей Валентинович, к.м.н.
Тетенова Елена Юрьевна, к.м.н.
Авторы:
1. Агибалова Татьяна Васильевна, доктор медицинских наук. Ассоциация наркологов России (Профессиональное сообщество врачей-наркологов). Национальное наркологическое общество. ЕАТА (Европейская ассоциация транзактного анализа).
2. Винникова Мария Алексеевна, доктор медицинских наук, профессор. Ассоциация наркологов России (Профессиональное сообщество врачей-наркологов). Национальное наркологическое общество.
3. Ненастьева Анна Юрьевна, кандидат медицинских наук. Национальное наркологическое общество. Российское общество психиатров.
4. Петухов Алексей Евгеньевич, кандидат фармацевтических наук. Федерация лабораторной медицины. Российская наркологическая лига.
5. Титков Максим Сергеевич, кандидат медицинских наук. Национальное наркологическое общество
6. Уткин Сергей Ионович, кандидат медицинских наук. Российское общество психиатров. Федерация анестезиологов и реаниматологов.
Конфликт интересов: нет
Все члены рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов, о которых необходимо сообщить.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория данных клинических рекомендаций:
1. Врач психиатр-нарколог.
2. Врач-психиатр-нарколог участковый.
3. Врач психиатр-подростковый.
4. Врач психиатр.
5. Врач-психиатр участковый.
6. Врач психотерапевт.
7. Медицинский психолог.
При разработке настоящих клинических рекомендаций использованы следующие информационные средства:
- "Требования к оформлению клинических рекомендаций для размещения в Рубрикаторе". Письмо Первого заместителя министра здравоохранения И.Н. Каграманяна от 01 сентября 2016 г. N 17-4/10/1-4939.
- Анализ источников научной литературы и других данных, а также интернет-ресурсов за последние 10 лет:
- отечественные: руководства для врачей, научные публикации в периодических изданиях, научная электронная библиотека e-library, Государственный Реестр Лекарственных Средств, Регистр лекарственных средств, Федеральная служба государственной статистики Российской Федерации;
- зарубежные: Cochrane Library, Medline, MedScape, PubMed, National Institute on Alcohol Abuse and Alcoholism (NIAAA), Substance Abuse and Mental Health Services Administration (SAMSHA), European Monitoring Centre for Drugs and Drug Addiction (EMCDDA);
- Регламентирующие документы Правительства Российской Федерации и Министерства здравоохранения Российской Федерации.
При разработке настоящих клинических рекомендаций использовалась рейтинговые схемы для оценки уровня достоверности доказательств (1, 2, 3, 4, 5) (Приложение 1, 2) и уровня убедительности рекомендаций (А, В, С) (Приложение 3, 4)
Уровень GPP - сложившаяся клиническая практика.
Уровень GPP используется в случае, если для данного тезиса-рекомендации отсутствуют доказательства, полученные на основании результатов систематического поиска и отбора КИ.
Уровень GPP используется для тезис-рекомендаций, относящихся к: сбору жалоб и анамнеза пациента; физикальному осмотру пациента; организации медицинской помощи (медицинского процесса); а также для медицинских вмешательств, для оценки эффективности и/или безопасности которых в силу этических причин (например, экстренная терапия и др.) невозможно выполнение КИ более высокого дизайна, чем несравнительные исследования, описания клинических случаев или серии случаев.
Приложение А2.1
РЕЙТИНГОВАЯ СХЕМА
ОЦЕНКИ УРОВНЯ ДОСТОВЕРНОСТИ ДОКАЗАТЕЛЬСТВ
ДЛЯ ДИАГНОСТИЧЕСКИХ ВМЕШАТЕЛЬСТВ
|
УДД
|
Иерархия дизайнов клинических исследований по убыванию уровня достоверности доказательств от 1 до 5
|
|
1
|
Систематические обзоры исследований с контролем референсным методом
|
|
2
|
Отдельные исследования с контролем референсным методом
|
|
3
|
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода
|
|
4
|
Несравнительные исследования, описание клинического случая
|
|
5
|
Имеется лишь обоснование механизма действия или мнение экспертов
|
Примечание:
УДД - уровень достоверности доказательств.
Приложение А2.2
РЕЙТИНГОВАЯ СХЕМА
ОЦЕНКИ УРОВНЯ ДОСТОВЕРНОСТИ ДОКАЗАТЕЛЬСТВ ДЛЯ ЛЕЧЕБНЫХ,
РЕАБИЛИТАЦИОННЫХ, ПРОФИЛАКТИЧЕСКИХ ВМЕШАТЕЛЬСТВ
|
УДД
|
Иерархия дизайнов клинических исследований по убыванию уровня достоверности доказательств от 1 до 5
|
|
1
|
Систематический обзор рандомизированных клинических исследований (РКИ) с применением мета-анализа
|
|
2
|
Отдельные РКИ и систематические обзоры исследований любого дизайна (помимо РКИ) с применением мега-анализа
|
|
3
|
Нерандомизированные сравнительные исследования, в том числе когортные исследования
|
|
4
|
Несравнительные исследования, описание клинического случая или серии случаев, исследования "случай-контроль"
|
|
5
|
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
|
Примечание:
УДД - уровень достоверности доказательств.
РКИ - рандомизированное клиническое исследование.
Приложение А2.3
РЕЙТИНГОВАЯ СХЕМА
ОЦЕНКИ УРОВНЯ УБЕДИТЕЛЬНОСТИ РЕКОМЕНДАЦИЙ
ДЛЯ ДИАГНОСТИЧЕСКИХ ВМЕШАТЕЛЬСТВ
|
УУР
|
Описание
|
|
A
|
Однозначная (сильная) рекомендация (все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Неоднозначная (условная) рекомендация (не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Низкая (слабая) рекомендация - отсутствие доказательств надлежащего качества (все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Примечание:
УУР - уровень убедительности рекомендаций.
Приложение А2.4
РЕЙТИНГОВАЯ СХЕМА
ОЦЕНКИ УРОВНЯ УБЕДИТЕЛЬНОСТИ РЕКОМЕНДАЦИЙ ДЛЯ ЛЕЧЕБНЫХ,
РЕАБИЛИТАЦИОННЫХ, ПРОФИЛАКТИЧЕСКИХ ВМЕШАТЕЛЬСТВ
|
УУР
|
Описание
|
|
A
|
Однозначная (сильная) рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
|
|
B
|
Неоднозначная (условная) рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
|
|
C
|
Низкая (слабая) рекомендация - отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
|
Примечание:
УУР - уровень убедительности рекомендаций.
Приложение А3
СВЯЗАННЫЕ ДОКУМЕНТЫ
Приложение Б
АЛГОРИТМЫ ВЕДЕНИЯ ПАЦИЕНТА
Алгоритм диагностики синдрома отмены
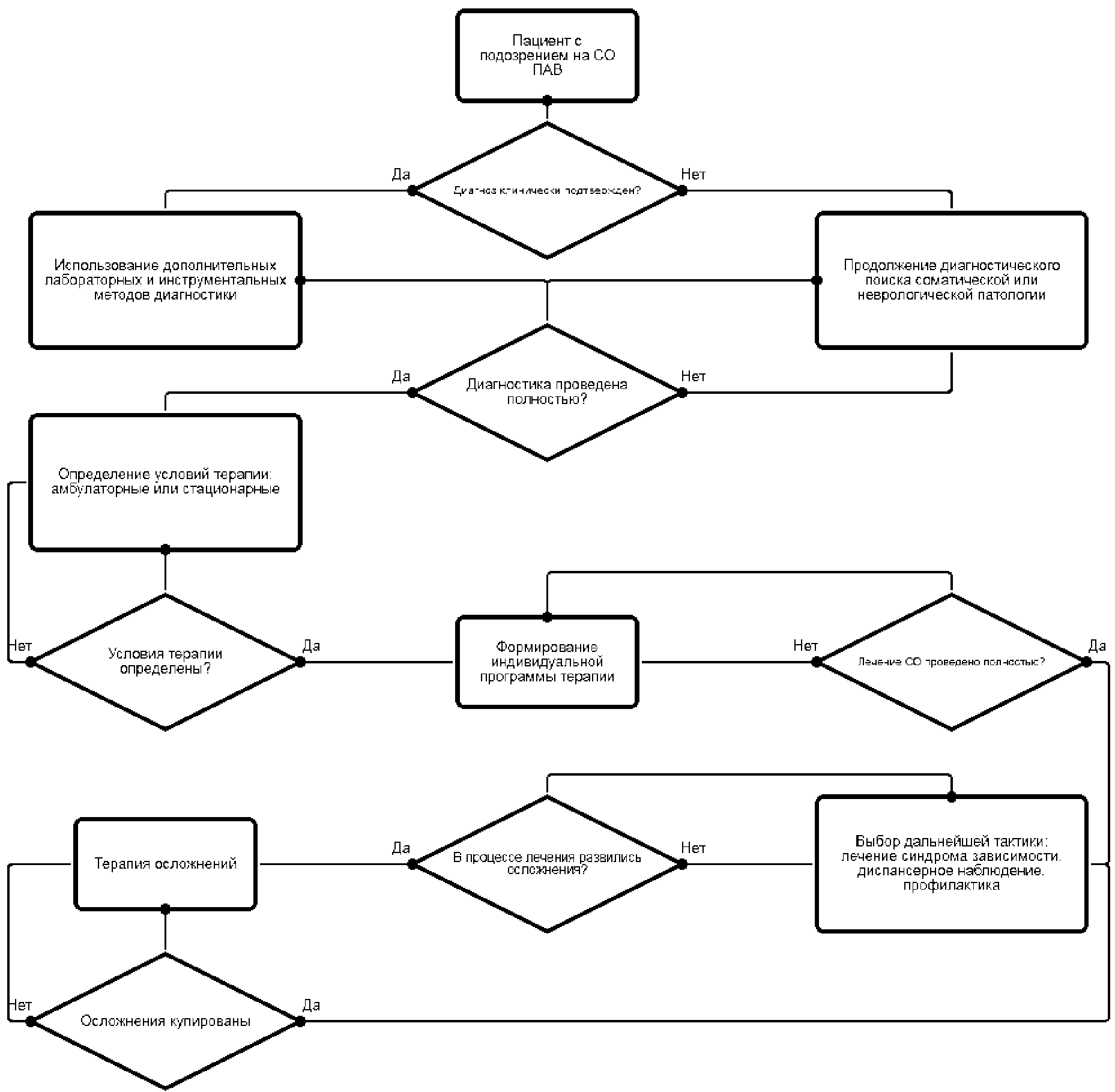
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТОВ
F11.3 СИНДРОМ ОТМЕНЫ ОПИОИДОВ. ОПИЙНЫЙ АБСТИНЕНТНЫЙ СИНДРОМ.
Возникновение синдрома отмены ("ломки") при опийной наркомании свидетельствует о формировании качественно нового этапа заболевания - второй (средней) стадии зависимости от опиоидов. Синдром отмены формируется примерно через 2 недели - 1,5 месяца после начала систематического употребления опиоидов.
Синдром отмены опиоидов ("ломка") возникает после прекращения длительного интенсивного употребления наркотика или резкого уменьшения его дозы. Развивается через 6 - 24 часа после последнего употребления наркотика. Время развития синдрома отмены зависит от вида употребляемого наркотика (например, при злоупотреблении метадоном отмечается его отсроченный характер), а также от различных удлиняющих психотропное действие опиоидов примесей (бензодиазепинов, антигистаминных препаратов).
Основные клинические проявления синдрома отмены опиоидов включают в себя вегетативные, болевые и психопатологические расстройства. К вегетативным проявлениям относятся: зевота, слезотечение, насморк и заложенность носа с частым чиханием, диарея, расширение зрачков, повышение температуры тела, учащенное сердцебиение, повышение артериального давления, потливость, озноб, пилоэрекция ("гусиная кожа"). На начальных сроках наркотизации, когда болевые расстройства могут быть выражены слабо или отсутствуют, пациенты нередко принимают данное состояние за грипп или ОРЗ. Нередко первым проявлением синдрома отмены являются психопатологические расстройства: появляется напряженность, чувство дискомфорта, тревога, раздражительность, угрюмость, сопровождающиеся общим недомоганием, физической слабостью. Нарушения сна, вплоть до полной бессонницы, появляются в течение первых суток после прекращения употребления наркотиков и отличаются продолжительностью и устойчивостью к лечению.
В структуре синдрома отмены, вызванной злоупотреблением опиоидов, болевые расстройства являются одними из важнейших и относятся к категории наиболее тяжело переживаемых пациентом расстройств. Отсюда название абстиненции на сленге наркоманов - "ломка". На вторые сутки после последнего приема наркотиков появляются мышечные и суставные боли в конечностях, спине, а иногда во всем теле выкручивающего характера. Часто бывают боли в животе, диарея. Болевые расстройства субъективно крайне тягостны и мучительны для больных. При этом необходимо отметить склонность зависимых от опиоидов к преувеличению тяжести своего состояния. Влечение к наркотику осознанное, часто непреодолимое, как правило, не скрывается пациентами. Нередко в этом состоянии употребляющие опиоиды становятся неуправляемыми, агрессивными. На состояние отмены опиоидов приходится наибольшее число правонарушений зависимыми от наркотиков, возрастает опасность самоубийства. Максимальной выраженности расстройства синдрома отмены при употреблении опиоидов достигают на 2 - 3 сутки, а их продолжительность зависит от вида наркотика, длительности заболевания, проводимого лечения. Острые расстройства при героиновой зависимости в условиях лечения редко продолжаются более 7 - 10 дней.
Лечение
Принципы и подходы к лечению при всех видах зависимости одинаковы. Лечение больных наркоманией должно быть длительным, комплексным. Оно включает в себя несколько этапов.
1-й этап: лечение "ломки". На этом этапе выводят наркотик из организма, облегчают боль. Сейчас существует множество хороших методов и препаратов, которые позволяют облегчить это страдание. Перечисление их заняло бы слишком много места. Главная задача этого этапа - облегчить боль, снять страдание, восстановить жизненно важные функции организма.
2-й этап: лечение "тяги", поддерживающая терапия.
Здесь препараты уже специфические, которые снимают напряжение, улучшают настроение, выравнивают сон. Также важное внимание уделяется состоянию, и, по необходимости, лечению внутренних органов, особенно печени, почек, головного мозга.
На этом этапе проводится психотерапия, в работу включаются психологи. 1-й и 2-й этапы проходят в стационаре.
Главная задача 3-го этапа - адаптировать пациента в нормальной жизни, он называется реабилитационный. Это очень длительный этап лечения, чем он дольше, тем лучше результат.
Профилактика
Для больных опийной наркоманией существуют различные специфические методы терапии, например, использование блокаторов опиоидных рецепторов - при нахождении в организме их действие уберегает больного от действия наркотиков; активно разрабатываются методы и лекарства, направленные на лечение гепатита C и других последствий наркомании. Применение каждого из перечисленных методов должно быть строго индивидуально и проводиться под наблюдением врачей.
F12.3 СИНДРОМ ОТМЕНЫ КАННАБИНОИДОВ.
Абстинентный синдром при зависимости от каннабиноидов формируется длительно, срок его формирования крайне индивидуальны, в среднем, через 2 - 3 года регулярного злоупотребления. В абстинентном синдроме преобладают депрессивные нарушения: усталость, разбитость, раздражительность, злобность, дисфория, бессонница. Могут наблюдаться тремор, потливость, тошнота, рвота. В отдельных случаях в абстинентном синдроме преобладает интенсивная тревога - состояние, схожее с паническими реакциями. Возможны суицидальные попытки. Иногда отмечаются тяжело переживаетмые, странные (сенестопатические) ощущения в разных частях тела: сдавление груди, затрудненное дыхание, неприятные ощущения в области сердца, чувство сжатия и сдавления головы в височной области. Выраженность влечения к наркотику весьма вариабельна. Своего пика абстинентные расстройства достигают на 3 - 5 сутки, их продолжительность в среднем - 7 дней.
Лечение
Принципы и подходы к лечению при всех видах зависимости одинаковы (см. синдром отмены опиоидов). Специфического лечения синдром отмены каннабиноидов нет.
Профилактика
Следует понимать, что хроническое (постоянное) употребление каннабиноидов (марихуаны, гашиша) приводит к изменениям личности больных. У больных развивается амотивационный синдром, в структуре которого преобладает апатия, анергия, пассивность, отсутствие притязаний. Пациенты пренебрегают всеми своими обязанностями. Хроническая интоксикация препаратами конопли приводит к нарушениям памяти, внимания, а также может явиться пусковым механизмом дебюта шизофрении у лиц с соответствующей предрасположенностью. При массивном употреблении каннабиноидов может возникать психотическое расстройство с поздним (отставленным) дебютом ("флэшбек"), напоминающее подобные состояния при злоупотреблении галлюциногенами. Таким образом, основным средством профилактики является поддержание здорового, трезвого образа жизни.
F13.3 СИНДРОМ ОТМЕНЫ СЕДАТИВНЫХ ИЛИ СНОТВОРНЫХ ВЕЩЕСТВ
Сроки наступления синдрома отмены зависят от периода полувыведения принимаемого лекарственного препарата, как правило возникают на 1 - 2 день после последнего приема и достигают максимума на 1 - 2 сутки, а, в отдельных случаях, до 1 недели. Клинически проявляется следующими симптомами: тремор пальцев вытянутых рук, кончика языка или век, тошнота или рвота, тахикардия, ортостатическая гипотония, головные боли, бессонница, психомоторное беспокойство, большие судорожные припадки, транзиторные зрительные, осязательные или слуховые галлюцинации (иллюзии), бредовая настороженность.
Лечение
При лечении абстинентного синдрома рекомендуется постепенное снижение дозы вещества. Лечение необходимо проводить в стационарных условиях.
Профилактика
Хроническая интоксикация седативными и снотворными средствами приводит к выраженным и стойким изменениям со стороны соматической, неврологической и психической сфер. Отмечается повышенная утомляемость, истощаемость внимания, снижение сообразительности. По мере прогрессирования болезни появляется медлительность, замкнутость, подавленность, что нередко сменяется вспышками злобы и гнева. Выявляются нарушения глотания, ухудшение почерка, вялая мимика, мышечная гипотония, нарушения тонких движений и походки. Прогрессирующее снижение интеллекта приводит к утрате трудоспособности больного и инвалидности. Весьма высока частота смертельных исходов. Причиной смерти служат самоубийства, несчастные случаи в состоянии опьянения, передозировки. Во избежание развития выше перечисленных осложнений, рекомендовано обращение к врачу в любых случаях появления проблем настроения и сна. Категорически опасно заниматься самолечением.
F14.3 СИНДРОМ ОТМЕНЫ КОКАИНА,
F15.3 СИНДРОМ ОТМЕНЫ ДРУГИХ СТИМУЛЯТОРОВ, ВКЛЮЧАЯ КОФЕИН
Синдром отмены возникает через 12 - 24 часа после последнего употребления амфетаминов, максимальной выраженности расстройства достигают на 2 - 4 сутки. Абстинентный синдром характеризуется усталостью, ощущением разбитости, заторможенностью, нарушениями сна - бессонницей или сонливостью с кошмарными сновидениями. Нередко отмечаются раздражительность, злобность, истерические реакции со склонностью к аутоагрессии. Выраженное астеническое или астено-депрессивное состояние может сопровождаться идеями самообвинения и суицидальными попытками. Могут отмечаться отдельные идеи отношения, преследования. Острые проявления абстинентных расстройств исчезают в течение 7 - 14 дней, в тяжелых случаях проявления сохраняются до 1 месяца. При отнятии стимуляторов могут наблюдаться психозы в виде помрачения сознания по типу делириозного с речевым и двигательным возбуждением хронические амфетаминовые психозы, продолжающиеся от 2 - 3 недель до нескольких месяцев.
Вслед за этим периодом, как правило, начинается период хронической дисфории и ангедонии. Больные отчетливо ощущают неполноценность собственного существования, безысходность, испытывают чувство внутренней пустоты, безрадостность и т.д. При этом влечение к наркотику проявляется стойкой ангедонической депрессией, часто влечение принимает непреодолимый характер, что приводит к рецидиву.
Лечение
Специфических средств терапии не существует. Принципы и подходы к лечению при всех видах зависимости одинаковы (см. синдром отмены опиоидов). Основная задача терапии - предупредить развитие психических осложнений.
Профилактика
Все психостимуляторы, исключая кофеин, чрезвычайно наркогенны. Наркогенность (способность вызывать зависимость) зависит от многих факторов: вида наркотика, способа его введения, дозы и др. Для данной формы наркомании характерно быстрое развитие психической зависимости, развитие психотических нарушений при приеме больших доз препаратов в виде галлюцинаций и бредовых идей, а также быстрое формирование слабоумия. Таким образом, основным средством профилактики является поддержание здорового, трезвого образа жизни.
F16.3 СИНДРОМ ОТМЕНЫ ГАЛЛЮЦИНОГЕНОВ
Абстинентный синдром при употреблении ЛСД, псилоцибина и мескалина, кетамина, фенциклидина, по данным большинства исследователей, отсутствует. В отдельных случаях при длительном систематическом употреблении могут встречаться нарушения сна, вегетативная дисфункция, общий дискомфорт продолжительностью 7 - 10 дней, переходящие в выраженное астено-апатическое состояние.
Лечение
Специфической терапии не существует. Принципы и подходы к лечению при всех видах зависимости одинаковы (см. синдром отмены опиоидов).
Профилактика
Последствия длительного употребления галлюциногенов проявляются психической тупостью ("психической глухотой"), наблюдающейся по истечении многих дней после их приема, психозами с богатой симптоматикой, продолжающимися и после выведения препарата из организма.
Рецидивы галлюцинаций, по разным данным, возникают у 16 - 57% потребителей ЛСД в результате воздействия провоцирующих факторов: стрессовых ситуаций, приема другого ПАВ или соматического заболевания.
В ряде случаев галлюциногены провоцируют развитие психического заболевания - шизофрении. Предугадать, диагностировать вероятность или предупредить развитие эндогенного заболевания невозможно. В связи с этим даже единичный прием галлюциногенов может быть опасен. Учитывая непредсказуемость последствий употребления галлюциногенов, наилучшим средством профилактики является поддержание здорового, трезвого образа жизни.
F18.3 СИНДРОМ ОТМЕНЫ ЛЕТУЧИХ РАСТВОРИТЕЛЕЙ
Синдром отмены ингалянтов возникает через 6 - 12 месяцев после начала злоупотребления и через 1 - 3 суток после последнего употребления. Проявляется в виде вялости, разбитости, неприятных ощущений в теле, головной боли, потливости, головокружения, тошноты, плохого сна, пониженного настроения и раздражительности. Эти проявления похожи на проявления вегетососудистой дистонии. На 5 - 7 сутки присоединяется депрессивная симптоматика. На 4 - 5 сутки синдром отмены может осложниться развитием острого психоза, длящегося от нескольких часов до 3 суток и представляющего собой делирий с иллюзиями, истинными зрительными и слуховыми галлюцинациями. В целом, продолжительность синдрома отмены в условиях лечения около 2-х недель.
Лечение
По терапевтическим подходам схоже с лечением алкогольного абстинентного синдрома.
Профилактика
При хроническом злоупотреблении ингалянтами развивается токсическая энцефалопатия с признаками мозговой атрофии и хроническими двигательными нарушениями. Появляются выраженные нарушения центральной, периферической и вегетативной нервной системы. Нередко встречается полинейропатия, проявляющаяся в снижении чувствительности, ослаблении рефлексов, парестезиях кистей и стоп, онемением по типу "носков" и "перчаток", сочетающаяся с мышечной гипотрофией и акрогипергидрозом. Токсическое поражение нервных окончаний в головном мозге приводит к ухудшению зрения вплоть до слепоты, а также к звону в ушах и ослаблению слуха. Также возникают нарушения сердечно-сосудистой, дыхательной, мочевыделительной системы.
Изменения личности тяжелые, быстро нарастают, развивается психоорганический синдром с интеллектуальным снижением, психопатоподобным поведением.
Учитывая фактор возраста (пристрастие формируется, в основном, у лиц младшего и подросткового возраста), меры первичной профилактики, идущей от семьи, являются важнейшими в предупреждения развития зависимости.
Приложение Г
КЛИНИЧЕСКИЕ ПРИЗНАКИ
СИНДРОМА ОТМЕНЫ ПРИ УПОТРЕБЛЕНИИ РАЗЛИЧНЫХ ВИДОВ ПАВ
Приложение Г1
ОСНОВНЫЕ КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
АБСТИНЕНТНОГО СИНДРОМА ВСЛЕДСТВИЕ УПОТРЕБЛЕНИЯ ОПИОИДОВ
(ОПИЙНОГО АБСТИНЕНТНОГО СИНДРОМА)
|
Категория
|
Проявления
|
|
Психопатологические нарушения
|
Патологическое влечение к наркотику, которое проявляется:
- аффективными нарушениями: тревога, напряженность, раздражительность, дисфория, сопровождающиеся общим недомоганием, чувством дискомфорта, расстройства сна, наиболее тягостным из которых является бессонница, отличающаяся продолжительностью и устойчивостью к проводимой терапии;
- поведенческими нарушениями: агрессия, психомоторное возбуждение;
- собственно идеаторными расстройствами (мысли о наркотике, непреодолимое желание употребить его и пр.)
|
|
Вегетативные нарушения
|
- мидриаз (в интоксикации - миоз);
- зевота, слезотечение, ринорея с частым чиханием, диарея, повышенная потливость, озноб, пилоэрекция ("гусиная кожа");
- повышение температуры тела, учащение сердцебиения, артериальная гипертензия.
|
|
Болевой симптомокомплекс
|
"Ломка" на жаргоне наркоманов.
На вторые сутки после последнего приема наркотиков появляются мышечные и суставные боли в конечностях, спине, иногда распространяющиеся по всему телу, описываемые больными как "выкручивающие". Нередко имеют место боли в животе. Болезненные расстройства крайне тягостны и мучительны, могут принимать характер сенестопатий.
|
|
Неврологические нарушения
|
- мелкоразмашистый горизонтальный нистагм;
- пирамидные и мозжечковые нарушения;
- мышечная гипотония;
- угнетение сухожильных рефлексов.
|
Приложение Г2
ОСНОВНЫЕ КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
АБСТИНЕНТНОГО СИНДРОМА ВСЛЕДСТВИЕ
УПОТРЕБЛЕНИЯ КАННАБИНОИДОВ
|
Категория
|
Проявления
|
|
Психопатологические нарушения
|
Патологическое влечение к наркотику, которое проявляется:
- аффективными нарушениями: тревога, сопровождающаяся мышечной слабостью, недомоганием, чувством дискомфорта, расстройства сна;
- собственно идеаторными расстройствами (мысли о наркотике, непреодолимое желание употребить его и пр.)
- поведенческие нарушения (агрессия, негативизм к лечению) проявляются при тяжелом течении абстинентного синдрома.
|
|
Вегетативные нарушения
|
- умеренный миоз (в интоксикации - мидриаз);
- зевота, озноб, мышечная слабость;
- учащение сердцебиения и дыхания, артериальная гипертензия.
|
|
Неврологические нарушения
|
- мелкий тремор;
- гиперрефлексия, возможны фибриллярные подергивания.
|
|
Сенестопатии
|
- характерны для тяжелого течения абстинентного синдрома:
вычурные, своеобразные ощущения тяжести и давления в груди, сжатия и сдавливания головы; на коже и под кожей ощущение жжения, неприятного покалывания, дергания, ползания.
|
Приложение Г3
ОСНОВНЫЕ КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
АБСТИНЕНТНОГО СИНДРОМА ВСЛЕДСТВИЕ УПОТРЕБЛЕНИЯ СЕДАТИВНЫХ
ИЛИ СНОТВОРНЫХ СРЕДСТВ
|
Категория
|
Проявления
|
|
Психопатологические нарушения
|
- влечение к приему препаратов отличается стойкостью, проявляется аффективной симптоматикой депрессивного спектра и собственно идеаторными расстройствами (мысли о наркотике, непреодолимое желание употребить его и пр.);
- тревога, страх;
- дисфория, раздражительность, напряженность;
- чувство дискомфорта;
- деперсонализация;
- расстройства сна
|
|
Соматовегетативные нарушения
|
- снижение аппетита;
- зевота, озноб, мышечная слабость;
- тахикардия, артериальная гипертензия;
- ортостатическая гипотония;
- потливость;
- бледность кожных покровов,
- потливость,
- боли в желудке, рвота,
- летучие боли в крупных суставах
|
|
Неврологические нарушения
|
- мидриаз (в интоксикации - миоз);
- нистагм;
- мелкий тремор;
- мышечное напряжение;
- судороги икроножных мышц;
- гиперрефлексия
|
|
Характерные осложнения
|
- судорожные припадки
- психоз делириозной структуры
|
Приложение Г4
ОСНОВНЫЕ КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
АБСТИНЕНТНОГО СИНДРОМА ВСЛЕДСТВИЕ УПОТРЕБЛЕНИЯ
ПСИХОСТИМУЛЯТОРОВ (КОКАИН И ДРУГИЕ ПСИХОСТИМУЛЯТОРЫ)
|
Категория
|
Проявления
|
|
Психопатологические нарушения
|
- влечение к приему препаратов отличается стойкостью, проявляется, как правило, дисфорией.
- дисфория, раздражительность, напряженность;
- идеи отношения, преследования;
- чувство дискомфорта;
- тревога, страх;
- суицидальные мысли;
- расстройства сна (бессонница или сонливость);
- повышенный аппетит;
- астенический симптомокомплекс (усталость, разбитость, заторможенность, др.) на выходе из абстинентного синдрома
|
|
Неврологические нарушения
|
- умеренный миоз (в интоксикации - мидриаз);
- нарушение координации движений,
- нистагм;
- сниженный мышечный тонус;
- гиперрефлексия
|
Приложение Г5
ОСНОВНЫЕ КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
АБСТИНЕНТНОГО СИНДРОМА ВСЛЕДСТВИЕ УПОТРЕБЛЕНИЯ ИНГАЛЯНТОВ
|
Категория
|
Проявления
|
|
Психопатологические нарушения
|
- влечение к приему препаратов проявляется чаще идеаторными расстройствами (мысли о наркотике, непреодолимое желание употребить его и пр.);
- дисфория, раздражительность, напряженность;
- расстройства сна
|
|
Соматовегетативные нарушения
|
- снижение аппетита;
- бледность кожных покровов,
- летучие боли в крупных суставах
|
|
Неврологические нарушения
|
- миоз (в интоксикации - мидриаз);
- нистагм;
- мышечное напряжение;
- судороги икроножных мышц;
- гиперрефлексия
|
Приложение Д
КЛИНИЧЕСКИЕ КРИТЕРИИ
ДЛЯ БЫСТРОЙ ПЕРВИЧНОЙ ДИАГНОСТИКИ, ВАРИАНТЫ СКРИНИНГА,
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Приложение Д1
ДИФФЕРЕНЦИАЛЬНО-ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ
АБСТИНЕНТНОГО СИНДРОМА ПО РЕАКЦИИ ЗРАЧКА
|
ПАВ
|
Реакция зрачка
|
|
Опий
|
Мидриаз
Боль (ломка)
|
|
Каннабис
|
Миоз умеренный
Инъецированность склер
|
|
Седативные или снотворные средства
|
Мидриаз
Нистагм
|
|
Кокаин и другие стимуляторы
|
Умеренный миоз
|
|
Ингалянгы
|
Миоз
|
Примечание: ПАВ - психоактивное вещество
Приложение Д2
ВОЗМОЖНЫЕ ВАРИАНТЫ СКРИНИНГА ПРИ АБСТИНЕНТНОМ СИНДРОМЕ
|
ПАВ
|
Скрининг
|
|
Опий
|
Специфический антагонист - налоксон
|
|
Каннабис
|
Биологическое тестирование
|
|
Седативные или снотворные средства
|
Специфический антагонист при БЗД - флюмазенил
|
|
Кокаин и другие стимуляторы
|
Биологическое тестирование
|
|
Ингалянты
|
Отсутствует
|
Примечание: ПАВ - психоактивное вещество
Приложение Д3
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
|
ПАВ
|
Состояния для дифференциальной диагностики
|
|
Опий
|
- СО вследствие употребления других ПАВ (особенно алкоголь, седативные или снотворные средства);
- Интоксикация холинолитическими препаратами;
- ОРЗ, грипп;
- Острые или обострения хронических соматических (панкреатит, язвенная болезнь, гастроэнтериты) или неврологических (вертеброгенный болевой синдром) заболеваний;
- Психические расстройства, проявляющиеся тревогой (тревожное расстройство, обсессивно-компульсивное расстройство, паническая атака)
- др.
|
|
Каннабис
|
- Психические расстройства, проявляющиеся тревогой (тревожное расстройство, обсессивно-компульсивное расстройство, паническая атака)
- Пароксизмальная тахикардия
- Эндогенные психозы (в структуре шизофрении)
- Злоупотребление галлюциногенами
- СО психостимуляторов (особенно синтетических)
- Органический амнестический синдром, органическое бредовое расстройство, расстройство личности и поведения органического генеза.
- др.
|
|
Седативные или снотворные средства
|
- СО вследствие употребления других ПАВ (особенно алкоголь, опиоиды, ингалянты);
- болезни мозжечка;
- судорожные расстройства;
- отравление ангихолинэргическими или симпатомиметическими веществами;
- гипертиреоидизм.
|
|
Кокаин
|
- СО вследствие употребления других психостимуляторов, седативных или снотворных средств;
- Интоксикация галлюциногенами;
- Биполярное аффективное расстройство;
- Психические расстройства, проявляющиеся тревогой (тревожное расстройство, обсессивно-компульсивное расстройство, паническая атака)
- Гипертиреоидизм;
- Шизоаффективное расстройство;
- Шизофрения
|
|
Психостимуляторы
|
- СО вследствие употребления алкоголя, седативных или снотворных средств, кокаина;
- Интоксикация галлюциногенами;
- Биполярное аффективное расстройство;
- Психические расстройства, проявляющиеся тревогой (тревожное расстройство, обсессивно-компульсивное расстройство, паническая атака)
- Шизоаффективное расстройство;
- Шизофрения;
- Гипертиреоидизм;
- Шизоаффективное расстройство.
|
|
Ингалянты
|
- СО вследствие употребления алкоголя, седативных или снотворных средств, синтетических каннабиноидов;
- Соматические, неврологические, метаболические, травматические, опухолевые заболевания, влияющие на деятельность мозга в целом.
|
Примечание:
ПАВ - психоактивное вещество
СО - синдром отмены
ОРЗ - острое респираторное заболевание
Приложение Е
АЛГОРИТМ ПРОВЕДЕНИЯ НАЛОКСОНОВОГО ТЕСТА
|
Составляющие алгоритма
|
Описание
|
|
Условия проведения теста
|
1. Кушетка или кровать
2. Возможность монкторирования АД, ЧСС, др.
3. Возможность при необходимости проведения ИВЛ
4. Наличие препаратов для купирования опийного абстинентного синдрома:
- Седативные
- Ненаркотические анальгетики
- Противорвотные
- Антигистаминные
- др.
|
|
Методика проведения теста
|
1. Осуществляется надежный венозный доступ
2. Подсоединяется монитор
3. Пациенту объясняется суть теста
4. Первое введение: налоксон в дозе 0,2 - 0,4 мг вводится внутривенно (в/в) в течение 30 - 45 секунд
5. Ведется наблюдение за пациентом в течение 5 минут, фиксируются АД, пульс, кожные реакции, диаметр зрачка, субъективные ощущения пациента.
6. Повторное введение: при отсутствии реакции на первое введение налоксона, препарат вводят повторно в/в в дозе 0,4 мг и продолжают наблюдение за пациентом в течение 15 - 30 минут.
7. Препарат предпочтительно вводить в/в, но если венозный доступ затруднен, то можно вводить препарат подкожно (п/к) или внутримышечно (в/м) в дозе 0,4 - 0,8 мг. В этом случае реакция оценивается в течение 15 - 20 минут.
|
|
Оценка теста
|
1. Тест считается отрицательным, если отсутствуют объективные и субъективные реакции на первое/повторное введение налоксона;
2. Тест считается положительным, если непосредственно после введения налоксона развиваются субъективные и объективные реакции. Обязательно подтверждение субъективных ощущений объективными данными.
|
Примечание:
АД - артериальное давление
ЧСС - частота сердечных сокращений
ИВЛ - искусственная вентиляция легких
Приложение Ж
АЛГОРИТМ НАРАНЖО
|
NN
|
Вопросы
|
Да
|
Нет
|
Неизвестно
|
|
1
|
Были ли ранее достоверные сообщения об этом НЯ?
|
+ 1
|
0
|
0
|
|
2
|
НЯ возникло после введения (приема) подозреваемого лекарства?
|
+ 2
|
- 1
|
0
|
|
3
|
Улучшилось ли состояние испытуемого (проявления НЯ) после прекращения приема препарата или после введения специфического антидота?
|
+ 1
|
0
|
0
|
|
4
|
Возобновилось ли НЯ после повторного введения препарата?
|
+ 2
|
- 1
|
0
|
|
5
|
Есть ли еще причины (кроме подозреваемого лекарства), которые могли вызвать НЯ?
|
- 1
|
+ 2
|
0
|
|
6
|
Было ли лекарство обнаружено в крови (или других жидкостях) в концентрациях, известных как токсические?
|
+ 1
|
0
|
0
|
|
7
|
Было ли НЯ более тяжелым после увеличения дозы и менее тяжелым после ее уменьшения?
|
+ 1
|
0
|
0
|
|
8
|
Отмечал ли испытуемый аналогичную реакцию на то же или подобное лекарство при прежних его приемах?
|
+ 1
|
0
|
0
|
|
9
|
Было ли НЯ подтверждено объективно?
|
+ 1
|
0
|
0
|
|
10
|
Отмечалось ли повторение НЯ после назначения плацебо?
|
- 1
|
+ 1
|
0
|
Примечание:
НЯ - нежелательное явление.
Приложение З
ВЗАИМОДЕЙСТВИЕ
НЕЙРОТРАНСМИТТЕРА С РЕЦЕПТОРОМ И ВЫЗЫВАЕМЫЕ
КЛИНИЧЕСКИЕ ЭФФЕКТЫ
|
Нейротрансмиттер
|
Рецептор
|
Клинические эффекты
|
|
Ацетилхолин
|
Никотиновые и мускариновые рецепторы
|
Координация, кратковременная память, когнитивные функции, REM-фаза сна
|
|
Дофамин
|
Дофаминовые
|
Познавательная деятельность, регуляция двигательной активности, рабочая память
|
|
ГАМК
|
ГАМК-рецепторы
|
Торможение активности коры, регуляция работы мозжечка, гиппокампа и лимбической системы
|
|
Норэпинефрин
|
 , ,  , , 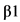 и и 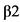 рецепторы рецепторы |
Поддержание сна, регуляция настроения
|
|
Эндорфины
|
 , ,  и и 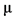 рецепторы рецепторы |
Анальгезия, эйфория, седация, угнетение дыхания, гипотермия
|
|
Серотонин
|
Серотониновые (5-HT) рецепторы
|
Засыпание, регуляция настроения, болевой чувствительности, тревоги, агрессии, поддержание внимания
|
|
Анандамид
|
Каннабиноидные рецепторы CB1, CB2, Дельта(9)-ТГК
|
Регуляция пищевого поведения, мотивации
|
Примечание:
ГАМК - гамма-аминомасляная кислота.
ТГК - тетрагидроканнабинол.
--------------------------------
[1] Дети, подростки и взрослые, пожилые, беременные и кормящие грудью матери
[2] Чай, кофе, какао, энергетические напитки, шоколад, др.
[3] Лекарственные средства от головной боли, простуды, для похудания, добавка к витаминам и пр.)
[4] Психические расстройства и расстройства поведения (F00 - F99). (Класс V МКБ-10, адаптированный для использования в Российской Федерации). Под общей редакцией Казаковцева Б.А., Голланда В.Б. М.: Минздрав России, 1998; 512 с.
[5] Федеральный закон от 08.01.1998 N 3-ФЗ "О наркотических средствах и психотропных веществах"; Постановление Правительства РФ от 30.06.1998 N 681 "Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации" (Собрание законодательства Российской Федерации, 1998, N 27); Постановление Правительства РФ от 04.07.2007 N 427 "О внесении изменений в некоторые постановления Правительства Российской Федерации по вопросам, связанным с оборотом наркотических средств и психотропных веществ".
[6] В разделе "Диагностика" представлены диагностические критерии Международной классификации болезней 10 пересмотра: Психические расстройства и расстройства поведения (F00 - F99). (Класс V МКБ-10, адаптированный для использования в Российской Федерации). Под общей редакцией Казаковцева Б.А., Голланда В.Б. - М.: Минздрав России, 1998; 512 с.
[7] Приказ Минздрава России от 18.12.2015 N 933н "О порядке проведения медицинского освидетельствования на состояние опьянения (алкогольного, наркотического или иного токсического)" (Зарегистрировано в Минюсте России 11.03.2016 N 41390).
[8] Например, некоторые из антипсихотических препаратов обладают обезболивающим действием, что способствует качественной редукции болевых расстройств в структуре СО опиоидов и полностью соответствует рекомендациям ВОЗ по лечению болевых расстройств.
[9] Например, такие проявления, как тревожная ажитация, психопатоподобное поведение, психомоторное возбуждение, суицидальная настроенность, агрессия и др., являются лишь симптомами проявления патологического влечения к наркотику, однако требуют назначения препаратов с соответствующим спектром действия.
[10] По данным American Psychiatric Association (АРА) 1990; Wesson and Smith 1985 (https://www.ncbi.nlm.nih.gov/books/NBK64116/table/A85649/?report=objectonly), с некоторыми изменениями.
[11] ФЗ 61 "Об обращении лекарственных средств" от 12.04.2010 (статья 64); Приказ МЗ РФ от 26 августа 2010 г. N 757н "Об утверждении порядка осуществления мониторинга безопасности лекарственных препаратов для медицинского применения, регистрации побочных действий, серьезных нежелательных реакций, непредвиденных нежелательных реакций при применении лекарственных препаратов для медицинского применения".
[12] Методические рекомендации "Определение степени достоверности причинно-следственной связи "Неблагоприятная побочная реакция-лекарственное средство" (классификация и методы)" (утв. руководителем Федеральной службы по надзору в сфере здравоохранения и социального развития Н.В. Юргелем 2 октября 2008 г.) http: //www.rosminzdravnadzor.ru/.
[13] http: //www.roszdravnadzor.ru/drugs/monitpringlp/documents/547/. Дата обращения: 03.03.2019.
[14] Приказ МЗ РФ от 30 декабря 2015 года N 1034 (зарегистрировано в Минюсте России 22.03.2016 г. N 41495) "Об утверждении порядка оказания медицинской помощи по профилю "психиатрия-наркология" и порядка диспансерного наблюдения за лицами с психическими расстройствами и/или расстройствами поведения, связанными с употреблением психоактивных веществ.